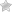Дисциркуляторная энцефалопатия головного мозга (ДЭП)– это такое заболевание, когда мозговая ткань хронически страдает от дефицита кровообращения, питания кислородом.
В МКБ не встречается, термин ДЭП больше применяется для обозначения характерных патологических явлений со стороны мозга. Патология всегда вторична, потому что возникает как реакция на уже имеющиеся проблемы с сосудами. Считается хроническим, восстановить функции мозговой коры до исходного состояния невозможно.
Разобраться, что такое дисциркуляторная энцефалопатия головного мозга, поможет картина, выдаваемая при прохождении МРТ. Методика показывает очаги поражения вещества мозга, скорость их развития.
- атеросклероз мозговых сосудов, из-за холестериновых бляшек, ухудшается проходимость сосудов;
- артериальная гипертензия, причиной которой может стать как сердечная патология, так и более редкие поликистоз почек, болезнь Иценко-Кушинга;
- диабетические изменения;
- черепно-мозговые травмы;
- патология шейных артерий, врожденная или приобретенная вследствие физических травм, заболеваний.
Каждая из причин способствует тому, что кровоток в сосудах мозга сокращается, приводит к кислородному голоданию и образованию очагов некроза. К сожалению, у одного пациента могут иметь место два и больше описанных выше факторов. Это отягощает течение болезни.
При поражении отдельных веточек сосудов, очаги будут сосредоточены в той или иной части мозга (лакунарная, очаговая форма ДЭП). Когда перекрывается просвет крупной артерии, страдает больший объем вещества головного мозга. Такой вариант называется диффузным, распространенным. И встречается чаще.
Выделяют такие стадии дисциркуляторной энцефалопатии на основании темпов прогрессирования и проявившихся симптомов:
- Первая ступень. Преобладание субъективной симптоматики над объективной. Обследование у невролога показывает незначительные отклонения от нормы. Характеризуется как “что-то не то с головой”.
- Вторая ступень. Нарастают когнитивные нарушения (память, логика), больные становятся менее критичными к своему состоянию. Когда им говорят, что нужна помощь, патологию отрицают.
- Третья ступень. Память и интеллект слабеют до уровня деменции. Возникают проблемы с координацией движений. Простые задачи по самообслуживанию становятся невыполнимыми.
Дисциркуляторную энцефалопатию еще делят на типы. Критериями служат проявления поражения соответствующего отдела мозга. Например, при нарушениях равновесия, имеет место вестибулярный тип ДЭП. Нарушения психогенного характера обозначаются как нейроциркуляторный. Головные боли вследствие нарушения оттока крови – венозный тип.
Медицина серьезно относится к проблеме диффузной дисциркуляторной энцефалопатии головного мозга, пытаясь решить, как лечить ее с помощью субкомпенсации и поддерживающей терапии.
Жалобы при дисциркуляторной энцефалопатии (ДЭП) головного мозга даже на начальной стадии указывают на признаки дисфункции мозга и кровеносной системы. Изначально, по причине легкой выраженности, принимаются за легкое недомогание. Такое, которое не требует диагностики и лечения. Подобная особенность приводит к тому, что патология обнаруживается в продвинутых стадиях.
Типичными симптомами ДЭП являются:
- появление вязкости речи;
- нарушения в координации движений, сохранении равновесия;
- головокружения и головные боли;
- тошнота;
- проблемы со сном, при которых днем человек сонный, а ночью страдает от бессонницы;
- ухудшается память;
- замедляется мышление, страдает логика, ухудшается способность обрабатывать новую информацию;
- изменяется характер, возникает раздражительность, немотивированная агрессия.
В обострении, при грубых поражениях мозга, возникает апатичное состояние и депрессия. Больные теряют интерес к своему внешнему виду и контактам с окружающим миром.
В зависимости от стадии и особенностей проявлений, ответить на вопрос «Можно ли остановить развитие дисциркуляторной энцефалопатии из-за хронической анемии или атеросклероза, диабета», врач может по-разному. Прогноз основывается на результатах диагностики и особенностях динамики болезни у конкретного пациента.
Сначала – опрос и осмотр. Обязательно прохождение диагностических проб и процедур. По итогам врач-невролог ставит диагноз умеренно-выраженной или прогрессирующей циркуляторной энцефалопатии головного мозга, определяет, как ее лечить, объясняет, что означают результаты МРТ, определяет по признакам, начальная стадия болезни или она имеет давнюю историю.
Обоснованные выводы делаются после прохождения необходимых диагностических процедур:
- осмотр и опрос со сбором анамнеза, позволяющие выявить возможную первопричину плохого самочувствия;
- базовые анализы крови, мочи;
- МРТ головного мозга, сосудов шеи.
Если первопричина проблем с сосудами не установлена, проводятся дополнительные исследования, выявляющие, почему кровеносная система головы получает недостаточно кислорода.
Это необходимо, так как лечение строится на нейтрализации первопричины и уже после этого на стабилизации состояния пациента.
После этапа диагностики и выявления причины развития заболевания, подбирается комплексное лечение дисциркуляторной сосудистой энцефалопатии головного мозга у взрослых людей.
Лечение кризов, обострений проводится в отделении неврологии, так как симптомы дисциркуляторной энцефалопатии головного мозга могут выражаться как в физиологических проблемах, так и в психиатрических. В фазе ремиссии, минимальных проявлений, лечится в амбулаторных условиях.
Результативной признана комплексная терапия, сочетающая в себе медикаментозные и немедикаментозные способы и приемы.
Действенными физиотерапевтическими методами борьбы с ДЭП, в зависимости от первопричины, считаются:
- лечебная физкультура, комплекс упражнений которой назначается врачом;
- транскраниальная магнитная стимуляция;
- массаж воротниковой зоны;
- иглоукалывание;
- электромиостимуляция;
- вихревые поля.
Параллельно проводится лечение медикаментами:
- диуретиками;
- бета-блокаторами;
- сосудистые средства;
- нейрометаболиты;
- вестибулокорректоры;
- антидепрессанты.
Когда деструктивная энцефалопатия затрагивает масштабные области мозга вследствие перекрытия крупных сосудов, допускается хирургическое вмешательство.
Распространение получили два типа операций:
- Каротидная эндартерэктомия, очищение внутренних стенок сонной артерии при атеросклерозе.
- Стентирование, в этом случае в сосуд вставляется специальный расширитель, улучшающий кровоток в суженной части артерии.
Необходимо понимать, что лечение симптомов и признаков дисциркуляторной энцефалопатии головного мозга у взрослых людей – это замедление развития болезни, остановка патологических процессов. Восстановить пораженные очаги уже невозможно. Как и навсегда излечиться, без опасности снова столкнуться с ухудшением состояния.
ДЭП – хроническое заболевание, требующее регулярного прохождения поддерживающей терапии и изменения образа жизни.
Любой тип: вестибулярный, нейроциркуляторный, циркулярный, венозный, дисфункциональный, деструктивный радикулярный – ДЭП (дисциркуляторной энцефалопатии) без лечения развивается быстро, признаки прогрессируют на глазах. Уже через 2 года ожидается заметное ухудшение симптомов, переход на следующую стадию.
На процесс влияют многие факторы. Патология замедлится, если регулярно проходить курсы лечения, изменить образ жизни соответственно советам невролога, внимательно следить за проявляющимися признаками. Человек, которому поставлен подобный диагноз, не имея других серьезных проблем со здоровьем, способен без серьезных ухудшений прожить 10 лет и даже больше.
Список использованной литературы
Мрт и кт головы и шеи
Медицинский термин «лейкоэнцефалопатия» применяется для определения группы заболеваний, сопровождающихся поражением белого вещества и ряда глубоких структур головного мозга. Быстрое прогрессирование приводит к формированию старческого слабоумия.
У детей встречаются сосудистые разновидности, врожденные формы с длительным хроническим течением. Сроки выживаемости при этом типе больше по сравнению с многоочаговым аналогом.
МР-снимок сосудистой лейкоэнцефалопатии
Для отличия патологии от ряда других нейродегенеративных болезней с аналогичными клиническими симптомами разработана классификация по МКБ 10, где четко выделяют формы нозологии.
Что такое лейкоэнцефалопатия головного мозга
Поражение белого вещества мозга обуславливается в большинстве случаев вирусами. Сосудистая, дисциркуляторная формы обусловлены нарушением кровоснабжения определенного участка головного мозга. Хроническая ишемия обуславливает необратимые изменения.
Клинические симптомы болезни чаще возникают при поражении папилломавирусами. Вероятность нозологии у пациентов с ВИЧ менее 6% по данным статистики МРТ головного мозга в СПб.
Формы сосудистого генеза прогрессируют медленно. Хроническое течение заболевания характеризуется постепенным необратимым поражением ткани. Легкая ишемия провоцирует образование небольших некротических участков. Диффузное расположение приводит к неврологическим расстройствам.
Виды лейкоэнцефалопатии
Самой малоопасной формой является очаговая. Формируется хроническими воспалительными процессами сосудистого генеза. Недостаток микроциркуляции определенного отдела мозга провоцирует гипоксию, нехватку кислорода. Гибель зон белого вещества развивается несколько лет.
Агрессивнее протекают морфологические изменения при гипертонической болезни. Увеличение внутричерепного давления обуславливает разрывы мелких капилляров с участками некроза мозговой паренхимы. Разновидность медицинским языком называется «дисциркулярная энцефалопатия». Появляется у людей старше 55 лет.
Прогрессирующая мультифокальная лейкоэнцефалопатия имеет агрессивное течение. Люди при патологии живут не более 5 лет. Летальные исходы связаны с обширными инфарктами, инсультами.
Классификация видов лейкоэнцефалопатии по МКБ 10
Прогрессирующий вид сосудистого генеза (болезнь Бинсвангера) кодируется символами «I67.3». Из классификации болезней десятого пересмотра исключена субкортикальная деменция с кодом «F01.2».
Прогрессирующая мультифокальная (многоочаговая) лейкоэнцефалопатия – «A81.2». К одноименной группе относится фенилкетонурия, болезнь Александера, Канавана.
Патологии категории «IA» выделяют по причинам, так как имеют аутоиммунное происхождение – обусловлены повреждением тканей иммуноглобулинами собственного организма.
Антитела становятся агрессивными при изменении структуры мембраны или генетической информации клетки под влиянием вирусов, химических, физических факторов.
Рассмотрим полный алгоритм классификации:
- Болезни системы кровоснабжения – «IX. 100-199»;
- Цереброваскулярные заболевания «I60-69»;
- Другие цереброваскулярные болезни – «I67»;
- Прогрессирующая сосудистая лейкоэнцефалопатия – «I67.3»;
- Другие уточненные поражения сосудов – «I67.8».
Международная классификация десятого пересмотра является действующей. При кодировке диагноза нередко встречается дисциркуляторная энцефалопатия, острая цереброваскулярная недостаточность БДУ ишемия мозга (хроническая).
Клинические симптомы мелкоочаговой лейкоэнцефалопатии
Очаговая симптоматика имеет подострое течение. Начальные стадии болезни выявляются неврологами:
- Нарушения зрения, речи;
- Патология иннервации мускулатуры одной половины туловища;
- Приступы эпилепсии;
- Головные боли, головокружение;
- Атаксия, анопсия.
Дифференциальная диагностика очаговых видов проводится для отличия от изменений белого вещества при ВИЧ, деменции. Спинальные очаги протекают без нарушения психических функций. Повреждение белого вещества сопровождается когнитивными расстройствами.
Прогрессирующая мультифокальная лейкоэнцефалопатия
Причина многоочагового повреждения белого вещества – вирус JC, приводящий к распространенному поражению нервной системы. Заболевание развивается на фоне сниженной активности иммунной системы. Антиретровирусное лечение дорогое, поэтому большинство людей погибает.
Прогрессирующая энцефалопатия быстро приводит к разрушению миелина большинства нервных клеток. Изменения необратимы, симптомы постепенно нарастают.
Около 80% населения страны являются носителем полиомавируса человека второго типа, но энцефалопатия не возникает. Только иммунодефициты при СПИДе создают возможности быстрого размножения возбудителя.
Иммунитет пожилых людей не справляется с активность полиомавируса (JC) после иммуномодуляторной или иммуносупрессивной терапии после лечения онкологического новообразования, операций по пересадке органов.
У детей появление патологии наблюдается после начала терапии хронического лимфолейкоза, болезни Ходжкина.
Передается вирус 1С воздушно-капельным или фекально-оральным способом. У большинства населения наблюдается бессимптомное течение. Провоцирующие факторы:
- ВИЧ-инфекция;
- Прием иммунодепрессантов;
- Лимфогранулематоз;
- Лейкозы.
Магнитно-резонансная томография – единственный способ, позволяющий выявить патологические очаги внутри белого вещества. После появления нарушения зрения, дизартрии, гемипареза, афазии неврологи смогут предположить диагноз. Окончательная верификации возможна только после микроскопического обследования биоптатов головного мозга – участки ткани, взятые из места повреждения.
Дисциркулярная энцефалопатия
Хроническое прогрессирующее течение цереброваскулярной патологии сопровождается диффузными многоочаговыми изменениями, приводящими к гемипарезам, ишемическому инсульту, множественным нейропсихологическим и неврологическим расстройствам.
Прогрессирование дисциркуляторной энцефалопатии связано с дегенерацией тканей, накоплением агрессивных метаболитов.
До использования методов нейровизуализации большую часть причин появления когнитивных расстройств специалисты объясняли дисциркуляторной энцефалопатией. Практика показывает гипердиагностику случаев нозологии. Ядерно-магнитный резонанс указывает только 20% случаев встречаемости очагов белого вещества у пожилых пациентов с сосудистыми заболеваниями.
Основным отличием дисциркулярной разновидности в сравнении с инсультом является поражение не крупных мозговых артерий, а мелких пенетрирующих сосудов, артериол. Диффузные повреждения мелких ветвей вызывает ряд морфологических изменений:
- Многочисленные инфаркты (лакунарные);
- Диффузное разрушение белого вещества;
- Смешанная форма.
Раннее выявление любой категории предотвращает прогрессирование после назначения правильной поддерживающей терапии.
Особенности перивентрикулярной и резидуальной лейкоэнцефалопатии у детей
Хронический недостаток поступления кислорода, длительная ишемия мозговых тканей приводит к повреждению подкорковых структур, полушарий, мозгового ствола. Патологические очаги обнаруживаются в глубине серого вещества, сопровождаются изменениями подкорковых волокон.
Перивентрикулярная энцефалопатия характеризуется преимущественной локализацией патологических очагов вокруг желудочков мозга.
Резидуальный вид имеет врожденные и приобретенные причины. Провоцирующим фактором у ребенка являются травматические повреждения черепа, воспалительные процессы внутри черепной коробки. Отдельная разновидность – энцефаломиелопатия возникает из-за аномалий строения сосудистой сети мозга.
Симптомы резидуальной энцефалопатии детей:
- Церебральный паралич;
- Олигофрения;
- Эпилепсия;
- Вегето-сосудистая дистония;
- Неспокойный сон.
Практика показывает наличие латентного течения нозологии у новорожденных с весом около четырех килограмм. Клинические симптомы появляются после начала активного кровоснабжения. Случаи появления слабоумия у дошкольников и школьников связаны с травмами черепной коробки.
Сколько живут с энцефалопатией
Длительность жизни определяется клинической формой болезни, скоростью прогрессирования, индивидуальными изменениями организма человека.
Прогрессирующая многоочаговая энцефалопатия сопровождается летальным исходом через 1-3 года после выявления. Поддерживающая терапия увеличивает выживаемость.
Разновидности сосудистого генеза имеют хроническое прогрессирование. Люди с данной разновидностью при грамотной организации лечения живут десятки лет. Сокращает сроки гипертония, выраженные ишемические очаги структуры головного мозга, кровоизлияния внутрь мозга.
Принципы диагностики лейкоэнцефалопатии
Лучшим способом верификации изменений белого и серого вещества головного мозга является МРТ. Лейкоэнцефалопатия локализуется в головном и спинном мозге.
На снимках визуализируются участки высокой интенсивности диаметром от трех миллиметров до трех сантиметров неправильной округлой и овальной формы.
Расположение очагов в субкортикальных и перивентрикулярных отделах определяет режим Т1 взвешенных последовательностей с дополнительным контрастированием (МР-ангиография). Способ диагностирует атрофию, расширение желудочковых пространств, свежие патологические зоны.
Мультифокальная лейкоэнцефалопатия
МРТ головного мозга при лейкоэнцефалопатии выявляет участки разной интенсивности в мозжечке, стволе, теменно-затылочных и лобных областях. Реже встречается инфратенториальная локализация. Сканирование головного мозга должно сочетаться с обследованием спинномозговой жидкости. Анализ позволяет выявить патологических агентов, являющихся причиной патологии.
Прямое выявление вируса JC, ВИЧ методом ПЦР имеет достоверность близкую к 100%. Если тест отрицательный, подтверждение или исключение диагноза возможно способом биопсии – взятие материала из патологического участка после обнаружения МРТ с трехмерным моделированием.
Обязательна диагностика аутоиммунных состояний, иммунодефицита.
Электронейромиография регистрирует снижение проведения сигнала по слуховым, зрительным, соматосенсорным нервным волокнам. Существует специфические места локализации патологии, выявление которых позволяет предположить патологию с высокой долей вероятности.
Разрушение миелина нервных оболочек, верификация дегенерации аксона – признаки нейродегенеративных процессов. Патологические волны возникают на субклинической стадии до первых выраженных симптомов.
Чтобы выявить патологии вначале развития, следует сделать МРТ. Процедура качественно показывает мягкотканый компонент, насыщенный водой. Жидкость после воздействия магнитным полем начинает резонировать, изменяется радиочастотный сигнал. Регистрация импульса позволяет отобразить графическую картинку на экране монитора после обработки программой.
Что означает лейкоэнцефалопатия головного мозга
Сердце
Лейкоэнцефалопатия головного мозга характеризуется развитием нарушений со стороны белого вещества мозга. Это заболевание изначально описывается в качестве сосудистого слабоумия. Чаще всего этот недуг возникает у людей в пожилом возрасте.
Что такое лейкоэнцефалопатия в области головного мозга? Это прогрессирующее заболевание, как правило, хроническое. С течением времени патологические изменения сопровождаются появлением деменции.
Полное уничтожение нервных клеток происходит вследствие нарушений со стороны процессов кислородного питания и кровоснабжения. Эти факторы способствуют развитию микроангиопатии, что чревато изменением плотности белого вещества. Подобное состояние указывает на то, что в организме присутствуют нарушения процессов циркуляции крови.
Виды лейкоэнцефалопатии
Заболевание может протекать в нескольких разновидностях. В соответствии с формой патологического процесса и назначается лечение.
Мелкоочаговая (сосудистого генеза)
При сосудистой лейкоэнцефалопатии головного мозга происходит медленное поражение полушарий мозга, что сопровождается появлением клинической симптоматики. Возникает эта форма заболевания на фоне гипертонии, сопровождаемой скачками артериального давления.
В группу риска включены мужчины в возрасте от 55 лет. В основном заболевание возникает у тех людей, родственники которых также сталкивались с подобными нарушениями. Патологические изменения со стороны белого вещества со временем приводит к старческому слабоумию.
Что такое лейкоэнцефалопатия сосудистого генеза? Это болезнь, которую специалисты относят к числу цереброваскулярных патологических процессов.
Лейкоэнцефалопатия сосудистая прогрессирующая возникает на фоне следующих причин:
- Атеросклероз. Наличие липидных бляшек является серьезным препятствием движению крови в области мозговых артерий.
- Сахарный диабет. Способствует сгущению крови и, соответственно, затруднению ее движения.
- Патологии позвоночного столба. Возникает вследствие травмы или врожденных факторов и является причиной недостаточного снабжения головного мозга питательными веществами и кислородом.
Что это такое мелкоочаговая лейкоэнцефалопатия сосудистого генеза? Это последствия лишнего веса, злоупотребления алкогольными напитками и курением, нарушения в рационе питания и недостаток физической активности. Наличие факторов риска требует проведения профилактики развития патологических нарушений еще до тех пор, пока не появились симптомы заболевания.
Мультифокальная (прогрессирующая)
Эта форма нарушений со стороны головного мозга представляет собой вирусное поражение нервной системы. Этот процесс сопровождается выраженным разжижением белого вещества. Основные причины возникновения отклонений – снижение иммунитета. Мультифокальная лейкоэнцефалопатия носит агрессивный характер и может стать причиной летального исхода.
Что такое перивентрикулярная лейкоэнцефалопатия? Это развитие когнитивных нарушений, которые могут варьироваться от выраженной деменции до легких дисфункций. При очаговой форме заболевания наблюдается неврологическая симптоматика. Это чревато развитием нарушений речи и зрения.
Не исключена вероятность полной слепоты. Отмечаются отдельные нарушения со стороны двигательной активности, которые со временем приводят к инвалидности.
Чаще всего эта форма заболевания встречается у больных с приобретенным или врожденным иммунодефицитом. В группу риска входят люди, у которых отмечается СПИД или ВИЧ.
Характеризуется поражением подкорковой структуры в области головного мозга. Возникает вследствие хронической ишемии и гипоксии. Развивается в области мозжечка и ствола головного мозга.
Что такое перивентрикулярная лейкоэнцефалопатия? Это поражение двигательных ядер в области продолговатого мозга. Развивается стремительно и сопровождается выраженными нарушениями двигательной активности.
Симптоматика лейкоэнцефалопатии
Чаще всего развитие лейкоэнцефалопатии сопровождается постепенным нарастанием клинической картины. Среди первичных проявлений можно выделить рассеянность, неловкость и апатичность. Человек становится неуклюжим и слезливым. Как правило, происходит снижение умственной работоспособности. Постепенно нарушается сон, возникает раздражительность и мышечный гипертонус.
Обратите внимание! У больного снижается круг интересов, и он с трудом может произносить сложные слова. Если лечение не начато вовремя, то отмечается развитие психоза и невроза. Возникает грубая деменция, и появляются судороги.
Развитие клинической картины:
- Нарушение координации движений и шаткость походки, появление выраженной слабости в области конечностей;
- Возможен односторонний паралич нижних или верхних конечностей;
- Отмечается нарушение речи и зрительных функций;
- Появляются скотомы и гипестезия;
- Снижается интеллект и появляется спутанность сознания;
- Присутствует слабая степень слабоумия и гемианопсия;
- Больной страдает от дисфагии, недержания мочи и эпиприступов.
Очаговая неврологическая симптоматика прогрессирует достаточно быстро. У больного могут присутствовать псевдобульбарный и паркинсонический синдром. При осмотре практически во всех случаях отмечаются сбои со стороны интеллектуально-мнестических функций.
Больной страдает от постуральной неустойчивости. Расстройства со стороны психики сочетаются с постоянным беспокойством, тошнотой, головными болями и онемением конечностей.
Практически во всех случаях больные не воспринимают то, что им требуется помощь, поэтому к врачу их, как правило, приводят родственники.
Постановка диагноза
При развитии мультифокальной прогрессирующей лейкоэнцефалопатии, сосудистой и перивентикулярной форме заболевания, требуется проведение комплексной диагностики, включающей в себя следующие процедуры:
- Консультация и визуальный осмотр на приеме у врача-невролога;
- Забор анализов: кровь, определение уровня наркотических веществ и алкоголя;
- Допплерография, МРТ, КТ, ЭЭГ;
- ПЦР, биопсия головного мозга и люмбальная пункция.
Прогноз заболевания
К большому сожалению, в настоящее время не разработано терапии, которая бы помогла полностью излечиться от лейкоэнцефалопатии. Если меры вообще не приняты, то продолжительность жизни больного составляет не более 6 месяцев с того момента, как появились симптомы поражения центральной нервной системы.
Проведение антивирусного лечения способствует увеличению продолжительности жизни больного до 12 месяцев. В некоторых случаях сроки выживаемости составляют 1,5 года с того момента, как появились первые изменения со стороны мозговых структур.
Сколько живут при острой лейкоэнцефалопатии? Смерть наступает уже через месяц с того момента, как начали развиваться отклонения.
Учитывая тот факт, что развитие любой формы лейкоэнцефалопатии происходит на фоне иммунодефицита, для исключения развития заболевания необходимо соблюдать все возможные меры по ее профилактике. Каждый человек должен заботиться о сохранности защитных сил организма и укреплять их. В обязательном порядке должны быть приняты меры для профилактики ВИЧ и СПИД.
Основные меры:
- Избирательность половых партнеров и использование средств, которые делают половые акты безопасными.
- Отказ от употребления наркотиков.
- Своевременное лечение заболеваний, связанных со скачками артериального давления и закупоркой сосудов.
От чего с возрастом развивается энцефалопатия? Свое мнение рассказал доктор Шишонин
Прогрессирующая мультифокальная энцефалопатия в практике врача-невролога
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) до недавнего времени считалась редким быстро прогрессирующим демиелинизирующим заболеванием ЦНС, вызванным активацией кольцевого вируса рода Polyomavirus семейства Polyomaviridae (полиомавирусов) ― вируса Джона Каннингема (John Cunninghamvirus ― JC-вируса), названного в честь пациента, у которого в 1971 г.
он впервые был обнаружен и носителями которого являются около 80% населения мира [1―2].
Современные данные свидетельствуют, что ПМЛ развивается у лиц со сниженным иммунитетом (у иммунокомпрометированных лиц): при неопластических заболеваниях (лейкемия, болезнь Ходжкина, лимфосаркома, миелопролиферативные заболевания), туберкулезе, саркоидозе, при иммунодефиците, СПИДе, лекарственной иммуносупрессии цитостатиками при пересадке органов или новообразованиях различной локализации [3]. ПМЛ часто встречается при терапии демиелинизирующих заболеваний моно-клональными антителами, возможно также развитие ПМЛ в качестве опасного осложнения в рамках системного воспалительного ревматического заболевания на фоне иммуносупрессивной терапии [4]. В то же время в ряде случаев развитие ПМЛ происходит и при отсутствии тяжелого иммунодефицита. ПМЛ по сути является оппортунистической вирусной инфекцией. Для неврологов актуальность изучения ПМЛ связана с активным использованием иммуносупрессивной терапии и широким распространением ВИЧ-инфекции. После введения в практику высокоактивной антиретровирусной терапии (ВААРТ) частота ПМЛ увеличилась и составила 1,3 на 1000 ВИЧ-инфицированных в год [5].
В клинической практике ранняя диагностика ПМЛ сложна из-за отсутствия выраженной симптоматики, так как инфицирование JC-вирусом происходит в детском возрасте и вирус находится в организме пожизненно [6]. Точное место его персистенции до конца не выяснено ― предположительно, это почки и костный мозг.
При ослаблении иммунитета вирус транспортируется лейкоцитами в ЦНС, где начинает свою репликацию в белом веществе мозга, а точнее, в олигодендроцитах. Разрушение миелиновых оболочек макроскопически проявляется мультифокальной демиелинизацией.
Чаще поражается белое вещество полушарий головного мозга, но возможно поражение мозжечка и серого вещества.
Клинические проявления ПМЛ не имеют специфической картины. Начало появления неврологической и психопатологической симптоматики подострое (несколько дней) или постепенное (несколько недель). Первым развивается быстро прогрессирующий психотический синдром.
Позже присоединяются моно- или гемипарезы, нарушение речи и выпадение полей зрения (гемианопсия). Значительно реже встречаются головная боль, головокружение, атаксия и эпилептические приступы. Характерно отсутствие общеинфекционных и менингеальных симптомов.
На ранних этапах заболевания возникают прогрессирующие когнитивные нарушения, но в отличие от деменции при ВИЧ-инфекции они сопровождаются очаговой неврологической симптоматикой [7]. У пациентов иногда встречается атипичный вариант заболевания (спинальный), который протекает без нарушения психики [8].
Течение вариабельно, летальный исход наступает в течение 6—12 мес [9]. В терминальной стадии заболевания развиваются тяжелая деменция, кома и гибель больного. Наибольшие диагностические трудности возникают при СПИДе, когда клиника и признаки картины МРТ сходны при ПМЛ и ВИЧ-ассоциированной энцефалопатии [10].
В данных случаях только выявление JC-вируса в цереброспинальной жидкости (ЦСЖ) и биоптате головного мозга позволяет установить диагноз.
Постановка диагноза ПМЛ базируется на критериях, рекомендованных Американской академией неврологии в 2013 г. [11] (табл. 1).
Таблица 1. Клинические, лабораторные и МРТ-критерии диагностики ПМЛ
- Иногда для точного подтверждения ПМЛ проводится биопсия ткани мозга с выявлением классической гистопатологической триады: увеличение ядер олигодендроцитов, изменение размеров и формы астроцитов, которые становятся крупными, причудливой формы с гиперхроматическими ядрами.
- Таким образом, алгоритм действий врача при подозрении на ПМЛ состоит из нескольких этапов (рис. 1)
Рис. 1. Алгоритм действия врача при подозрении на ПМЛ. JCV — JC-вирус. [12].
Дифференциальный диагноз ПМЛ в первую очередь необходимо проводить с инфекционными энцефалопатиями (Herpes simplex, вирус CMV, Varicella zoster, Cryptocoсcus, Aspergillus), с лимфомой, с подострым склерозирующим панэнцефалитом. В отличие от вышеназванных инфекций, при ПМЛ нет общеинфекционных и менингеальных симптомов.
С учетом нарастания числа рисков, при которых создаются оптимальные условия для пролиферации JC-вируса под влиянием медикаментозной иммунокоррекции, предложен термин «лекарственная ПМЛ» [13].
У больных рассеянным склерозом, находящихся на терапии натализумабом, необходимо исключить обострение основного заболевания (при МРТ-контроле очаги будут усиленно накапливать контрастное вещество) [14, 15]. Следует также обращать внимание на пациентов, получающих ритуксимаб.
Риск развития ПМЛ у больных, получающих ритуксимаб, составляет 1:8000 [16]. Ритуксимаб — препарат моноклональных антител против CD20 предшественников В-лимфоцитов и зрелых В-лимфоцитов. Разрешен к применению при клеточной неходжкинской лимфоме, резистентном ревматоидном артрите. В 2006 г.
одобрен FDA для лечения системной красной волчанки. В настоящее время для контроля за действием ритуксимаба и выявления побочных эффектов препарата создан специальный проект (Research on Advers Drag Events and Report — RADAR) при участии вирусологов, онкологов, неврологов и других специалистов [17]. В начале 2014 г.
Федеральная служба по надзору в сфере здравоохранения Российской Федерации опубликовала письмо, в котором сообщалось о 2 случаях ПМЛ у пациентов с системной красной волчанкой, получавших белимумаб в пострегистрационном периоде1.
В 2015 г. L. Calabrese и соавт. [18] предложили условную градацию рисков, разработанную для лекарственной ПМЛ. В 1-й класс были включены натализумаб и эфализумаб (снят с производства) как препараты, обладающие высоким риском развития ПМЛ (1/10 000—1/100).
Ко 2-му классу (низкий риск) отнесены ритуксимаб, белимумаб, азатиоприн, микофенолатамофетил, метотрексат. В 3-й класс (очень низкий риск) вошли ингибиторы фактора некроза опухоли-α (иФНО-α), абатацепт, тоцилизумаб, анакинра, устекинумаб и тофацитиниб.
Использование этих препаратов требует особого тщательного наблюдения за пациентами и необходимости информирования их о риске развития ПМЛ.
Специфическая терапия ПМЛ до настоящего времени не разработана. Для лечения применяются следующие препараты: противовирусные средства, цитостатики, антагонисты серотониновых рецепторов, ВААРТ-терапия у ВИЧ-инфицированных больных [19]. При развитии этой патологии целесообразно максимально снизить дозу глюкокортикоидов и цитостатических препаратов.
Описан положительный эффект от сочетания плазмафереза (5 сеансов через день) с последующим приемом аминохинолинового препарата мефлоцина и миртазапина (антидепрессант, ингибитор обратного захвата серотонина, замедляющий распространение JC-вируса путем блокирования специфических рецепторов) [19].
Очень часто проводится симптоматическая терапия (противоотечная, нейропротективная, антиоксидантная).
Таким образом, ПМЛ — это заболевание, которое может встретиться в практике врача-невролога. Оно может имитировать острое нарушение мозгового кровообращения (ОНМК), хроническую ишемию головного мозга с выраженными когнитивными нарушениями. Клиницисту следует постоянно помнить, что развитие этой патологии возможно у пациентов с демиелинизирующими заболеваниями, ВИЧ, нейроинфекциями.
Приводим данные собственных наблюдений.
Наблюдение 1.
Пациент А., 35 лет. Поступил в ГКБ № 15 им. О.М. Филатова по направлению скорой медицинской помощи (СМП) с диагнозом ОНМК. При поступлении предъявлял жалобы на дезориентацию в пространстве, эмоциональную лабильность, снижение памяти на текущие события.
Анамнез жизни: женат, имеет двоих здоровых детей. Курит с 17 лет. Два года назад, после командировки в Таиланд, резко похудел, это связывал с переходом на «здоровый образ жизни»: сбалансированное питание, усиленные тренировки. Стал чаще болеть простудными заболеваниями. К врачам не обращался.
Анамнез заболевания: со слов пациента и его жены, около 6 мес назад перенес правостороннюю бронхопневмонию (диагностирована при проведении КТ легких).
Лейкоэнцефалопатия
- Лейкоэнцефалопатия (энцефалопатия Бинсвангера, болезнь Бинсвангера) – это вид сосудистой деменции (старческого слабоумия), при котором происходит разрушение белого вещества головного мозга.
- Факторы риска
- СПИД;
- снижение иммунитета вследствие лечения иммунодепрессантами (например, после операции по пересадке органа);
- лейкоз (рак крови);
- лимфогранулематоз (злокачественная опухоль в лимфатической системе);
- хроническая артериальная гипертензия;
- туберкулез;
- саркоидоз (системное заболевание, при котором в различных органах образуются специфические гранулемы);
- карцинома (злокачественная опухоль в клетках эпителия кожи или внутренних органов).
Причины лейкоэнцефалопатии Поражение вирусом JC (JCV, полиомавирус человека) на фоне остро ослабленного иммунитета.
Симптомы лейкоэнцефалопатии:
- гемипарезы (асимметричное ослабление двигательной сферы);
- атаксия (нарушение координации движений);
- афазия (системные нарушения речи);
- дизартрия (нарушения словопроизношения);
- нарушения чувствительности;
- расстройства зрения;
- распад интеллектуальной сферы, прогрессирующее слабоумие;
- спутанность сознания;
- изменения личности (эмоций, мотивов и т.д.);
- дисфагия (нарушение акта глотания);
- нарастающая физическая слабость;
- головные боли;
- эпилептические припадки.
Диагностика лейкоэнцефалопатии
- консультация невролога, инфекциониста;
- компьютерная томография головного мозга;
- магнитно-резонансная томография головного мозга;
- электроэнцефалография;
- биопсия головного мозга (выявление вируса).
Лечение лейкоэнцефалопатии Лечение симптоматическое. Эффективных препаратов для борьбы с вирусом JC не разработано.
Прогноз Прогноз в целом неблагоприятный, однако иногда встречаются спонтанные улучшения. При лейкоэнцефалопатии неврологические нарушения необратимы из-за деструктивных изменений в центральной нервной системе. При остром течении летальный исход наступает в течение одного месяца.
Точно установить продолжительность жизни больного лейкоэнцефалопатией сложно, т.к. симптомы появляются стерто на фоне соматического заболевания.
Профилактика лейкоэнцефалопатии Специфической профилактики не существует.