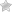Гипертиреоз — это патология, заключающаяся в избыточной секреции гормонов щитовидной железы.
Болезнь вызывает довольно неприятные симптомы, а также приводит к тяжелым осложнениям, наиболее опасное из которых — кризис щитовидной железы. Узнайте, каковы причины и симптомы гипертиреоза и как он лечится.
Причины гипертиреоза
Щитовидная железа отвечает за секрецию трийодтиронина (Т3) и тироксина (Т4), которые очень важны, поскольку влияют на функционирование большинства тканей организма.
Эти гормоны также связаны с обменом веществ и выработкой энергии.
Функционирование органа контролируется гипофизом, который, в свою очередь, выделяет тиреотропный гормон (TSH) и стимулирует щитовидную железу к выделению гормонов T3 и T4.
Гипертиреоз (hyperthyreosis, гипертиреоидизм) возникает, когда щитовидная железа выделяет избыточное количество гормонов тироксина (Т4), трийодтиронина (Т3) и кальцитонина. Последствие избытка гормонов щитовидной железы в организме — тиреотоксикоз.
Причины гипертиреоза могут включать: тяжелую психологическую травму (например, беспокойство, гнев), беременность, сексуальную дисфункцию, гормональные нарушения менопаузы, острые или хронические инфекционные заболевания.
Эти раздражители обычно работают по схеме: кора головного мозга — гипоталамус — передняя доля гипофиза. Таким образом, повышенная выработка гормона щитовидной железы провоцирует симптомы гипертиреоза.
Наиболее распространенные причины, вызывающие гипертиреоз
Причины гормонального сбоя:
- болезнь Грейвса, когда собственные антитела стимулируют выработку гормонов щитовидной железы;
- узловой зоб, диффузный зоб;
- воспаление щитовидной железы: хронический аутоиммунный тиреоидит (начальная фаза болезни Хашимото), подострый тиреоидит (начальная фаза болезни Кервена);
- потребление чрезмерного количества йода, например, в добавках;
- чрезмерные дозы гормонов щитовидной железы (факт тиреотоксикоза);
- опухоли гипофиза, которые выделяют ТТГ;
- опухоли трофобласта.
Редкие причины гипертиреоза включают: подострый тиреоидит (заболевание, связанное с предшествующей вирусной инфекцией) и послеродовой тиреоидит.
Фактором риска является женский пол, так как гипертиреоз диагностируется у женщин в пять раз чаще, чем у мужчин.
Типы гипертиреоза
В зависимости от того, развивается ли гипертиреоз без предшествующих изменений в щитовидной железе или на основе простого зоба, мы говорим о первичном или вторичном гипертиреозе.
В дополнение к этому также различаются формы гипертиреоза, при которых встречаются только некоторые симптомы, причем в различной степени.
Пример первичного гипертиреоза — болезнь Грейвса, связанная с повышением гормональной активности железы. Это вызвано, среди прочего, производством антител, стимулирующих щитовидную железу к выработке гормонов.
Симптомы гипертиреоза
Гипертиреоз характеризуется гипертрофией железы, сопровождающейся учащением пульса.
Характерные симптомы расстройства:
- Гиперчувствительность к теплу и чрезмерное потоотделение. Из-за ускоренного обмена веществ организм вырабатывает больше тепла. Характерный симптом — у пациента постоянно мокрые руки. Человек с гипертиреозом плохо переносит жаркую погоду, зимой не замерзает, поэтому одевается относительно легко. Пациенты испытывают жажду независимо от погоды и времени года.
- Раздражительность, нервозность. Из-за этого человек часто не может выполнить свои обязанности, получает замечания, ему трудно сосредоточиться.
- Тремор пальцев. Он может быть настолько сильным, что больному трудно держать в руке ручку, застегнуть пуговицу. Иногда пациент обращается за помощью к неврологу, предполагая развитие болезни Паркинсона
- Сильное сердцебиение. Опасный симптом, приводящий к мерцательной аритмии и сердечной недостаточности. Чтобы узнать состояние сердца, нужно проходить ЭКГ.
- Слабость в мышцах ног. Может быть настолько сильной, что трудно подниматься по лестнице или вставать со стула
- Кожные заболевания. Красные, зудящие пятна могут появиться на голенях и ступнях, а ноги над лодыжками могут опухать.
- Плохое состояние волос и ногтей. Волосы становятся тонкими и редкими, их трудно укладывать. Ногти ломкие, имеют неровную поверхность и темнеют. При этом симптоме нужна консультация дерматолога, чтобы узнать, является ли щитовидная железа единственной причиной проблемы.
- Одышка. Появляется даже после небольших физических нагрузок.
- Нерегулярные менструации. При гипертиреозе могут быть скудными или полностью исчезнуть. Симптом требует контроля гинеколога.
- Расстройства пищеварения. Возможно появление диареи (следствие быстрого метаболизма), но чаще встречаются запоры.
- Слезотечение. Слезы появляются на ветру и ярком свете. Глаза могут болеть с ощущением песка под веками. Изображение иногда размыты или двоятся. Для облегчения состояния, после консультации с врачом можно использовать капли — искусственные слезы, а в солнечные дни рекомендуется ношение темных очков.
- Потеря веса.
Гипертиреоз также может давать скудные, едва заметные симптомы — это субклинический (скрытый) гипертиреоз.
Лабораторные тесты показывают увеличение скорости основного обмена и перепроизводство гормонов щитовидной железы. Симптомы у пациентов могут отличаться.
Какой врач лечит гипертиреоз
Заметив симптомы, указывающие на гипертиреоз, нужно обратиться к эндокринологу, который проведет опрос и обследование, а затем решит, что делать.
Обследование при гипертиреозе
Первым проводится анализ на определение уровня ТТГ. Это базовое обследование уже позволяет врачу заподозрить заболевание щитовидной железы. По мнению врачей, именно ТТГ является наиболее чувствительным показателем секреции гормонов щитовидной железой. Результат ниже нормы указывает на гипертиреоз, то есть чрезмерное производство гормонов.
Если результат этого теста плохой, сдаются анализы на свободный гормон щитовидной железы (FT4 и / или FT3). Результаты теста могут отличаться в зависимости от аналитического метода, поэтому стоит проводить дальнейшие анализы в той же лаборатории и во время лечения.
В результате чрезмерной выработки гормонов часто образуются «холодные» (негормональные) и «горячие» (активные) узелки. Оба угрожают злокачественным новообразованием, но рак чаще возникает на базе активных узлов.
Обязательно проводится УЗИ щитовидной железы. Сдаются анализы крови на антитела. При наличии узлов назначаются рентген, сцинтиграфия щитовидной железы или тонкоигольная биопсия (БАК). Эти тесты позволяют определить тип и размер узелков.
- УЗИ щитовидки. Выявляет поражения щитовидной железы, когда речь идет о болезни Грейвса. На изображении пораженная область имеет сниженную эхогенность.
- Анализы крови на антитела. Выявляются, например, антитела против рецептора TSH (TSHR). Высокие уровни антител против TSHR характерны для болезни Грейвса.
- Аспирационная тонкоигольная биопсия. Представляет собой взятие клеток щитовидки на анализ. Дает ответ на вопрос, являются ли узлы злокачественными или нет.
- Рентген. Изображение показывает, растет ли щитовидная железа в направлении трахеи, создавая так называемый загрудинный зоб. Образование затрудняет дыхание.
- Сцинтиграфия. Позволяет поставить точный диагноз. Пациенту дают радиоактивный йод в капсуле или жидкости. Йод попадая в щитовидную железу, дает излучение, регистрируемое гамма-камерой. Горячие узелки поглощают йод, холодные — нет. На мониторе врач видит те места, которые поглотили йод, и те, в которых его нет. Так создается карта щитовидной железы — сцинтиграфия.
УЗИ щитовидной железы
Лечение гипертиреоза
Чтобы восстановить нормальную функцию гормонов щитовидной железы у людей с гипертиреозом, необходимо обеспечить им душевное спокойствие, устранить все источники конфликтов и эмоций, создать благоприятные условия окружающей среды.
Медикаментозное лечение включает фармакологические препараты, блокирующие или подавляющие чрезмерное производство гормонов, обусловливающих набор клинических симптомов. Тип медикаментозного лечения гипертиреоза, доза препарата и продолжительность применения определяются и меняются эндокринологом каждый раз после обследования и получения новых результатов анализов.
В некоторых случаях используется изотопное или хирургическое лечение.
Лечение гипертиреоза зависит от:
- причины;
- возраста больного;
- степени тяжести;
- наличия других заболеваний.
Поэтому метод лечения подбирается врачом индивидуально. Основное условие получения лечебного эффекта — его регулярность.
Врач подбирает и назначает:
- Препараты: бета-блокаторы и тиреостатики, уменьшающие секрецию гормонов. В эту группу препаратов включены тиамазол и пропилтиоурацил. Эти препараты отвечают за ингибирование выработки гормонов щитовидной железы, и их действие проявляется примерно через 2-4 недели использования. Тиростаты облегчают симптомы: дрожание рук или учащенное сердцебиение. Доза препарата определяется врачом индивидуально. Использование тиреостатиков может привести к побочным эффектам в виде: боли в суставах или зуда кожи. В этих случаях следует изменить дозировку или (в некоторых случаях) прекратить прием. Опасное осложнение — агранулоцитоз — уменьшение количества нейтрофилов (тип лейкоцитов) в сыворотке крови из-за обратимого токсического повреждения костного мозга, которое исчезает только после отмены препарата, но требует тщательного медицинского наблюдения. Во время этого осложнения организм теряет устойчивость к инфекции. Внимание! Если у вас повышенная температура, боль в горле или общая слабость, немедленно обратитесь в клинику, чтобы проверить морфологию мазка.
- Введение радиоактивного йода. Пероральное лечение радиоактивным йодом вызывает медленное и необратимое разрушение клеток щитовидной железы, которые захватывают сывороточный йод. Для получения результата требуется несколько месяцев лечения. Радиоактивный йод нельзя давать беременным или кормящим грудью женщинам. В течение как минимум полугода после окончания лечения нельзя планировать беременность.
- Оперативное лечение.
Медицинский центр Prima Medica
развивается при поражении каудальных отделов ствола головного мозга (продолговатый мозг) или его связей с исполнительными аппаратами.
Функции продолговатого мозга многообразны и имеют витальное значение. Ядра IX, X и XII нервов являются центрами контроля рефлекторной деятельности глотки, гортани и языка и участвуют в обеспечении артикуляции и глотания.
Они получают интероцептивную информацию и имеют отношение ко многим висцеральным рефлексам (кашель, глотание, чихание, слюноотделение, сосание) и различным секреторным реакциям.
В продолговатом мозге проходит медиальный (задний) продольный пучок, имеющий важное значение в регуляции движений головы и шеи и координации последних с движениями глаз. Он содержит релейные ядра слуховых и вестибулярных проводников.
Через него проходят восходящие и нисходящие пути, связывающие ниже- и вышележащие уровни нервной системы.
Ретикулярная формация играет важную роль в облегчении или подавлении моторной активности, регуляции мышечного тонуса, проведении афферентации, в постуральной и другой рефлекторной активности, в контроле сознания, а также висцеральных и вегетативных функций. Кроме того через систему вагуса продолговатый мозг участвует в регуляции дыхательных, кардиоваскулярных, дигестивных и других метаболических процессов в организме.
Здесь мы рассмотрим развёрнутые формы бульбарного паралича, развивающиеся при двусторонних поражениях ядер IX, X и XII нервов, а также их корешков и нервов внутри и вне черепа. Сюда же мы отнесли поражения соответствующих мышц и синапсов, которые приводят к тем же нарушениям бульбарных двигательных функций: глотания, жевания, артикуляции, фонации и дыхания.
Причины бульбарного синдрома
- Болезни моторного нейрона (боковой амиотрофический склероз, спинальная амиотрофия Фацио-Лонде, бульбоспинальная амиотрофия Кеннеди).
- Миопатии (окулофарингеальная, синдром Кирнса-Сейра).
- Дистрофическая миотония.
- Пароксизмальная миоплегия.
- Миастения.
- Полинейропатия (Гийена-Барре, поствакцинальная, дифтерийная, паранеопластическая, при гипертиреозе, порфирии).
- Полиомиелит.
- Процессы в стволе головного мозга, задней черепной ямке и кранио-спинальной области (сосудистые, опухолевые, сирингобульбия, менингиты, энцефалиты, грануломатозные заболевания, костные аномалии).
- Психогенная дисфония и дисфагия.
Болезни моторного нейрона
Конечная стадия всех форм бокового амиотрофического синдрома (БАС) или начало его бульбарной формы относятся к типичным примерам нарушения бульбарных функций. Обычно болезнь начинается с двустороннего поражения ядра XII нерва и её первыми проявлениями являются атрофия, фасцикуляции и паралич языка.
На первых этапах может иметь место дизартрия без дисфагии или дисфагия без дизартрии, но довольно быстро наблюдается прогрессирующее ухудшение всех бульбарных функций.
В начале болезни затруднение глотания жидкой пищи наблюдается чаще, чем твёрдой, но по мере прогрессирования заболевания развивается дисфагия и при приёме твёрдой пищи. При этом к слабости языка присоединяется слабость жевательных а затем и лицевых мышц, мягкое нёбо свисает, язык в полости рта неподвижен и атрофичен.
В нём видны фасцикуляции. Анартрия. Постоянное слюнотечение. Слабость респираторных мышц. В этой же области или в других регионах тела выявляются симптомы вовлечения верхнего мотонейрона.
Критерии диагноза бокового амиотрофического склероза
- наличие знаков поражения нижнего мотонейрона (включая ЭМГ — подтверждение переднерогового процесса в клинически сохранных мышцах); клинические симптомы поражения верхнего мотонейрона (пирамидный синдром); прогрессирующее течение.
«Прогрессирующий бульбарный паралич» сегодня рассматривается как один из вариантов бульбарной формы бокового амиотрофического склероза (точно так же как «первичный боковой склероз» как другая разновидность бокового амиотрофического склероза, протекающая без клинических знаков поражения передних рогов спинного мозга).
Нарастающий бульбарный паралич может быть проявлением прогрессирующей спинальной амиотрофии, в частности — терминальной стадии амиотрофии Вердниг-Гофмана (Werdnig-Hoffmann), а у детей — спинальной амиотрофии Фацио-Лонде (Fazio-Londe).
Последняя относится к аутосомно-рецессивным спинальным амиотрофиям с дебютом в раннем детском возрасте. У взрослых известна Х-сцепленная бульбарная спинальная амиотрофия, начинающаяся в возрасте 40 лет и старше (болезнь Кеннеди {Kennedy}).
Характерны слабость и атрофии мышц проксимальных отделов верхних конечностей, спонтанные фасцикуляции, огранические объёма активных движений в руках, снижение сухожильных рефлексов с двуглавой и трёхглавой мышц плеча.
По мере прогрессирования заболевания развиваются бульбарные (как правило, негрубые) расстройства: попёрхивание, атрофия языка, дизартрия. Мышцы ног вовлекаются позже. Характерные особенности: гинекомастия и псевдогипертрофия икроножных мышц.
При прогрессирующих спинальных амиотрофиях процесс ограничивается поражением клеток передних рогов спинного мозга. В отличие от бокового амиотрофического склероза здесь процесс всегда симметричен, он не сопровождается симптомами вовлечения верхнего мотонейрона и имеет более благоприятное течение.
Миопатии
Некоторые формы миопатий (окулофарингеальная, синдром Кирнса-Сейра) могут проявляться нарушением бульбарных функций.
Окулофарингеальная миопатия (дистрофия) — наследственное (аутосомно-доминантное) заболевание, особенностью которого является поздний дебют (обычно после 45 лет) и мышечная слабость, которая ограничивается мышцами лица (двусторонний птоз) и бульбарной мускулатурой (дисфагия).
Птоз, нарушения глотания и дисфония медленно прогрессируют. Основной дезадаптирующий синдром — дисфагия. На конечности процесс распространяется лишь у некоторых больных и в поздних стадиях заболевания.
Одна из форм митохондриальной энцефаломиопатии, а именно синдром Кирнса-Сейра («офтальмоплегия плюс») проявляется, помимо птоза и офтальмоплегии, миопатическим симптомокомплексом, который развивается позже глазных симптомов. Вовлечение бульбарной мускулатуры (гортани и глотки) обычно не бывает достаточно грубым, но может приводит к изменению фонации и артикуляции, поперхиваниям.
Облигатные признаки синдрома Кирнса-Сейра:
- наружная офтальмоплегия
- пигментная дегенерация сетчатки
- нарушения проводимости сердца (брадикардия, атриовентрикулярная блокада, синкопы, возможна внезапная смерть)
- повышение уровня белка в ликворе
Дистрофическая миотония
Дистрофическая миотония (или миотоническая дисторофия Россолимо-Куршмана-Штейнерта-Баттена) наследуется по аутосомно-доминантному типу и поражает мужчин в 3 раза чаще женщин. Её дебют приходится на возраст 16-20 лет.
Клиническая картина складывается из миотонического, миопатического синдромов и внемышечных расстройств (дистрофические изменения в хрусталике, яичках и других эндокринных железах, коже, пищеводе, сердце и иногда в головном мозге).
Миопатический синдром максимально выражен в мышцах лица (жевательные и височные мышцы, что приводит к характерному выражению лица), шеи и у некоторых больных — в конечностях. Поражение бульбарных мышц приводит к носовому оттенку голоса, дисфагии и поперхиваниям и иногда — к дыхательным расстройствам (в том числе к апноэ во время сна).
Пароксизмальная миоплегия (периодический паралич)
Пароксизмальная миоплегия — заболевание (гипокалиемическая, гиперкалиемическая и нормокалиемическая формы), проявляющееся генерализованными или парциальными приступами мышечной слабости (без потери сознания) в виде парезов или плегии (вплоть до тетраплегии) со снижением сухожильных рефлексов и мышечной гипотонией.
Продолжительность приступов вариирует от 30 минут до нескольких суток. Провоцирующие факторы: богатая углеводами обильная пища, злоупотребление поваренной солью, отрицательные эмоции, физические нагрузки, ночной сон. Лишь в некоторых приступах отмечается вовлечение шейных и краниальных мышц.
Редко в процесс вовлекается в той или иной степени дыхательная мускулатура.
Дифференциальный диагноз проводят с вторичными формами миоплегии, которые встречаются у больных тиреотоксикозом, при первичном гиперальдостеронизме, гипокалиемии при некоторых желудочно-кишечных заболеваниях, болезнях почек. Описаны яттрогенные варианты периодического паралича при назначении препаратов, способствующих выведению калия из организма (диуретики, слабительные, лакричник).
Миастения
Бульбарный синдром — одно из опасных проявлений миастении. Миастения (myasthenia gravis) — заболевание, ведущим клиническим проявлением которого является патологическая мышечная утомляемость, уменьшающаяся вплоть до полного восстановления после приёма антихолинестеразных препаратов.
Первыми симптомами чаще бывают нарушения функций глазодвигательных мышц (птоз, диплопия и ограничение подвижности глазных яблок) и лицевой мускулатуры, а также мышц конечностей. Примерно у одной трети больных наблюдается вовлечение жевательных мышц, мышц глотки, гортани и языка.
Существуют генерализованные и локальные (главным образом глазная) формы.
Дифференциальный диагноз миастении проводят с миастеническими синдромами (синдром Ламберта-Итона, миастенический синдром при полиневропатиях, комплекс миастения-полимиозит, миастенический синдром при ботулинической интоксикации).
Полинейропатии
Бульбарный паралич при полинейропатиях наблюдается в картине генерализованного полинейропатического синдрома на фоне тетрапареза или тетраплегии с характерными чувствительными нарушениями, что облегчает диагностику природы бульбарных расстройств.
Последние характерны для таких форм как острая демиелинизирующая полинейропатия Гийена-Барре, постинфекционные и поствакцинальные полинейропатии, дифтерийная и паранеопластическая полинейропатия, а также полинейропатия при гипертиреозе и порфирии.
Полиомиелит
Острый полиомиелит, как причина бульбарного паралича, распознаётся по наличию общеинфекционных (предпаралитических) симптомов, быстрому развитию параличей (обычно в первые 5 дней болезни) с большим поражением проксимальных отделов, чем дистальных. Характерен период обратного развития параличей вскоре после их появления.
Выделяют спинальную, бульбарную и бульбоспинальную формы. Чаще поражаются нижние конечности (в 80 % случаев), но возможно развитие синдромов по гемитипу или перекрёстно. Параличи носят вялый характер с выпадением сухожильных рефлексов и быстрым развитием атрофии.
Бульбарный паралич может наблюдаться при бульбарной форме (10-15 % от всей паралитической формы заболевания), при которой страдают ядра не только IХ, Х (реже XII) нервов, но и лицевой нерв. Поражение передних рогов IV-V сегментов может вызвать паралич дыхания. У взрослых чаще развивается бульбоспинальная форма.
Вовлечение ретикулярной формации ствола мозга может приводить к кардио-васкулярным (гипотензия, гипертензия, аритмии сердца), респираторным («атактическое дыхание») нарушениям, расстройствам глотания, нарушениям уровня бодрствования.
Дифференциальный диагноз проводится с другими вирусными инфекциями, способными поражать нижний мотонейрон: бешенство и herpes zoster. Другие болезни, часто требующие дифференциального диагноза с острым полиомиелитом: синдром Гийена-Барре, острая интермиттирующая порфирия, ботулизм, токсические полиневропатии, поперечный миелит и острая компрессия спинного мозга при эпидуральном абсцессе.
Процессы в стволе головного мозга, задней черепной ямке и краниоспинальной области
Некоторые заболевания иногда легко вовлекают обе половины продолговатого мозга, учитывая маленький размер и компактную форму каудальной части ствола мозга: опухоли интрамедуллярного (глиомы или эпендимомы) или экстрамедуллярного характера (нейрофибромы, менингиомы, гемангиомы, метастатические опухоли); туберкулёма, саркаидоз и другие грануломатозные процессы могут напоминать клинические симптомы опухоли. Объёмные процессы рано или поздно сопровождаются повышением внутричерепного давления. Паренхиматозные и субарахноидальные кровоизлияния, черепно-мозговая травма и другие процессы, сопровождающиеся внутричерепной гипертензией и вклинением продолговатого мозга в foramen magnum, могут приводить к гипертермии, дыхательным нарушениям, коматозному состоянию и смерти больного от остановки дыхания и сердца. Другие причины: сирингобульбия, врождённые нарушения и аномалии краниоспинальной области (платибазия, болезнь Педжета), токсические и дегенеративные процессы, менингиты и энцефалиты, приводящие к дисфункции каудальных отделов ствола головного мозга.
Психогенная дисфония и дисфагия
Психогенные расстройства бульбарных функций иногда требуют проведения дифференциального диагноза с истинным буль-барным параличом. Психогенные расстройства глотания и фонации могут наблюдаться как в картине психотических нарушений, так и в рамках конверсионных расстройств.
В первом случае они обычно наблюдаются на фоне клинически очевидных нарушений поведения, во втором — они редко являются моносимптомным проявлением заболевания и в таком случае их распознавание облегчается выявлением полисиндромных демонстративных расстройств.
Необходимо использование как позитивных критериев диагностики психогенных нарушений, так и исключения органических заболеваний с применением современных параклинических методов обследования.
Диагностические исследования при бульбарном синдроме
Общий и биохимический анализ крови; общий анализ мочи; КТ или МРТ головного мозга; ЭМГ мышц языка, шеи и конечностей; клинические и ЭМГ-пробы на миастению с фармакологической нагрузкой; осмотр окулиста; ЭКГ; исследование ликвора; эзофагоскопия; консультация терапевта.
Все новости Предыдущая Следующая
Псевдобульбарный синдром
Псевдобульбарный синдром развивается при нарушении высшей регуляции моторных нервных ядер в продолговатом мозге (bulbus cerebri). Это центры 9, 10 и 12 пар черепно-мозговых нервов. Многие нервные пути в головном мозге имеют частичный или полный перекрест.
Поэтому полное исчезновение контролирующих импульсов возможно при двустороннем поражении лобных отделов коры головного мозга или при обширном повреждении корково-ядерных, подкорковых нервных путей.
Поэтому, оставшиеся без центрального регулирования ядра начинают работать автономно, что вызывает следующие явления:
- Дисфония (глухой, низкий, тихий голос)
- Дисфагия (нарушение глотания)
- Дизартрия (нарушение артикуляции, речь нечеткая)
- Непроизвольные стереотипные гримасы с имитацией эмоциональных реакций (насильственный плач, значительно реже смех)
- Активируются глубокие безусловные рефлексы орального автоматизма, которые в норме могут быть обнаружены только у младенцев
- Сохраняется функция дыхательных мышц и сердца, то есть жизненно важные акты остаются неизменными;
В формировании таких изменений принимают участие сами ядра продолговатого мозга, мозжечок, ствол мозга, лимбическая система и множество путей между отдельными подкорковыми структурами головного мозга.
Причины псевдобульбарного синдрома:
-
- сосудистые заболевания, поражающие обе гемисферы головного мозга (васкулит, атеросклероз, гипертонические лакунарные инфаркты мозга);
- черепно-мозговые травмы;
- повреждение головного мозга из-за тяжелой гипоксии;
- эпилептоформный синдром у детей (может произойти единичный эпизод паралича);
- демиелинизирующие расстройства;
- болезнь Пика;
- билатеральный перисильвиев синдром;
- мультисистемная атрофия;
- внутриутробная патология или родовая травма у новорожденных детей;
- генетические нарушения (латеральный амиотрофический склероз, оливопонтоцеребеллярные дегенерации, болезнь Крейтцфельдта – Якоба, семейная спастическая параплегия и др.);
- болезнь Паркинсона;
- глиома;
- неврологические состояния после воспаления мозга и его оболочек.
Чаще всего псевдобульбарный синдром развивается при хронических прогрессирующих заболеваниях, но он может возникнуть и при остром кислородном голодании обширных зон головного мозга. Псевдобульбарный синдром характеризуется сочетанием нарушения глотания, речи, появлением насильственных гримас (смеха и плача) и симптомов орального автоматизма.
Появление поперхивания и пауз перед началом глотания объясняется парезом (слабостью) мышц глотки и мягкого неба. При этом нарушения симметричные и не столь грубы, как при бульбарном параличе. Отсутствуют явления атрофии и подергиваний пораженных мышц. А глоточный рефлекс сохранен или даже повышен.
Нарушения речи при псевдобульбарном синдроме касается только произношения – речь становится нечеткой, смазанной дизартричной. Причина в параличе или спастическом тонусе мышц. Кроме того, голос становится глухим, тихим — дисфония. В состав синдрома всегда входят симптомы орального автоматизма.
Сам пациент может их не замечать, эти признаки обнаруживаются при неврологическом осмотре. Легкое раздражение определенных зон приводит к сокращению подбородочных или периоральных мышц. Эти движения напоминают сосание или поцелуй. К примеру, такая реакция появляется после прикосновения к ладони или углу рта, при постукивании по спинке носа.
А при легком ударе по подбородку сокращаются жевательные мышцы, закрывая приоткрытый рот. Характерно возникновение насильственного плача, реже смеха. Так называют характерные кратковременные сокращения мимических мышц, сходные с эмоциональными реакциями.
Эти непроизвольные гримасы не связаны с какими-либо впечатлениями, не могут быть прекращены усилием воли. Нарушаются и произвольные движения лицевой мускулатуры, из-за чего человек может открывать рот при просьбе зажмурить глаза.
Псевдобульбарный синдром не является изолированным проявлением заболевания, он возникает в рамках неврологического заболевания, явившегося его причиной. Общая клиническая картина зависит от вида патологии. Например, для поражения лобных долей характерны эмоционально-волевые нарушения.
Человек при этом может становиться малоактивным, безынициативным или, наоборот, расторможенным в своих желаниях. Дизартрия часто сочетается со снижением памяти и речевыми расстройствами (афазией). При поражении подкорковых зон нередко возникают разнообразные двигательные нарушения.
Лечение
Так как псевдобульбарный синдром является следствием определенного заболевания, то в первую очередь необходимо лечить основную патологию.
Если это гипертоническая болезнь, дисциркуляторная энцефалопатия, последствия инсультов, назначают гипотензивную и сосудистую терапию.
При специфических васкулитах (сифилитическом, туберкулезном) обязательно используют противомикробные средства, антибиотики. При этом лечение может проводиться совместно с узкими специалистами – дерматовенерологом или фтизиатром.
Помимо специализированной терапии назначаются препараты для улучшения микроциркуляции в головном мозге, нормализации работы нервных клеток и улучшения передачи нервных импульсов. Для этого используются различные сосудистые, метаболические и ноотропные средства, антихолинэстеразные препараты.
Нет универсального средства для лечения псевдобульбарного синдрома. Врач подбирает индивидуальную схему комплексной терапии с учетом всех имеющихся нарушений.
При этом в дополнение к медикаментозному лечению могут быть использованы специальные упражнения для пораженных мышц, дыхательная гимнастка по Стрельниковой, физиотерапия.
При нарушении речи эффективны занятия с логопедом, специальный массаж.
К сожалению, полностью излечиться от псевдобульбарного синдрома как правило невозможно, так как такие нарушения возникают при выраженных двусторонних поражениях головного мозга, которые нередко сопровождаются утратой многих нейронов и разрушением нервных путей.
Однако лечение позволяет компенсировать нарушения, а реабилитационные занятия помогут человеку адаптироваться к возникшим изменениям.
Поэтому не стоит пренебрегать рекомендациями доктора, ведь важно замедлить прогрессирование основного заболевания и сохранить нервные клетки.
Ларингофарингеальный рефлюкс: симптомы и лечение
Ларингофарингеальный рефлюкс (ЛФР) — это заброс желудочного содержимого (кислоты и таких ферментов, как пепсин) в гортань, приводящий к появлению охриплости, ощущению кома в горле, затруднению глотания, кашлю, ощущению слизи в гортаноглотке.
Рефлюкс, как причина вышеописанных симптомов без гастроэзофагеальной рефлюксной болезни (ГЭРБ), постоянно ставится под сомнение.
Руководства, выпущенные специализированными обществами в области ларингологии и гастроэнтерологии, представляют разные точки зрения.
Обе группы признают, что интерпретация существующих исследований затрудняется из-за неопределенных диагностических критериев ЛФР, различных показателей ответа на лечение и значительного эффекта плацебо при проводимом лечении.
Имеются относительно ограниченные данные о распространенности ЛФР: примерно у 30% здоровых людей могут фиксироваться эпизоды рефлюкса на суточной pH-метрии или обнаруживаться характерные изменения в гортани.
ЛФР может прямо или косвенно вызывать гортанные симптомы. Прямой механизм включает раздражение слизистой оболочки гортани едкими веществами — рефлюксатами (кислота, пепсин). Косвенный механизм включает раздражение пищевода, что приводит к гортанным рефлексам и появлению симптомов.
Инфекция Helicobacter pylori также может вносить свой вклад. Распространенность H. pylori среди пациентов с ЛФР составляет около 44%.
Ларингофангеальный рефлюкс и ГЭРБ
Хотя кислота желудка является общей как для ЛФР, так и для ГЭРБ, существует много различий, что делает ЛФР отдельным клиническим объектом.
- Обязательным условием ГЭРБ является изжога, которая достоверно наблюдается только у 40% пациентов с ЛФР.
- Большинство пациентов с ГЭРБ имеют признаки эзофагита при биопсии, в то время как пациенты с ЛФР только в 25% случаев.
- Считается, что ГЭРБ является проблемой нижнего сфинктера пищевода и возникает в основном в положении лежа. Напротив, ЛФР рассматривается в первую очередь как проблема верхнего сфинктера пищевода, и возникает в основном в вертикальном положении во время физических нагрузок.
- Для формирования ЛФР необходимо гораздо меньшее воздействие кислоты, чем при ГЭРБ.
Между слизистой оболочкой пищевода и гортани есть существенные различия.
- Верхним пределом нормы для кислотного рефлюкса в пищевод считается до 50 эпизодов в день, при этом 4 эпизода заброса рефлюксата в гортань уже не является вариантом нормы.
- В гортани, в отличие от пищевода, который при перистальтике устраняет кислоту, рефлюксат сохраняется намного дольше, вызывая дополнительное раздражение.
- Эпителий гортани тонкий и плохо приспособлен для борьбы с едкими химическими повреждениями от того же пепсина и кислоты.
Симптомы ларингофарингеального рефлюкса
- Дисфония или охриплость;
- кашель;
- ощущение кома в горле;
- дискомфорт и ощущение слизи в горле;
- дисфагия (нарушение глотания).
Некоторые исследователи считают, что хроническое раздражение гортани может приводить к развитию карциномы у пациентов, не употребляющих алкоголь или не курящих, хотя данных, подтверждающих это, нет.
Симптомы, характерные для ЛФР, также могут быть обусловлены следующими состояниями:
- постназальный синдром;
- аллергический ринит;
- вазомоторный ринит;
- инфекции верхних дыхательных путей;
- привычное покашливание;
- употребление табака или алкоголя;
- чрезмерное использование голоса;
- изменение температуры или климата;
- эмоциональные проблемы;
- раздражители окружающей среды;
- блуждающая нейропатия.
Диагностика
Существуют значительные разногласия по поводу подходящего способа диагностики ЛФР.
Большинству пациентов диагноз ставится клинически — на основании симптомов, связанных с ЛФР.
При ларингоскопии (осмотре гортани) отмечается отечность и гиперемия (краснота) различной степени. Однако относительно слабая корреляция между симптомами и эндоскопическими данными является аргументом против использования эндоскопических методов диагностики.
- Шкала рефлюксных признаков и индекс рефлюксных симптомов хорошо подходят как для диагностики, так и для мониторинга ответа на терапию.
- Суточная Ph-метрия зондом с двойным сенсором, несмотря на превосходную чувствительность и специфичность, ставится под сомнение, так как результаты этого диагностического метода зачастую не коррелируют с тяжестью симптомов.
- Еще одним вариантом диагностики может быть эмпирическое назначение терапии ИПП.
Изменение образа жизни и диета являются основным подходом при лечении ЛФР и ГЭРБ. Роль медикаментозной терапии более противоречива.
Нуждаются ли в лечении пациенты без симптомов заболевания, со случайно выявленными признаками ЛФР, неизвестно.
Существуют теоретические опасения, что ЛФР может увеличить риск злокачественных новообразований, но это пока не доказано. В любом случае, пациентам с бессимптомный ЛФР рекомендуется соблюдение диеты.
Пациентам рекомендуется отказаться от курения, алкоголя, исключить продукты и напитки, содержащие кофеин, шоколад, мяту. К запрещенным продуктам также относятся большинство фруктов (особенно цитрусовых), помидоры, джемы и желе, соусы для барбекю и большинство заправок для салатов, острая пища. Питание рекомендуется дробное.
Следует избегать физических упражнений в течение как минимум двух часов после еды, воздерживаться от еды и питья за три часа до сна.
Медикаментозная терапия обычно включает ингибиторы протонной помпы (ИПП), блокаторы H2 и антациды. ИПП рекомендуется принимать в течение шести месяцев для большинства пациентов с ЛФР.
Данная цифра основана на результатах эндоскопических исследований (именно это время необходимо для уменьшения отека гортани), а также высоком проценте рецидива в случае трехмесячного курса терапии.
Прекращение терапии следует проводить постепенно.
Если терапия ИПП и блокаторами Н2 оказалась безуспешна, следует рассмотреть вариант лечения трициклическими антидепрессантами, габапентином и прегабалином, так как один из возможных механизмов развития рефлюкса — повышенная чувствительность гортани.
Как проходит лечение ларингофарингеального рефлюкса в клинике Рассвет?
Все пациенты с жалобами на охриплость, ощущение кома в горле, затруднение глотания, кашель, ощущение слизи в гортаноглотке осматриваются оториноларингологом и гастроэнтерологом.
Проводится эндоскопическое исследование полости носа, носоглотки и гортани для исключения других заболеваний, которые, помимо ЛФР, могут провоцировать эти симптомы. Гастроэнтеролог также назначает весь необходимый спектр обследований, в том числе исключает инфекцию H. Pylori.
Залог успешной терапии — совместное ведение пациента оториноларингологом, гастроэнтерологом, в ряде случаев психиатром и психотерапевтом.
Чекалдина Елена Владимировна оториноларинголог, к.м.н.
Диагностика и лечение экстрапирамидных гиперкинезов | #06/05 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи
Экстрапирамидные гиперкинезы относятся к числу расстройств, которые не столько угрожают жизни, сколько «разрушают» ее, значительно ограничивая функциональные возможности пациентов, приводя их к психологической и социальной изоляции.
Длительное время результаты лечения экстрапирамидных гиперкинезов вызывали лишь разочарование как у самих пациентов, так и у врачей. Но в последние десятилетия ситуация начала меняться.
Появились более четкие критерии диагностики различных вариантов экстрапирамидных гиперкинезов, существенно расширились возможности лечения, как за счет появления новых методов, так и за счет более рационального применения ранее существовавших.
И если мы до сих пор в подавляющем большинстве случаев не можем кардинально излечить гиперкинез, то, по крайней мере, способны существенно улучшить качество жизни многих пациентов. В данной статье рассмотрены современные подходы к диагностике и лечению наиболее частых вариантов экстрапирамидных гиперкинезов.
Определение и классификация экстрапирамидных гиперкинезов
Экстрапирамидные гиперкинезы (или дискинезии) — это непроизвольные (насильственные) избыточные движения, обусловленные поражением базальных ганглиев и связанных с ними структур, условно объединяемых в экстрапирамидную систему [9].
Экстрапирамидные гиперкинезы следует отличать от более редких периферических гиперкинезов, связанных с поражением или дисфункцией периферических нервов (например, лицевого гемиспазма, синдрома «болезненных ног (рук) — движущихся пальцев», тетания и др.
), а также от психогенных гиперкинезов, являющихся соматическим выражением того или иного психического заболевания.
К основным экстрапирамидным гиперкинезам относят тремор, дистонию, хорею, атетоз, баллизм, тики, миоклонию, акатизию [11]. Традиционно считается, что каждый гиперкинез имеет свой неповторимый двигательный рисунок, в основе которого лежит уникальный патофизиологический механизм. Отчасти это действительно так.
Тем не менее накопленный нами опыт позволяет говорить не столько об отдельных, дискретных синдромах, сколько о едином спектре (континууме) синдромов, в котором наряду с изолированными формами широко представлены переходные или комбинированные формы, что существенно затрудняет их синдромальную диагностику и выбор правильного лечения.
Справедливо мнение, что гиперкинезы «сопротивляются» жесткой вербальной категоризации, и их значительно проще узнать, чем описать. Ситуация усложняется еще и тем обстоятельством, что один и тот же гиперкинез в разных частях тела может выглядеть по-разному.
В связи с этим распознавание гиперкинезов, особенно в сложных или переходных случаях, невозможно без выделения ограниченного числа ключевых признаков.
По нашему мнению, особенно важное значение имеют три признака: двигательный рисунок, временной рисунок, характер возникновения.
По двигательному рисунку гиперкинезы могут быть разделены на три основные группы:
- ритмические гиперкинезы, вызываемые регулярным попеременным или синхронным сокращением мышц-агонистов и антагонистов (пример — дрожание, или тремор);
- преимущественно тонические (медленные) гиперкинезы, вызываемые одновременным сокращением мышц-антагонистов с развитием патологических поз (пример — дистония, а также феноменологически и патофизиологически близкий к ней атетоз);
- преимущественно фазические (быстрые, мобильные) гиперкинезы, приближающиеся по структуре к нормальному двигательному акту (пример — хорея, тики).
По временному рисунку гиперкинезы могут быть разделены на две группы:
- постоянные (большинство форм дистонии, хорея, тремор);
- пароксизмальные (тики, миоклония, а также отдельный вид гиперкинезов, проявляющийся повторяющимися кратковременными приступами — пароксизмальные дискинезии).
По характеру возникновения непроизвольные гиперкинезы могут быть разделены на четыре основные группы:
- спонтанные гиперкинезы (пример — хорея, баллизм, некоторые виды миоклонии);
- акционные (от лат. action — действие) гиперкинезы, возникновение которых провоцируется произвольным движением (кинезигенные гиперкинезы, например кинетический тремор, дистония, пароксизмальные дискинезии) либо определенной позой (постуральные гиперкинезы, например тремор);
- рефлекторные гиперкинезы, провоцируемые внешними раздражителями (пример — рефлекторная миоклония);
- индуцированные («полупроизвольные», или «псевдопроизвольные») гиперкинезы, которые формально совершаются по воле больного, но в силу непреодолимой внутренней потребности (пример — тики или акатизия); усилием воли индуцированные гиперкинезы могут быть временно задержаны, но обычно ценой неумолимо нарастающего внутреннего напряжения, в конечном итоге заставляющего больного сдаться.
Феноменологические особенности основных форм экстрапирамидных гиперкинезов, в сравнении с психогенными гиперкинезами, представлены в таблице.
Общие принципы диагностики экстрапирамидных гиперкинезов
Распознавание того или иного экстрапирамидного синдрома — только отправная точка сложной диагностической работы, итогом которой может быть установление нозологического диагноза.
Диагностика экстрапирамидного синдрома включает три последовательных этапа.
- Распознавание экстрапирамидного синдрома.
- Уточнение анамнестических данных, выявление сопутствующих синдромов, лабораторных и нейровизуализационных маркеров.
- Установление нозологического диагноза.
С нозологической точки зрения в рамках любого экстрапирамидного гиперкинеза могут быть выделены три основные формы.
- Первичные (идиопатические) формы гиперкинеза представляют собой проявление дегенеративных заболеваний, избирательно поражающих базальные ганглии, при которых данный гиперкинез является облигатным и доминирующим (хотя иногда и не единственным) признаком (пример — эссенциальный тремор).
- Вторичные формы гиперкинеза являются осложнением заболеваний известной этиологии (сосудистые поражения мозга, травмы, опухоли, инфекции, рассеянный склероз, метаболические энцефалопатии и т. д.), интоксикаций, побочным действием лекарственных средств.
- Гиперкинезы при мультисистемных дегенерациях ЦНС обычно сопровождаются другими неврологическими синдромами, при этом патологический процесс может быть системным (например, гепатолентикулярная дегенерация) или ограничен пределами ЦНС (например, мультисистемная атрофия или некоторые формы спиноцеребеллярных дегенераций) [10, 11].
Большинство случаев экстрапирамидных гиперкинезов имеют первичный (идиопатический) характер, однако их диагностика требует исключения других, прежде всего вторичных, форм гиперкинезов, особенно связанных с курабельными заболеваниями (такими, как опухоли или эндокринопатии), а также курабельных форм мультисистемных дегенераций, в первую очередь гепатолентикулярной дегенерации (болезни Вильсона–Коновалова). Подобные случаи в клинической практике встречаются редко, но именно они должны быть исключены в первую очередь. Исключение вторичной природы гиперкинеза может потребовать дополнительного инструментального (КТ или МРТ головного мозга, ЭЭГ) либо лабораторного исследования. Следует помнить, что любой экстрапирамидный синдром, впервые проявившийся в возрасте до 50 лет, служит основанием для исключения гепатолентикулярной дегенерации (для этого требуется как минимум анализ крови на церулоплазмин и исследование роговицы с помощью щелевой лампы с целью обнаружения пигментного кольца Кайзера–Флейшера) [12].
Наконец, в каждом случае гиперкинеза следует подумать и о том, что он может иметь психогенную природу. В прошлом большинство случаев гиперкинезов нередко рассматривались как психогенные расстройства.
Этому способствовали вариабельность и динамичность проявлений экстрапирамидных гиперкинезов, их зависимость от движений, позы, эмоционального состояния пациента, нередкое присутствие у пациентов с первичными формами гиперкинезов аффективных расстройств.
В настоящее время очевидно, что психогенные гиперкинезы встречаются редко, но тем более важным представляется их своевременное выявление, позволяющее проводить целенаправленное лечение и как минимум избавляющее пациента от ненужной,
а иногда и опасной для него терапии.
В пользу психогенной природы гиперкинеза могут свидетельствовать: острое начало, последующее волнообразное течение с периодами длительных спонтанных ремиссий, непостоянство гиперкинеза, причудливость его рисунка, обычно не соответствующего характерным формам экстрапирамидных гиперкинезов, ослабление при отвлечении внимания, стойкая реакция на плацебо, полная резистентность к стандартной терапии, наличие других псевдоневрологических симптомов с феноменом селективной несостоятельности, выраженных аффективных расстройств, сопровождающихся множественными соматоформными жалобами, наличие рентной ситуации (в которой больной извлекает моральную или, реже, материальную выгоду из своего заболевания) и т. д. [1].
Ниже более подробно рассмотрены подходы к диагностике и лечению четырех наиболее часто встречающихся форм экстрапирамидных гиперкинезов: тремора, дистонии, хореи и тиков.
Тремор
Тремор (дрожание) — самый частый экстрапирамидный гиперкинез, характеризующийся непроизвольными ритмичными колебательными движениями части тела (чаще всего конечностей и головы) или всего тела, которые упорядочены во времени и пространстве. Феноменологически выделяют два основных типа тремора: тремор покоя и тремор действия (акционный тремор). Тремор покоя характерен для синдрома паркинсонизма, и прежде всего болезни Паркинсона.
Тремор действия подразделяют на постуральный, возникающий при удержании определенной позы (например, вытянутых рук), кинетический, появляющийся при движении (в том числе при приближении к цели — так называемый интенционный тремор), изометрический — при изометрическом мышечном сокращении (например, при сжимании кисти в кулак). К особым формам тремора относятся ортостатический тремор, развивающийся при переходе в вертикальное положение и стоянии, а также селективный кинетический тремор (возникающий только при определенных движениях, например при письме — писчий тремор).