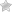1
Чеснокова Н.П. 1
Понукалина Е.В. 1
Моррисон В.В. 1
Бизенкова М.Н. 1
1 ФГБОУ ВО «Саратовский Государственный медицинский университет им. В.И. Разумовского Минздрава России»
4.1. Транспорт кислорода
В сложных механизмах транспорта газов кровью и газообмена в тканях важная роль отводится эритроцитам, ответственным за доставку О2 к различным органам и удаление образующегося в процессе метаболизма СО2.
Эритроцит – безъядерная клетка, лишенная митохондрий, основным источником энергии для эритроцита служит глюкоза, метаболизируемая в гексозомонофосфатном шунте или цикле Эмбдена-Мейергофа.
Транспорт О2 обеспечивается в значительной мере гемоглобином, состоящим из белка глобина и гема. Последний представляет собой комплексное соединение железа и порфирина. Глобин представляет собой тетрамер полипептидной цепи.
Hb A (HbA) – основной гемоглобин взрослых содержит 2 – альфа и 2 – бета – цепи, Hb A2 – содержит две альфа и две дельта цепи.
Гем состоит из иона железа, встроенного в порфириновое кольцо. Ион железа гема обратимо связывает одну молекулу О2. С одной молекулой Hb максимально связываются 4 молекулы О2 с образованием оксигемоглобина.
Гем может подвергаться не только оксигенации, но и истинному окислению, когда железо становится из двухвалентного трехвалентным. Окисленный гем носит название гематина, а молекула гемоглобина становится метгемоглобином. В крови человека метгемоглобин находится в незначительных количествах, его уровень резко возрастает при отравлениях. Метгемоглобин не способен отдавать кислород тканям.
В норме метгемоглобин составляет менее 3% общего Hb крови. Основная форма транспорта О2 – в виде оксигемоглобина. Кислород транспортируется артериальной кровью не только в связи с гемоглобином, но и в растворенном виде.
Принимая во внимание тот факт, что 1 г Hb может связать 1,34 мл О2, кислородная емкость крови в среднем у взрослого человека составляет около 200 мл/л крови.
Одним из показателей кислородного транспорта является насыщение артериальной крови О2(Sa O2), равного отношению О2, связанного с Hb, к кислородной емкости крови:
SaO2=O2, связанного с Hb/O2 емкость крови* 100%.
В соответствии с кривой диссоциации оксигемоглобина насыщение артериальной крови кислородом в среднем составляет 97%, в венозной крови – 75%.
PaO2 в артериальной крови около 100 мм. рт. ст., а в венозной – около 40 мм. рт. ст.
Количество растворенного кислорода в крови пропорционально парциальному давлению О2 и коэффициэнту его растворимости.
Последний для О2 составляет 0,0031/100 мл крови/ 1 мм. рт. ст.. Таким образом, 100 мл крови при PaO2, равном 100 мм. рт. ст., содержит менее 0,31 мл O2.
Диссоциация оксигемоглобина в тканях обусловлена главным образом химическими свойствами гемоглобина, а также рядом других факторов – температурой тела, рН среды, р СО2.
При понижении температуры тела наклон кривой диссоциации оксигемоглобина возрастает, а при ее повышении – снижается, и соответственно снижается сродство Hb к О2.
При снижении рН, т.е. при закислении среды, сродство гемоглобина к О2 уменьшается. Увеличение напряжения в крови СО2 также сопровождается снижением сродства Hb к О2 и уплощением кривой диссоциации оксигемоглобина.
Известно, что степень диссоциации оксигемоглобина определяется содержанием в эритроцитах некоторых фосфорорганических соединений, главным из которых является 2,3 – ДФГ (2,3 дифосфоглицерат), а также содержанием в эритроцитах катионов. В случаях развития алкалозов, поглощение О2 в легких увеличивается, но в то же время затрудняется отдача кислорода тканями. При ацидозах наблюдается обратная картина.
4.2.Утилизация кислорода тканями
Тканевое или клеточное дыхание включает три стадии. На первой стадии пируват, аминокислоты и жирные кислоты окисляются до двухуглеродных фрагментов ацетильных групп, входящих в состав ацетилкофермента А.
Последние на втором этапе окисления включаются в цикл лимонной кислоты, где происходит образование высокоэнергетических атомов водорода и высвобождение СО2 – конечного продукта окисления органических субстратов.
На третьей стадии клеточного дыхания атомы водорода делятся на протоны (Н+) и «высокоэнергетические» электроны, передающиеся по дыхательной цепи на молекулярный О2 и восстанавливающие его до НО2. Перенос электронов сопряжен с запасом энергии в форме АТФ, т.е. с окислительным фосфорилированием (рис.6).
Касаясь патогенеза метаболических сдвигов, свойственных гипоксическим состояниям, следует отметить, что в организме человека более 90% всего потребляемого кислорода восстанавливается с участием цитохромоксидазы митохондрий, и лишь около 10% кислорода метаболизируется в тканях с участием оксигеназ: диоксигеназы и монооксигеназы.
Рис.6. Схема тканевого дыхания. Конечные продукты каждой стадии даны в рамке (Ленинджер А., 1999)
Наиболее многочисленны и сложны монооксигеназные реакции, протекающие в эндоплазматическом ретикулуме клеток при участии цитохрома Р-450 и обеспечивающие гидроксилирование субстрата (стероидных гормонов, лекарственных препаратов и различных др. соединений) и, как правило, его инактивацию.
Диоксигеназы катализируют реакции, в которых в молекулу органического субстрата включаются оба атома молекулы кислорода (например, реакция окисления катехола молекулярным кислородом с раскрытием кольца).
В реакциях, связанных с переносом электронов, т.е.
в реакциях окисления-восстановления, где, как указывалось выше, используется более 90% потребляемого кислорода, атомы водорода, отщепленные дегидрогеназами от субстратов в цикле лимонной кислоты, передают свои электроны в цепь переноса электронов и превращаются также в Н +.
Как известно, помимо 4 пар атомов водорода, поставляемых каждым оборотом цикла лимонной кислоты, образуются и другие атомы водорода, отщепленные дегидрогеназами от пирувата, жирных кислот и аминокислот в процессе их расщепления до Ацетил-СоА и других продуктов.
Таким образом, все атомы водорода, отщепляемые дегидрогеназами от субстратов, передают свои электроны в дыхательную цепь к конечному акцептору электронов – кислороду.
Касаясь последовательности транспорта электронов в окислительно-восстановительных реакциях, протекающих на внутренней мембране митохондрий, прежде всего, следует отметить, что от всех НАД – зависимых реакций дегидрирования восстановленные эквиваленты переходят к митохондриальной НАДН – дегидрогеназе, затем через ряд железосерных ферментов передаются на убихинон М цитохрому b. Далее электроны переходят последовательно на цитохромы С1 и С, затем на цитохромы аа 3 (цитохромоксидазу – медьсодержащий фермент). В свою очередь цитохромоксидаза передает электроны на кислород. Для того, чтобы полностью восстановить кислород с образованием 2-х молекул воды требуется 4 электрона и четыре Н+ .
Скорость утилизации О2 в различных тканях различна. В среднем взрослый человек потребляет 250 мл О2 в 1 мин. Максимальное извлечение О2 из притекающей артериальной крови свойственно миокарду.
Кислород используется в клетках, в основном в метаболизме белков, жиров, углеводов, ксенобиотиков, в окислительно-восстановительных реакциях в различных субклеточных фракциях: в митохондриях, в эндоплазматическом ретикулуме, в реакциях липопероксидации, а также в межклеточном матриксе и в биологических жидкостях.
Коэффициент утилизации О2 в тканях равен отношению потребления О2 к интенсивности его доставки, широко варьирует в различных органах и тканях.
В условиях нормы минимальную потребность в О2 проявляют почки и селезенка, а максимальную потребность – кора головного мозга, миокард и скелетные мышцы, где коэффициент утилизации О2 колеблется от 0,4 до 0,6, а в миокарде до 0,7. При крайне интенсивной физической работе коэффициент утилизации О2 мышцами и миокардом может возрастать до 0,9.
Обмен дыхательных газов в тканях происходит в процессе свободной и облегченной диффузии. При этом О2 переносится по градиенту напряжения газа из эритроцитов и плазмы крови в окружающие ткани.
Одновременно происходит диффузия СО2 из тканей в кровь. На выход О2 из крови в ткани влияет диссоциация оксигемоглобина в эритроцитах, что обеспечивает так называемую облегченную диффузию О2.
Интенсивность диффузионного потока О2 и СО2 определяется градиентом их напряжения между кровью и тканями, а также площадью газообмена, плотностью капилляров, распределением кровотока в микроциркуляторном русле.
Интенсивность окислительных процессов в тканях определяется величиной критического напряжения О2 в митохондриях, которое в условиях нормы должно превосходить 0,1-1 мм рт. ст.
Соответствие доставки О2 к органам и тканям, возросшим потребностям в оксигенации обеспечивается на клеточном, органном уровнях за счет образования метаболитов изнашивания, а также при участии нервных, гормональных и гуморальных влияний.
4.3.Транспорт СО2
Основная масса углекислого газа (СО2) образуется в организме как конечный продукт различных метаболических реакций и транспортируется к легким с кровью. Вдыхаемый воздух содержит лишь незначительное количество СО2.
- Транспорт СО2 кровью осуществляется в 3-х состояниях: в виде аниона бикарбоната, в растворенной форме и в виде карбаминовых соединений.
- СО2 хорошо растворяется в плазме крови и в артериальной крови, около 5% от общей двуокиси углерода содержится в крови в растворенной форме.
- Анион бикарбоната составляет около 90% от общего содержания СО2 в артериальной крови: СО2+Н2О — Н++НСО-3.
Эта реакция медленно протекает в плазме крови, но чрезвычайно интенсивно происходит в эритроцитах при участии фермента карбоангидразы.
Мембрана эритроцита относительно непроницаема для Н+, как и вообще для катионов, но в тоже время, проницаема для ионов НСО-3, выход которых из эритроцитов в плазму обеспечивается притоком Cl- из плазмы в эритроциты.
Часть Н+ забуферивается гемоглобином с образованием восстановленного гемоглобина.
- Третьей формой транспорта СО2 кровью являются карбаминовые соединения, образованные взаимодействием СО2 с концевыми группами белков крови преимущественно с гемоглобином:
- Hb NH2 + CO2 — Hb NH COOH > Hb NH COO + Н+
- Карбаминовые соединения составляют около 5% от общего количества СО2, транспортируемого кровью.
В оксигенированной артериальной крови напряжение СО2 составляет 40 мм. рт. ст., а в венозной крови Рv СО2 равно 46 мм. рт. ст.
4.4.Связывание гемоглобина с окисью углерода
Угарный газ (СО) – окись углерода обладает значительно большим сродством к гемоглобину, чем О2, с последующим образованием карбоксигемоглобина. СО входит в состав бытового газа, а также выделяется при работе двигателей внутреннего сгорания.
При концентрации СО во вдыхаемом воздухе всего в количестве 7*10- 4 около 50% гемоглобина превращается в карбоксигемоглобин. В норме в крови содержится около 1% HbCO, у курильщиков – 3% . В крови водителей такси концентрация карбоксигемоглобина достигает 20%.
Карбоксигемоглобин диссоциирует с отдачей О2 в 200 раз медленней оксигемоглобина и в то же время препятствует его диссоциации в тканях.
Библиографическая ссылка
Чеснокова Н.П., Понукалина Е.В., Моррисон В.В., Бизенкова М.Н. ЛЕКЦИЯ 4 ФИЗИОЛОГИЯ ТРАНСПОРТА ГАЗОВ КРОВЬЮ И КИСЛОРОДНОГО ОБЕСПЕЧЕНИЯ ТКАНЕЙ // Научное обозрение. Медицинские науки. – 2017. – № 2. – С. 40-42;
URL: https://science-medicine.ru/ru/article/view?id=973 (дата обращения: 18.05.2022).
Физиология и патофизиология газообмена
Транспорт О2 из атмосферы до периферических тканей
организма представляет собой многоступенчатый процесс.
После того как воздух попадает в альвеолы легких, следующим этапом
газообмена является диффузия кислорода из альвеол в кровь легочных
капилляров и диффузия СО2 из крови легочных капилляров
в альвеолы. Диффузия представляет собой простое движение молекул через
респираторную мембрану из области более высокого давления в область
более низкого.
Таким образом, парциальное давление О2 (PO2)
является одним из основных факторов, определяющих его транспорт в
организме, причем не только в легких, но и во всем теле вплоть до
периферических тканей.
Помимо градиента давления скорость диффузии определяется 1) растворимостью
газа в жидкости; 2) площадью поверхности, через которую протекает
диффузия; 3) расстоянием, которое газ должен пройти при диффузии;
4) молекулярным весом газа; 5) температурой жидкости. Поскольку в
живом организме температура постоянна, она обычно не учитывается.
Применительно к альвеолокапиллярной мембране скорость диффузии газа
будет зависеть от:
- толщины мембраны;
- площади поверхности мембраны;
- диффузионного коэффициента газа в мембране;
- градиента давления газа по обе стороны мембраны.
По мере транспорта О2 от легких к периферическим
тканям его парциальное давление снижается. Если в атмосферном воздухе
при нормальном атмосферном давлении парциальное давление О2
составляет 159 мм рт. ст., то в периферических тканях, в зависимости
от уровня их обмена, — 35–85 мм рт. ст. Венозная кровь, поступающая
в легкие, имеет РО2 около 40 мм рт. ст.
Уже в альвеолярном воздухе содержание О2 и его парциальное
давление отличаются от атмосферного воздуха (13,6 % и 104 мм рт.
ст. соответственно). Это происходит вследствие нескольких причин:
- альвеолярный воздух лишь частично замещается атмосферным во время
каждого вдоха; - О2 постоянно абсорбируется из альвеолярного воздуха;
- СО2 постоянно диффундирует из крови легочных капилляров
в альвеолы; - сухой атмосферный воздух, который поступает в дыхательные пути, увлажняется,
насыщаясь водными парами, прежде чем достигает альвеол.
В артериальной крови, покидающей легкие, РО2
уменьшается уже до 95 мм рт. ст. вследствие так называемого венозного
примешивания.
Дело в том, что определенное количество венозной крови
(1–2 %) не аэрируется в легких, поступая напрямую в артериальное
русло, что и приводит к некоторому снижению РО2.
Увеличение объема шунтированной крови, которое происходит при гипоксии
может приводить к существенному понижению артериального РО2.
Увеличение толщины альвеолокапиллярной мембраны, затрудняющее диффузию
газов, часто является следствием отека — увеличения количества жидкости
в межклеточном пространстве мембраны. Состояние характеризуется как
интерстициальный отек легких.
Кроме того, жидкость может накапливаться
и в альвеолах, так что газам приходится проходить не только через
мембрану, но и через жидкость, что характерно уже для альвеолярного
отека легких. В большинстве случаев имеет место сочетание этих состояний
той или иной степени выраженности.
Имеет значение и исходное состояние
легких. При ряде заболеваний, может возникнуть фиброз какого либо
участка легких с утолщением альвеолокапиллярной мембраны.
Поскольку
скорость диффузии газов через мембрану обратно пропорциональна ее
толщине, любой фактор, увеличивающий ее толщину более чем в два –
три раза, может существенно нарушать нормальный газообмен.
Из капилляров кровеносного русла О2 диффундирует
в периферические ткани, поскольку парциальное давление О2
в капиллярах выше, чем в тканях. РО2 в интерстициальной
жидкости вне капилляров составляет в среднем 40 мм рт. ст., тогда
как в артериальной крови — 95 мм рт. ст.
В венозной крови, покидающей
капилляр, РО2 также составляет около 40 мм рт. ст.
Если скорость тканевого кровотока увеличивается, большие количества
О2 доставляются тканям и тканевое РО2
увеличивается.
Увеличение тканевого метаболизма приводит к снижению
РО2 как в периферических тканях, так и в венозной
крови.
Поскольку О2 постоянно используется тканями, внутриклеточное
РО2 всегда остается ниже интерстициального. Со снижением
интерстициального РО2 снижается и РО2
внутри клеток, повышение интерстициального РО2 ведет
к повышению внутриклеточного РО2. Важным общим свойством
живых организмов является большой запас функциональной прочности систем
поддержания жизнедеятельности.
Такая особенность характерна и для
процессов газообмена. Для полного обеспечения процессов метаболизма
достаточно РО2 1–5 мм рт. ст., в то время как внутриклеточное
РО2 может варьировать от 5 до 60 мм рт. ст. (в зависимости
от протяженности капиллярного русла). Поэтому организм человека и
может функционировать при весьма существенном снижении РО2
в атмосферном воздухе.
В нормальных условиях около 97 % кислорода от легких к тканям переносится
в химически связанном виде гемоглобином. Лишь 3 % составляет О2
растворенный в плазме крови. Следует учитывать, что способность гемоглобина
связывать О2 является ограниченной.
Каждый грамм
гемоглобина может максимально связать 1,34 мл О2.
Эта так называемая константа Гюффнера. Соответственно кислородная
емкость крови (т. е.
максимальное общее количество кислорода, которое
может быть перенесено кровью) будет находиться в прямой зависимости
от содержания гемоглобина:
Кислородная емкость крови = [ Hb ] x 1, 34 мл O2 / 100 мл крови
У здоровых людей с содержанием гемоглобина 150 г/л кислородная емкость
крови составляет 201 мл О2/л крови. Реально переносимое
количество мл О2 обычно меньше.
-
Ключевым фактором, характеризующим количество кислорода, связанного
с гемоглобином, является насыщение артериальной крови кислородом (сатурация,
SaO2). Оно выражает отношение между количеством кислорода,
связанного с гемоглобином и кислородной емкостью крови: - SaO2 = ( HbO2 / кислородная емкость крови ) x 100 %
-
Содержание кислорода в крови (контент, СаО2) — это
сумма связанного с гемоглобином и растворенного в плазме О2: - CaO2 = ( 1, 34 x [ Hb ] x SaO2 ) + ( PaO2 x 0, 0031 )
-
Очевидно, что СаО2 зависит главным образом от фракции
О2, связанной с гемоглобином.
Кровь содержит незначительное количество кислорода, не связанного
с гемоглобином, а растворенного в плазме.
Согласно закону Генри, количество
растворенного кислорода пропорционально парциальному давлению О2
и коэффициенту его растворимости, а растворимость О2
в крови очень низка: только 0,0031 мл О2 растворяется
в 0,1 л крови при увеличении давления на 1 мм рт. ст.
Таким образом,
при РаО2 равным 100 мм рт. ст., в 100 мл артериальной
крови содержится только 0,31 мл растворенного О2.
Со снижением РаО2 количество растворенного в плазме
О2 станет еще меньше.
Содержание О2 в связи с изменениями РаО2
колеблется незначительно до тех пор, пока устойчиво поддерживается
SaO2. Изменения содержания гемоглобина приводят к
более заметным сдвигам СаО2.
Нормальное СаО2
равно 198 мл О2/л крови при условии, что PaO2 = 100 мм рт. ст.,
содержание гемоглобина 150 г/л, а SaO2 = 97 %.
Умеренная анемия (например гемоглобин 120 г/л) при поддержании нормального
РаО2 проявляется снижением СаО2
до 160 мл О2/л крови.
Сродство гемоглобина к кислороду возрастает по мере последовательного
связывания молекул О2, что придает кривой диссоциации
оксигемоглобина сигмовидную или S-образную форму. Эта кривая, соотносящая
изменения SaO2 в зависимости от РаО2,
важна для анализа процессов транспорта кислорода к периферическим
тканям:
Верхняя часть кривой (при РаО2 > 60
мм рт. ст.) — относительно плоская. Это приводит к тому, что SaO2,
а следовательно, и СаО2 остаются достаточно постоянными,
несмотря на значительные колебания РаО2.
Повышение
СаО2 или транспорта кислорода в этой области кривой
может быть достигнуто только за счет увеличения содержания гемоглобина
(например, при переливании крови) или растворения в плазме крови кислорода
(например при гипербарической оксигенации).
Крутые средняя и нижняя часть кривой иллюстрируют то положение, что,
хотя SaO2 падает (когда РаО2 оказывается
ниже 60 мм рт. ст.), процесс насыщения гемоглобина кислородом продолжается,
поскольку градиент РаО2 между альвеолами и капиллярами
сохраняется. Периферические ткани в этих условиях могут продолжать
извлекать достаточное количество О2, несмотря на
снижение капиллярного РО2.
РаО2, при котором гемоглобин насыщен кислородом на
50 % (при 37 °С и рН 7,4) известно как Р50. Это
общепринятая мера сродства гемоглобина к кислороду. Р50
в крови человека в норме составляет 26,6 мм. рт. ст. Однако оно может
изменяться при различных метаболических и физиологических условиях,
воздействующих на процесс связывания кислорода гемоглобином.
Когда сродство гемоглобина к кислороду падает, О2
с большой легкостью переходит в ткани, и наоборот. Повышение Р50
определяет сдвиг кривой диссоциации оксигемоглобина вправо.
Сродство
гемоглобина к кислороду снижается, указывая, что теперь требуется
более высокое РаО2 для поддержания SaO2
на прежнем уровне.
Более низкое сродство гемоглобина к кислороду означает
повышенное высвобождение кислорода в тканях, но ухудшение связывания
гемоглобина с О2 в легких.
Сдвиг кривой диссоциации влево и соответствующее снижение Р50
указывает на повышенное сродство гемоглобина к кислороду — улучшение
связывания в легких и ухудшение высвобождения О2
в периферических тканях. На Р50 и положение кривой
диссоциации гемоглобина влияет несколько факторов, в частности, рН
и температура.
Для обеспечения обмена веществ в периферических тканях важное значение
имеет не только общее содержание О2 — ключевой физиологической
переменной является его доставка. Доставка кислорода — это количество
кислорода, транспортируемое к тканям в единицу времени.
Чтобы поддержать
аэробный метаболизм и предотвратить накопление лактата, периферические
ткани должны постоянно снабжаться кислородом.
Обстоятельства, которые
определяют адекватность кислородного снабжения, разнообразны и включают
состояние покоя, физическую нагрузку, гиперкатаболические состояния
и инфекцию.
Доставка кислорода к периферическим тканям зависит от количества кислорода
в определенном объеме крови и уровня кровотока. Хотя объем кровотока
к отдельным органам различен, в периферических тканях он в целом равен
сердечному выбросу (CB). Системная доставка О2 (DО2)
рассчитывается как DO2 = СВ (л/мин) x CaO2 (мл/л).
Нередко DО2 рассчитывают с учетом площади тела. То
есть на самом деле рассчитывают индекс DО2. Нормальными
величинами индекса DО2 считают 520–720 мл·мин-1·м-2.
Доставка кислорода падает при уменьшении сердечного выброса или снижении
объемного содержания кислорода в артериальной крови.
Это характерно
для многих критических и терминальных состояний и чаще всего наблюдается
при выраженных проявлениях сердечной недостаточности, повышении внутрилегочного
шунтирования крови, централизации кровообращения, при различных пороках
сердца, кардиохирургических и других длительных и травматичных вмешательствах.
С практической точки зрения следует иметь в виду, что любое нарушение
кровообращения будет ухудшать доставку О2.
Потребление кислорода является заключительным этапом транспорта кислорода
тканям и представляет собой кислородное обеспечение тканевого метаболизма.
В условиях основного обмена взрослый человек потребляет около 250
мл О2 в 1 мин. Однако скорость утилизации О2
различными тканями значительно отличается.
Потребление кислорода тканями (VO2) — интегральный
показатель, учитывающий как циркуляторный компонент транспорта кислорода
(сердечный выброс), так и его гемический компонент (артериовенозное
различие по кислороду, CaO2 — CvO2).
Его можно определить по формуле: VO2 = СВ x (CaO2 — CvO2) x 10.
Так же как и DО2, VO2 часто выражают
в виде индекса, то есть в перерасчете на площадь тела.
Нормальными
величинами индекса потребления кислорода являются 110–160 мл·мин-1·м-2.
В зависимости от состояния организма (покой, нагрузка или заболевание)
меняется фракционное распределение СВ к органам. Более того, и экстракция
кислорода тканями различных органов неодинакова. Например, миокард
получает лишь малую фракцию СВ, но извлекает почти весь доставляемый
кислород.
Нормальный компенсаторный ответ на снижение кровотока проявляется
в виде увеличения поглощения кислорода, достаточного для поддержания
VO2 на нормальном уровне. Падение сердечного выброса
компенсируется увеличением артериовенозного различия по кислороду,
и VO2 остается неизменным. Снижение насыщения венозной
крови кислородом отражает увеличение экстракции кислорода.
Способность компенсировать снижение кровотока повышением поглощения
кислорода является характерной особенностью микроциркуляторного русла
практически всех органов и тканей за исключением сердца и диафрагмы.
В них высокая экстракция кислорода из капиллярного ложа происходит
уже в норме. Поэтому уровень кислорода в тканях сердца и диафрагмы
весьма чувствителен даже к незначительным изменениям кровотока.
Таким образом, основными факторами, определяющими доставку О2,
являются:
- парциальное давление кислорода в атмосферном воздухе;
- нормальное состояние альвеолокапиллярной мембраны;
- эффективность дыхательной системы;
- достаточное количество гемоглобина крови;
- эффективность системы кровообращения.
Сергей Науменко,
г. Новосибирск, 2018 г.
23. Транспорт кислорода. Кривая диссоциации оксигемоглобина
О2
переносится к тканям в двух формах:
связанный с гемоглобином и растворенный
в плазме. В крови содержится лишь
незначительное количество О2, растворимого
в плазме.
Согласно закону Генри, количество
газа, растворенного в жид¬ кости, прямо
пропорционально его парциальному
давлению и коэффи¬ циенту растворимости.
Растворимость О2 в плазме крови низка:
при РО2 = = 1 мм рт.ст.
в 100 мл крови
растворяется 0,0031 мл О2
При
нормальных физиологических условиях
(РаО2 = 100 мм рт.ст.) в 100 мл крови растворяется
0,31 мл О2, т.е. 0,31 об.%. Такое количество О2
не обеспечивает потребности организма,
поэтому основное значение име¬ ет другой
способ переноса — в виде связи с
гемоглобином внутри эритро¬ цита.
Гемоглобин является основным протеином
эритроцитов.
Главной функцией гемоглобина
является транспорт О2 от легких к тканям
и транс¬ порт СО2 от тканей к легким.
Каждая молекула гемоглобина человека
со¬ стоит из белка глобина и гема.
Основной глобин взрослых — НЬА являет¬
ся тетрамером, состоящим из двух
полипептидных цепей а и двух поли¬
пептидных цепей р.
В спиральную структуру
каждой полипептидной цепи глобина
встроен гем, который является комплексным
соединением двух¬ валентного иона
железа Fe2+ и порфирина. Ион железа гема
способен присоединять одну молекулу
О2, т.е.
одна молекула гемоглобина способна
связать 4 молекулы О2 Следует особо
подчеркнуть уникальные особенно¬ сти
иона Fe2+ тема обратимо связывать молекулу
О2 НЬ + О2 НЬО2, в то время как обычно
при реакции изолированного Fe2+ и кислорода
обра¬ зуется Fe3+. Окисленный ион Fe3+ не
способен высвобождать О2, т.е.
об¬ разуется
необратимая связь, а связь иона Fe2+ тема
с О2 происходит за счет конформационных
изменений третичной и четвертичной
структуры глобина, она обратима, т.е.
в
тканях происходит высвобождение О2
Гемоглобин, связанный с четырьмя
молекулами О2, называется оксигемоглобином,
а гемоглобин, не содержащий О2или менее
четырех молекул О2, — деоксигенированным
гемоглобином. 1 г гемоглобина способен
максимально связать 1,34 мл О2 Учитывая,
что нормальное содержание гемоглобина
составляет 15 г/100 мл, можно рассчитать,
что в 100 мл крови максимально может
содержаться 20.1 мл О2 связанного с
гемоглобином. Данная величина называется
кислородной емкостью крови (КЕК):
Наиболее
важным параметром, определяющим
количество кислорода, связанного с
гемоглобином, является насыщение
гемоглобина кислоро¬ дом — сатурация
(SаО2), который рассчитывают по формуле:
При
РаO2, равном 100 мм рт.ст., насыщение
гемоглобина кислородом артериальной
крови составляет около 97 %. В венозной
крови (РО2 = 40 мм рт.ст.) SaO2 приблизительно
равна 75 %.
Кривая
диссоциации оксигемоглобина Зависимость
насыщения гемоглобина О2 от парциального
напряжения О2 может быть представлена
графически в виде кривой диссоциации
окси¬ гемоглобина. Кривая имеет
сигмовидную форму, при этом нижняя часть
кривой (РаО2< 60 мм рт.ст.) имеет крутой
наклон, а верхняя часть (РаО2 > 60 мм
рт.ст.) относительно пологая.
Нижний
участок кривой диссоциа¬ ции оксигемоглобина
показывает, что при снижении РаО2
продолжается насыщение гемоглобина
кислородом,т.е. ткани продолжают извлекать
до¬ статочное количество О2 из крови.
Верхняя пологая часть кривой демонст¬
рирует относительное постоянство
насыщения гемоглобина кислородом, а
следовательно, и содержания кислорода
в крови независимо от изменений РаО2
(рис. 7.9).
Положение
кривой диссоциации оксигемоглобина
зависит от сродства гемоглобина с
кислородом. При снижении сродства
гемоглобина к О2, т.е. облегчении перехода
О2 в ткани, кривая сдвигается вправо.
Повышение сродства гемоглобина к О2
означает меньшее высвобождение кислорода
в тканях, при этом кривая диссоциации
сдвигается влево.
Важным показате¬ лем,
отражающем сдвиги кривой диссоциации
оксигемоглобина, является параметр
Р50, т.е. такое РО2, при котором гемоглобин
насыщен кислоро¬ дом на 50 % (см. рис. 7.9).
В нормальных условиях у человека (при
t 37 °С, рН 7,40 и РаСО2= 40 мм рт.ст.) Р5о — 27 мм
рт.ст.
При сдвиге кривой дис¬ социации
вправо Р50 увеличивается, а при сдвиге
влево — снижается. На сродство гемоглобина
к О2оказывают влияние большое количество
метаболических факторов, к числу которых
относятся рН, РСО2 темпера¬ тура,
концентрация в эритроцитах
2,3-дифосфоглицерата (2,3-ДФГ).
Сни¬ жение
рН, повышение РСО2 и температуры снижают
сродство гемоглоби¬ на к О2 и смещению
кривой вправо. Такие метаболические
условия созда¬ ются в работающих мышцах,
и такой сдвиг кривой является физиологиче¬
ски выгодным, так как повышенное
высвобождение О2необходимо для активной
мышечной работы.
В противоположность
этому повышение рН, снижение температуры
и снижение РСО2(такие условиях создаются
в лег¬ ких) смещают кривую диссоциации
оксигемоглобина влево (рис. 7.10).
Влияние
рН и РаСО2 на кривую диссоциации называется
эффектом Бора. 2,3-ДФГ образуется в
эритроцитах в процессе гликолиза и
выполняет функцию главного энергетического
субстрата (в эритроцитах отсутствуют
митохондрии, поэтому не происходят
реакции окислительного фосфорилирования,
и АТФ не имеет большого значения как
источник энергии).
В условиях продолжительной
гипоксии увеличивается содержание
2,3-ДФГ в эритроцитах, что приводит к
снижению сродства гемоглобина к O2 и
более интенсивному переходу его из
крови в ткани. Снижение концентра¬ ции
2,3-ДФГ в эритроцитах приводит к сдвигу
кривой диссоциации влево.
На кривую
диссоциации оксигемоглобина может
оказать влияние и окись углерода (СО).
СО имеет сродство к гемоглобину в 240 раз
выше, чем О2, и, связываясь с гемоглобином,
образует карбоксигемоглобин (НЬСО). При
этом даже небольшие количества СО могут
связать большую часть НЬ крови и
значительно уменьшить содержание О2
крови.
Кроме того, СО сдвигает кривую
диссоциации влево, что препятствует
высвобож¬ дению О2 в тканях и также
усугубляет гипоксию. Еще одним фактором,
влияющим на сродство НЬ к кислороду,
является метгемоглобин — гемоглобин,
содержащий железо, окисленное до Fе3+.
У
здорового человека общее содержание
метгемоглобина не превышает 3 %, однако
при приеме некоторых лекарств (например,
фенацетин, суль¬ фаниламиды, нитроглицерин)
и дефиците фермента метгемоглобин-редуктазы
происходит образование значительных
количеств метгемоглобина. Метгемоглобинемия
вызывает смещение кривой диссоциации
влево, т.
е препятствует высвобождению
в тканях, а при повышении концентрации
метгемоглобина более 60 % происходит
также и уменьшение нормального НЬ, что
приводит к тяжелой гипоксии.
Кривая диссоциации оксигемоглобина
Нормальному уровню Ра02 (92-98 мм рт. ст.) соответствует S,0; 94-98 %. Добиться полного насыщения гемоглобина кислородом можно только посредством увеличения содержания кислорода во вдыхаемом газе.»
Выбирая пульсоксиметр, обычно проверяют его на себе. Если монитор показывает SpО2= 100 % (а такие модели-оптимисты встречаются достаточно часто), подумайте, стоит ли его покупать.
Испытывать пульсоксиметр должен некурящий человек, так как после выкуренной сигареты до 8-10 % гемоглобина крови превращаются в карбоксигемоглобин.
При этом пульсоксиметр завышает Sa02, и модель может оказаться незаслуженно скомпрометированной.
Зависимость SaO2 от РaО2 для каждого больного можно описать эмпирическими формулами (уравнение Хилла, алгоритмы Кел-мана, Северингхауза и др.), в которых учитываются температура, рН и прочие факторы.
Данные формулы в разных модификациях обычно вводят в современные автоматические приборы контроля КЩС и газового состава крови (Radiometer, AVL, Instrumentation Laboratories и пр.), которые вычисляют сатурацию гемоглобина по напряжению кислорода в крови. Собственно, сама кривая диссоциации оксигемоглобина и является графическим выражением этих уравнений.
Более простой показатель положения кривой диссоциации — индекс Рм; он равен напряжению кислорода в крови, при котором сатурация гемоглобина составляет 50 % (рис. 1.7).
Нормальная величина P50 равна 27 мм рт. ст. Ее уменьшение соответствует сдвигу кривой влево, а увеличение — сдвигу вправо.
После полного насыщения гемоглобина кислородом дальнейшее повышение Ра02 сопровождается лишь незначительным приростом СаО2 за счет физически растворенного кислорода. Поэтому увеличение концентрации кислорода во вдыхаемом или вдуваемом газе (F1O2) сверх уровня, достаточного для полного насыщения гемоглобиновой емкости (Sa02 = 99-100 %), редко бывает оправданным.
Проходя через капилляры, артериальная кровь отдает тканям часть содержащегося в ней кислорода и превращается в венозную (PvO2 = 40 мм рт. ст., SvO2 = 75 %). Таким образом, в газообмене участвует лишь около 25 % запаса кислорода артериальной крови, а сатурация и десатурация гемоглобина происходят, на пологом участке кривой диссоциации.
Патология дыхательной системы приводит к нарушению ок-сигенации крови в легких с развитием артериальной гипоксемии, степень которой количественно оценивается пульсоксиметром.
В этих условиях снабжение тканей кислородом осуществляется в «аварийном» режиме, на крутом участке кривой, где незначительного падения РаО2 оказывается достаточно для отделения от оксигемоглобина требуемого количества кислорода.
Аварийность режима заключается в уменьшении напряжения и, следовательно, содержания кислорода в тканях, о чем свидетельствует низкое напряжение кислорода в венозной крови.
Гемоглобин как транспортный белок призван решать две задачи: присоединять кислород в легких и отдавать его тканям.
Эти задачи противоположны по своей сути, но выполняются одним и тем же веществом, поэтому стремление гемоглобина связываться с кислородом (сродство гемоглобина к кислороду) должно быть достаточным — чтобы обеспечить оксигенацию крови в легких, но не избыточным — чтобы не нарушить процесс отдачи кислорода на периферии.
Нормальное положение кривой диссоциации оксигемоглобина как раз и соответствует оптимальной готовности гемоглобина к реализации обеих задач. Но при определенных условиях баланс между стремлением гемоглобина присоединить кислород и готовностью его отдать нарушается. Графически это выражается сдвигом кривой диссоциации вправо или влево (рис. 1.8).
Читать
Патофизиология. Том 2
Авторы:
Под ред. В.В. Новицкого, Е.Д. Гольдберга, О.И. Уразовой
Библиография:
Патофизиология : учебник : в 2 т. / под ред. В.В. Новицкого, Е.Д. Гольдберга, О.И.
Уразовой. — 4-е изд., перераб. и доп. — ГЭОТАР-Медиа, 2009. — Т. 2. — 640 с. : ил.
- Аннотация:
- Учебник подготовлен коллективом авторов — ведущими патофизиологами России и стран
- СНГ (Украина, Грузия). В его создании принимали участие известные педагоги —
- представители московской, томской, казанской, харьковской и тбилисской научных школ
- патофизиологов, а также крупнейшие специалисты, работающие в научно-
- исследовательских институтах Российской академии медицинских наук.
- Настоящее издание является практически полностью переработанным и дополненным
вариантом учебников «Патологическая физиология» под редакцией А.Д. Адо и В.В.
Новицкого (Томск, 1994 г.) и «Патофизиология» под редакцией В.В. Новицкого и Е.Д.
Гольдберга (Томск, 2001, 2006 гг.).
- Второй том посвящен патологической физиологии органов и систем. Существенно
- изменены и дополнены разделы по патофизиологии кроветворной, дыхательной и
- пищеварительной систем, опухолевого роста, типовых нарушений обмена веществ. В
- значительной степени пересмотрены и дополнены другие главы учебника.
- Для студентов медицинских вузов (всех факультетов).
- Оглавление
- АВТОРСКИЙ КОЛЛЕКТИВ
- СПИСОК СОКРАЩЕНИЙ
- ЧАСТЬ III ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ ГЛАВА 14
- ПАТОФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ
- ГЛАВА 15 ПАТОФИЗИОЛОГИЯ СЕРДЕЧНО- СОСУДИСТОЙ СИСТЕМЫ
- ГЛАВА 16 ПАТОФИЗИОЛОГИЯ ДЫХАНИЯ
- ГЛАВА 17 ПАТОФИЗИОЛОГИЯ ПИЩЕВАРЕНИЯ
- ГЛАВА 18 ПАТОФИЗИОЛОГИЯ ПЕЧЕНИ
- ГЛАВА 19 ПАТОФИЗИОЛОГИЯ ПОЧЕК
- ГЛАВА 20 ПАТОФИЗИОЛОГИЯ ЭНДОКРИННОЙ СИСТЕМЫ
- ГЛАВА 21 ПАТОФИЗИОЛОГИЯ НЕРВНОЙ СИСТЕМЫ
- ГЛАВА 22 ПАТОФИЗИОЛОГИЯ ВЫСШЕЙ НЕРВНОЙ ДЕЯТЕЛЬНОСТИ
- ЛИТЕРАТУРА
- ЦВЕТНАЯ ВКЛЕЙКА
- АВТОРСКИЙ КОЛЛЕКТИВ
Академики РАМН: А.Д. Адо, И.Г. Акмаев, Н.П. Бочков, Ю.А. Владимиров, Е.Д.
Гольдберг, Г.Н. Крыжановский, А.А. Кубатиев, В.А. Неговский, В.В. Новицкий, В.П.
Пузырев, М.М. Хананашвили.
Члены-корреспонденты РАМН: З.С. Баркаган, Н.Е. Кушлинский, Ю.Б. Лишманов, Г.В.Порядин, С.Б. Ткаченко;
Профессоры: М.Б. Баскаков, Э.И. Белобородова, В.Т. Долгих, В.В. Долгов, Н.А.
Клименко, В.В. Климов, В.С. Лаврова, Л.Н. Маслов, Г.И. Мчедлишвили, Н.П. Пирогова, В.И. Пыцкий, Е.А. Степовая, Ф.Ф. Тетенев, О.И. Уразова, Б.М. Федоров, Т.С. Федорова, О.Ю. Филатов, И.А. Хлусов.
Доценты: С.Э. Бармина, Г.В. Бурлаков, Л.М. Далингер, О.Б. Запускалова, М.Ю. Хлусова, Е.Н. Чернова
- СПИСОК СОКРАЩЕНИЙ
- АГ — антиген
- АДГ — антидиуретический гормон АДФ — аденозидифосфат
- АИГА — аутоиммунная гемолитическая анемия АКМ — альвеолярно-капиллярная мембрана
- АКТГ — адренокортикотропный гормон АлАТ — аланинаминотрансфераза АМФ —
- аденозинмонофосфат
- АПТВ — активированное парциальное тромбопластиновое время АПФ —
- ангиотензинпревращающий фермент АсАТ (АСТ) — аспартатаминотрансфераза АТ —
- антитело
- АТ-рТТГ — антитела к рецептору тиреотропного гормона
- АТ-ТГ — антитела к тиреоглобулину
- АТ-ТПО — антитела к тиреопероксидазе
- АТФ — аденозинтрифосфат
- АТФаза — аденозинтрифосфатаза
- АФК — активные формы кислорода
- АФС — антифосфолипидный синдром
- АХЗ — анемия хронических заболеваний
- Ацетил-КоА — ацетил-коэнзим А
- АЭС — атомная электростанция
- БАВ — биологически активные вещества
- БОЕ-Э — бурстобразующая единица эритроцитов
- БТШ — белок теплового шока
- ВИП — вазоактивный интестинальный полипептид
- ВИЧ — вирус иммунодефицита человека
- ВМК — высокомолекулярный кининоген
- ВОЗ — Всемирная организация здравоохранения
- Г-6-Ф — глюкозо-6-фосфат
- Г-6-ФДГ — глюкозо-6-фосфатдегидрогеназа
- ГАМК — γ-аминомасляная кислота
- ГБН — гемолитическая болезнь новорожденного
- ГЗТ — гиперчувствительность замедленного типа
- ГИМ — гемопоэзиндуцирующее микроокружение
- ГИП — гастринингибирующий пептид
- Г-КСФ — гранулоцитарный колониестимулирующий фактор ГЛП — гиперлипопротеинемия
- ГЛЮТ — глюкозный транспортер
- ГМ-КСФ — гранулоцитарно-макрофагальный колониестимулирующий фактор
- ГОМК — γ-оксимасляная кислота ГОЭ — гормон-отвечающий элемент ГП — гликопротеин
- ГПП — глюкагоноподобный пептид
- ГПУВ — генератор патологически усиленного возбуждения
- ГР — глюкокортикоидный рецептор
- Гр — грэй, единица измерения дозы облучения
- ГСИК — гормон, стимулирующий интерстициальные клетки
- ГТГ — гонадотропный гормон
- ГТТ — глюкозотолерантный тест
- ГТФ — гуанозинтрифосфат
- ГУС — гемолитико-уремический синдром
- ГЭБ — гематоэнцефалический барьер
- ДL — диффузионная способность легких
- ДВС — диссеминированное внутрисосудистое свертывание
- ДГР — дуоденогастральный рефлюкс
- ДИТ — дийодтирозин
- ДНК — дезоксирибонуклеиновая кислота
- ДНКаза — дезоксирибонуклеаза
- ДНТК — диффузный ноцицептивный тормозной контроль
- ДО — дыхательный объем
- ДПК — двенадцатиперстная кишка
- 2,3-ДФГ — 2,3-дифосфоглицерат
- ЕК — естественные (или натуральные) киллеры
- ЖЕЛ — жизненная емкость легких
- ЖКТ — желудочно-кишечный тракт
- ИБС — ишемическая болезнь сердца
- ИВЛ — искусственная вентиляция легких
- ИГА — индекс гистологической активности
- ИК — иммунный комплекс
- ИМТ — индекс массы тела
- ИР — инсулинорезистентность
- иРНК — информационная рибонуклеиновая кислота ИФР — инсулиноподобный фактор
- роста КОЕ-Ба — колониеобразующая единица базофилов КОЕ-Г — колониеобразующая
- единица гранулоцитов КОЕ-ГМ — колониеобразующая единица гранулоцитов и
- макрофагов КОЕ-ГЭММ — колониеобразующая единица гранулоцитов, эритроцитов,
- макрофагов, мегакариоцитов КОЕ-М — колониеобразующая единица макрофагов КОЕ-
- Мгкц — колониеобразующая единица мегакариоцитов КОЕ-Н — колониеобразующая
- единица нейтрофилов КОЕс — колониеобразующая единица селезенки КОЕ-Э —
- колониеобразующая единица эритроцитов КОЕ-Эо — колониеобразующая единица
- эозинофилов КОС — кислотно-основное состояние КСМ — кислые сульфатированные
- мукополисахариды КФК — креатинфосфокиназа ЛГ — лютеинизирующий гормон ЛДГ —
- лактатдегидрогеназа ЛП — липопротеины
- ЛП-липаза — липопротеиновая липаза
- α-ЛП — α-липопротеины (липопротеины высокой плотности) β-ЛП — β-липопротеины
- (липопротеины низкой плотности) ЛПВП — липопротеины высокой плотности ЛПНП —
- липопротеины низкой плотности ЛПОНП — липопротеины очень низкой плотности ЛППП —
- липопротеины промежуточной плотности ЛПС — лихорадоподобное состояние ЛПТ — липотрофин
- ЛХАТ — лецитин-холестерин-ацетилтрансфераза
- ЛЭО — лейко-эритробластическое отношение
- МАИР — Международное агентство по изучению рака
- МВБ — макрофагальный воспалительный белок
- МВЛ — максимальная вентиляция легких
- МВПР — множественные врожденные пороки развития
- Мег-КСФ — мегакариоцитарный колониестимулирующий фактор
- МИТ — монойодтирозин
- М-КСФ — макрофагальный колониестимулирующий фактор
- МОД — минутный объем дыхания
- МОК — минутный объем крови
- МПО — миелопероксидаза
- мРНК — матричная рибонуклеиновая кислота
- МСГ — меланоцитстимулирующий гормон
- мтДНК — митохондриальная ДНК
- МФЗ — мультифакториальное заболевание
- МХБ — макрофагальный хемоаттрактантный белок
- НАД — никотинамидадениндинуклеотид
- НАДФ — никотинамидадениндинуклеотидфосфат
- α-НАЭ — α-нафтилацетатэстераза
- НПС — нижний пищеводный сфинктер
- НЭЖК — неэтерифицированные жирные кислоты
- ОБЭ — относительная биологическая эффективность
- ОЕЛ — общая емкость легких