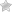Статьи
- Опубликовано в журнале:
- «Российский кардиологический журнал»
- »» N3 2005
Орлов В.А., Гиляревский С.Р., Урусбиева Д.М., Даурбекова Л.В. Российская медицинская академия последипломного образования МЗ и СР РФ, кафедра клинической фармакологии и терапии
Ингибиторы ангиотензин-превращающего фермента (ИАПФ) остаются краеугольным камнем лечения наиболее распространенных сердечно-сосудистых заболеваний.
В последние годы показания для назначения ИАПФ существенно расширились, благодаря доказательствам эффективности ИАПФ, для профилактики неблагоприятных сердечно-сосудистых событий у пациентов высокого риска [1].
В связи с этим, проблемы переносимости ИАПФ продолжают быть актуальными.
Влияние фармакологических свойств ИАПФ на их клиническую эффективность и риск развития побочных эффектов
Большая часть побочных эффектов ИАПФ, как видно из табл. 1, определяется общими для этой группы свойствами, поэтому фармакологические различия между препаратами не должны оказывать большого влияния на частоту развития побочных эффектов за исключением тех, которые определяются наличием в составе молекулы препарата определенной группировки, в частности – сульфгидрильной.
Различия ИАПФ могут касаться химической структуры части молекулы, ответственной за связывание с АПФ, биодоступности, времени полужизни в плазме, пути элиминации, распределения, сродства к тканевому АПФ, а также поступления в организм в виде активного препарата или пролекарства. Ингибиторы АПФ могут быть разделены на три группы в зависимости от химической структуры активной части молекулы.
Каптоприл является прототипом ИАПФ, содержащих сульфгидрильную группу; другие представители этой группы – фентиаприл, пивалоприл, зофеноприл и алацеприл.
Исследования in vitro показали, что наличие сульфгидрильной группы может обуславливать дополнительные свойства препаратов, которые не обусловлены ингибированием АПФ (связывание свободных радикалов, влияние на синтез простагландинов [2; 3]). Однако эти данные не подтверждены в клинических исследованиях.
Среди ИАПФ фозиноприл – единственный препарат, у которого активная часть молекулы содержит фосфонильную группу. Большинство ИАПФ содержат карбоксильную группу в активной части молекулы. Основные фармакологические свойства некоторых ИАПФ представлены в табл. 2. Каптоприл отличается от других препаратов коротким периодом полужизни в плазме.
За исключением фозиноприла, трандолаприла и спираприла, ИАПФ в основном выводятся почками, что определяет необходимость уменьшения дозы у больных с нарушением функции почек. Большая часть ИАПФ поступает в организм в виде пролекарства, которое становится активным после эстерификации в печени.
Как правило, пролекарства имеют более высокую биодоступность по сравнению с активными препаратами.
Гипотония после приема первой дозы
Все ИАПФ способны вызывать артериальную гипотонию. Снижение АД, наблюдаемое в течение нескольких часов после приема первой дозы ИАПФ, происходит в результате ингибирования ренин-ангиотензиновой системы (РАС). Быстрое снижение АД более вероятно у больных, имеющих исходно высокий уровень ренина и ангиотензина II плазмы, например, у больных, получающих высокие дозы диуретиков [4].
Хотя развитие гипотонии при лечении ИАПФ обычно связывают с приемом первой дозы, она может появиться и на более поздних этапах терапии.
Снижение АД после приема первой дозы обычно небольшое и бессимптомное, не приводящее к нарушению перфузии жизненно важных органов [5, 6].
Однако у небольшой части больных может отмечаться выраженная гипотония, сопровождающаяся симптомами гипоперфузии сердца, головного мозга и почек [7].
Хотя известно, что больные с ХСН имеют повышенный риск эффекта первой дозы, развитие клинически значимой гипотонии, требующей прекращения терапии ИАПФ, отмечается менее чем у 10% пациентов [8]. У больных с неосложненной эссенциальной гипертонией, которые не получают другие антигипертензивные препараты, начало терапии ИАПФ редко сопровождается клинически значимой гипотонией [9].
К факторам, способствующим развитию выраженной гипотонии, относят гипонатриемию [10] и гиповолемию [11], в частности, на фоне приема диуретиков [12], рвоты или диареи.
Пожилой возраст, наличие выраженной и/или осложненной артериальной гипертонией (включая злокачественную или ренин-зависимую реноваскулярную гипертонию) считаются факторами риска значимой гипотонии.
Исходное нарушение функции почек и стеноз почечных артерий также повышают риск развития гипотонии после приема первой дозы ИАПФ. Больным, имеющим один или несколько этих факторов риска, на начальном этапе терапии ИАПФ может потребоваться наблюдение в условиях стационара.
Риск развития гипотонии после приема первой дозы и в начале терапии ИАПФ можно свести к минимуму, если придерживаться определенной тактики.
Особенно важно добиться эуволемического состояния к моменту начала терапии, при необходимости корригируя дегидратацию [12]. Может также потребоваться временный отказ от ограничения употребления поваренной соли или менее жесткое ограничение ее потребления в раннем периоде лечения.
В случае высокого риска развития гипотонии после приема первой дозы или в начале терапии целесообразно использовать небольшую начальную дозу коротко действующего препарата (например, каптоприла в дозе 6,25 мг) [6], а также рекомендовать пребывание в постели после приема начальной дозы. В последующем возможен переход на длительно действующий препарат.
Две характеристики периндоприла определяют безопасность его использования в этих ситуациях: (1) постепенное начало действия; (2) отсутствие значимого гипотензивного действия у нормотоников при назначении в небольших дозах.
Navookarasu N.T. et al. у 80 больных с ХСН в двойном слепом рандомизированном плацебо-контролируемом исследовании сравнивали степень снижения АД после первого приема 2 мг периндоприла, 6,25 мг каптоприла, 2,5 мг эналаприла и 2,5 мг лизиноприла [13]. Измерение АД проводили каждые 30 мин в течение первых 2-х ч.
, а затем каждый час. Максимальное снижение среднего АД составило 5,3±2,5 мм рт. ст. для периндоприла, 13,3±3,3 мм рт. ст. – для эналаприла, 15,0±5,7 мм рт. ст. – для лизиноприла, 16,8±5,7 мм рт. ст. – для каптоприла и 5,9±2,7 мм рт. ст. – для плацебо.
Различия при сравнении с плацебо оказались достоверны для всех препаратов (p
Ингибиторы ангиотензинпревращающего фермента в кардиологической практике
РГМУ
Ингибиторы ангиотензинпревращающего фермента (иАПФ) применяются в клинической практике c 1975 года и к настоящему времени стали одной из наиболее часто используемых групп лекарственных средств для лечения артериальной гипертензии (АГ) и сердечной недостаточности (СН). В патогенезе этих состояний важную роль играет активация двух нейрогуморальных систем организма: ренин–ангиотензин–альдостероновой (РААС) и симпато–адреналовой (САС).
Процесс активации вызывается такими неблагоприятными факторами, как снижение сердечного выброса, ишемия жизненно важного органа, потеря натрия и воды, значимое изменение рH и др.
В результате происходит образование биологически активного вещества–ангиотензина II, которое является мощным вазоконстриктором, стимулирует выброс альдостерона, а также способно повышать активность САС (стимулировать выброс норадреналина). Норадреналин, в свою очередь, может активировать РААС (стимулирует синтез ренина).
В конечном итоге повышение активности этих двух систем организма, вызывая мощную вазоконстрикцию, увеличение ЧСС, сердечного выброса, поддерживает функцию кровообращения на оптимальном уровне, сохраняет гомеостаз организма.
В норме активации прессорных систем организма (РААС и САС) «противостоит» действие депрессорной системы (калликреин–кининовой: ключевое звено–брадикинин), вызывающее системную вазодилатацию. Однако при длительном действии различных патологических факторов, описанных выше, нормальная регуляция нарушается и преобладают эффекты прессорных систем.
иАПФ тормозят эффекты прессорных систем и одновременно являются активаторами депрессорных систем.
Основные эффекты иАПФ обусловлены блокадой ангиотензинпревращающего фермента (рис.
1): устранение вазопрессорного, антидиуретического и антинатрийуретического действия ангиотензина II, усиление сосудорасширяющего, диуретического и натрийуретического действия брадикинина и других эндогенных вазодилататоров (простагландинов J2 и E2, натрийуретического пептида, эндотелиального фактора релаксации), а также опосредованной блокадой активности САС путем торможения синтеза норадреналина. В середине 80–х годов выявлены локальные гормональные системы (прежде всего РААС) в различных органах и тканях организма. Активация тканевых РААС происходит параллельно плазменной (циркулирующей), но действие этих систем различается. Плазменная РААС активируется быстро, но оказывает кратковременные эффекты (рис. 2). Активность тканевых РААС нарастает постепенно, однако сохраняется долговременно. Синтезирующийся в миокарде ангиотензин II активирует протоонкогены и стимулирует гипертрофию и фиброз мышечных волокон. Кроме того, он активирует локальный синтез норадреналина. Аналогичные изменения наблюдаются в гладкой мускулатуре периферических сосудов и приводят к её гипертрофии (рис. 2).
Рис. 1. Нейрогуморальные взаимодействия: ренин-ангиотензин-альдостероновая, симпато-адреналовая и калликреин-кининовая системы
Рис. 2. Системные и локальные эффекты ренин-ангиотензин-альдостероновой системы
V. Dzau выделяет следующие сердечно–сосудистые эффекты иАПФ:
- – системная артериальная вазодилатация (уменьшение посленагрузки на левый желудочек) без развития рефлекторной тахикардии;
- – венозная вазодилатация (увеличение емкости венозной системы, уменьшение преднагрузки);
- – предотвращение дилатации желудочков (кардиопротекция);
- – обратное развитие гипертрофии желудочков (кардиопротекция) и стенки артерий и артериол;
- – коронарная вазодилатация;
- – подавление реперфузионных желудочковых аритмий (кардиопротекция);
- – предотвращение развития толерантности к нитратам и потенцирование вазодилатирующего действия нитратов;
- – уменьшение задержки натрия и воды, увеличение содержания калия.
Первые клинические испытания каптоприла (с 1975 года) показали высокую эффективность при АГ, в том числе резистентной к другим методам лечения. Коммерческий успех каптоприла стимулировал усилия других компаний по поиску новых иАПФ.
В 1980 году был синтезирован эналаприл – иАПФ следующего поколения, характеризующегося пролонгированным действием.
В настоящее время разрешено клиническое применение более 10 препаратов этой группы различных фирм–производителей: эналаприл, рамиприл, лизиноприл, цилазаприл, квинаприл, беназеприл, периндоприл и т.д.
Наряду со свойствами, характерными для каптоприла, они имеют отличительные черты. Для большинства из них характерен пролонгированный эффект, более высокая ингибирующая АПФ активность, различные фармакокинетические свойства. Однако фармакодинамические эффекты этих препаратов сходны между собой.
Классификация иАПФ
Классификация (общепринятой не существует) основана на химической структуре части молекулы, связывающейся с ангиотензинпревращающим ферментом. Препараты подразделяют на 3 группы:
- – иАПФ, содержащие сульфгидрильную группу (каптоприл);
- – иАПФ, содержащие карбоксильную группу или карбоксиалкилдипептиды (лизиноприл, эналаприл, рамиприл, периндоприл, цилазаприл, беназеприл, квинаприл, трандолаприл, спираприл);
- – иАПФ, содержащие фосфорильную группу (фозиноприл).
Реальное клиническое значение имеют некоторые особенности фармакокинетики иАПФ: биодоступность, биотрансформация (действует препарат самостоятельно, т.е. является ли он активным веществом или пролекарством, которое превращается в организме в активные метаболиты), пути элиминации и продолжительность торможения активности ангиотензинпревращающего фермента.
Каптоприл действует как активный препарат, биодоступность – 60%, быстро всасывается, но всасывание его уменьшается на 30–40% при одновременном приеме пищи, поэтому его следует принимать натощак, за 1–1,5 часа до приема пищи. Максимум концентрации в крови наступает через 1 час после перорального приема.
Активность каптоприла (то есть самого вещества) делает реальным его применение в качестве препарата «скорой помощи», в частности, для купирования гипертонических кризов при сублингвальном приеме. Эффект отмечается через 15–20 минут.
Каптоприл имеет короткий период полувыведения из плазмы (2 часа), поэтому требует 3–4–кратного приема в сутки, выделяется преимущественно с мочой.
Все карбоксиалкилдипептиды превосходят каптоприл по длительности действия, так как имеют более длительный период полувыведения и поэтому применяются 1–2 раза в сутки. Они меньше связываются с белками пищи, следовательно, их можно принимать независимо от еды.
Все карбоксиалкилдипептиды за исключением лизиноприла являются пролекарствами, т.е. для образования активных метаболитов требуется биотрансформация этих препаратов в печени.
Из этого следует, что данные препараты необходимо с осторожностью применять у лиц с печеночной недостаточностью, а также то, что они не могут быть использованы в качестве средств «скорой помощи».
Основной путь элиминации практически всех иАПФ, а также их активных и неактивных метаболитов – почечная экскреция. Поэтому у больных с явной или скрытой почечной недостаточностью, особенно у пожилых пациентов, дозы иАПФ должны быть уменьшены.
До начала терапии и в течение первой недели лечения иАПФ желательно контролировать не только уровень креатинина, но и скорость клубочковой фильтрации (проба Реберга). Кроме этого, необходимо не допускать развития гипотензии (АД менее 100/60 мм рт.ст.), не назначать одновременно другие гипотензивные препараты (в частности, диуретики и т.д.).
В отличие от большинства иАПФ новые препараты – спираприл, фозиноприл, трандолаприл – преимущественно инактивируются печенью и выводятся с желчью через кишечник. Следовательно, являются весьма перспективными препаратами для лечения лиц пожилого и старческого возраста, так как у этого контингента больных нередко имеется явная или скрытая почечная недостаточность.
Эналаприл – «пролекарство», в печени превращается в активное вещество – эналаприлат. Биодоступность – 40%, не изменяется при приеме пищи. Максимальная концентрация эналаприлата – через 2–4 часа, период полувыведения – 11 часов. Поражение печени или почек увеличивает время начала и длительность действия.
Периндоприл. При пероральном приеме происходит быстрое всасывание препарата. Биодоступность – 65–70%. Прием пищи замедляет метаболизм периндоприла. Активная форма – периндоприлат, его максимальная концентрация в плазме достигается через 3–4 часа после приема препарата, выводится из организма через почки.
Цилазаприл. Одновременный прием препарата с пищей несколько замедляет абсорбцию. Биодоступность – 45%. В печени цилазаприл метаболизируется в активную форму – цилазаприлат. Выводится – почками, период полуэлиминации составляет 7,5 часов.
Лизиноприл. Его выдающимися фармакокинетическими особенностями являются очень низкая жирорастворимость, отсутствие метаболизма в организме (вследствие низкой липофильности) и экскреция с мочой. Биодоступность – 30–50% и, вероятнее всего, что прием пищи на нее не влияет. Пик концентрации в крови отмечается через 6 часов после приема препарата. Период полувыведения – 12,5 часов.
Хинаприл=квинаприл быстро абсорбируется из желудочно–кишечного тракта, и прием пищи не влияет на абсорбцию. В печени препарат гидролизуется в квинаприлат. Пиковая концентрация квинаприлата в крови регистрируется через 2 часа после перорального приема. Выводится – через почки.
Беназеприл. Биодоступность – 17%. В печени превращается в беназеприлат. Период полувыведения – 11 часов. Экскретируется почками.
Рамиприл. Одновременный прием пищи не влияет на абсорбцию препарата. В печени происходит превращение в рамиприлат, который выводится в основном почками с клиренсом 80–130 мл/мин. Частично экскретируется с калом.
Спираприл в печени гидролизуется в спираприлат, выделяется преимущественно с желчью.
Трандолаприл в печени превращается в активную форму – трандолаприлат, экскретируется преимущественно с желчью.
Фозиноприл при приеме внутрь медленно всасывается, биодоступность 36% и прием пищи снижает ее до 20%, является «пролекарством», в печени метаболизируется в фозиноприлат, который экскретируется почти равномерно в мочу и желчь. Однако при наличии почечной недостаточности фозиноприл фактически полностью элиминируется через желудочно–кишечный тракт, что практически полностью снимает ограничения на его применение у больных с нарушенной функцией почек.
Побочные эффекты иАПФ
иАПФ обладают относительно небольшим количеством побочных эффектов. К основным из них относятся: гипотензия, гиперкалиемия, повышение уровня креатинина, сухой кашель, аллергические реакции. Гипотензия нередко развивается на фоне комбинированной терапии с применением диуретиков, блокаторов медленных кальциевых каналов и т.д.
или у пациентов, имеющих АД не более 110/70 мм рт.ст., и, как правило, носит дозозависимый характер. Поэтому в начале лечения рекомендуется использование малых доз короткодействующего иАПФ каптоприла.
Гиперкалиемия, как правило, встречается на фоне дополнительного приема калийсберегающих диуретиков, а применение препаратов с внепочечным путем выведения снимает ограничения на использование иАПФ у больных с почечной недостаточностью. Сухой кашель отмечается у 9–26% больных.
Считается, что сухой кашель развивается в ответ на чрезмерную концентрацию брадикинина в слизистой бронхов. В 90–е годы было обнаружено учащение случаев кашля у больных с ХСН и нарушенной функцией почек. При выраженном кашле целесообразно заменять прием иАПФ антагонистами рецепторов ангиотензина II.
Побочные эффекты каптоприла, связанные с приемом высоких доз (более 150 мг/сут.), как правило, объясняются наличием сульфгидрильной группы и проявляются протеинурией, кожными высыпаниями, нарушением вкусовых ощущений, нейтропенией.
Противопоказания для назначения иАПФ:
– двусторонние стенозы почечных артерий или стеноз артерии единственной почки;
– тяжелый аортальный или митральный стеноз, обструктивная кардиомиопатия;
– исходная гипотензия (АД менее 100/60 мм рт. ст.);
– беременность, лактация.
Лечение артериальной гипертензии ингибиторами АПФ
Опыт лечения АГ с помощью различных иАПФ показывает, что гипотензивное действие развивается у 50–75% больных с различными формами АГ (независимо от активности ренина плазмы крови).
Комбинация с другими препаратами повышает эффективность иАПФ до 75–90%.
В настоящее время выпускается много комбинированных препаратов: иАПФ в сочетании с салуретиком, иАПФ в комбинации с антагонистами кальция.
Гипотензивное действие иАПФ обусловлено снижением ОПСС. Однако не отмечается развития рефлекторной тахикардии, так как блокируется выброс катехоламинов. ЧСС, как правило, остается неизменной. Обычно наблюдается увеличение сердечного выброса.
В отличие от диуретиков и b-адреноблокаторов, иАПФ, как и антагонисты кальция, не оказывают неблагоприятного влияния на углеводный обмен, липидный состав крови и концентрацию мочевой кислоты, т.е. не активируют факторы риска ИБС. Поэтому есть основания для длительного применения иАПФ.
Рекомендуемые дозы иАПФ представлены в таблице 1. Лизиноприл (Диротон) – единственный гидрофильный ингибитор АПФ, не распределяющийся в жировой ткани, с продолжительностью действия 24–30 часов. Эти свойства позволяют считать его препаратом выбора при лечении тучных пациентов с АГ.
В этом плане большой интерес представляет многоцентровое двойное слепое рандомизированное плацебо–контролируемое исследование TROPHY, в котором сравнивалась эффективность 12–недельной терапии 232 больных с ожирением и АГ лизиноприлом и гидрохлортиазидом (под контролем суточного мониторирования АД).
Больные с уровнем ДАД 90–109 мм рт.ст. были рандомизированы на лечение лизиноприлом 10, 20 или 40 мг 1 раз в день, гидрохлортиазидом 12,5, 25 или 50 мг. Средний показатель индекса массы тела статистически достоверно не различался в разных группах больных.
Данные СМАД показали, что лизиноприл и гидрохлортиазид эффективно снижали АД на протяжении суток по сравнению с плацебо (р
Ингибиторы АПФ: препараты нового поколения
Для лечения от гипертонии, сердечной и почечной недостаточностью широко используются средства группы ингибиторов ангиотензинпревращающего фермента. Ингибиторы апф — это такие вещества, которые попадая в организм блокируют ферменты, которые приводят к повышению кровяного давления.
Классификация
Ингибиторы апф список препаратов последнего поколения включает широкий спектр средств, которые предлагает фармакологическая промышленность и они обладают практически одинаковым механизмом действия. Классифицируются они в зависимости от действующего вещества и способа его выведения иАПФ, проводят следующую классификацию:
- Сульфгидрильные. Рекомендуются гипертоникам с ишемической болезнью. Препараты быстро всасываются. Также возможен приём людям страдающим от диабета, болезнями лёгких и сердечной недостаточностью. Так как компоненты средства выводятся почками, то его не рекомендуют тем, кто имеет патологии мочевыделительной системы.
- Карбоксильные. Препараты более длительного действия. Перерабатываются в печени.
- Фосфинильные. Помогают переработать препарат печень и почки. Длительность действия составляет около 1 суток.
АПФ могут быть в комбинации с диуретиками и с антагонистами кальция, которые усиливают гипотензивный эффект, если один ингибитор АПФ уже с поставленной задачей не справляется.
Механизм действия
Не смотря на то, что список лекарств широк, механизм действия у них практически одинаков. Влияя на гормональную систему, которой подконтрольны объём и давление крови человека, ингибиторы АПФ работают над угнетением ангиотензинпревращающего фермента.
Он в свою очередь видоизменяет биологически неактивный ангиотензин I, в ангиотензин II и блокирует рецепторы на которые он влияет. Ангиотензин II представляет собой гормон с сосудосуживающим действием, помимо этого, стимулирует выработку альдостерона надпочечниками.
Альдостерон повышает способность тканей удерживать воду.
Параллельно при помощи усиления работы белков калликреин-кининовой системы, которые отвечают за процессы воспаления в и поддержании кровяного давления, происходит гипотензивный эффект.
АПФ препятствуют распаду брадикидина — гормона, способного расширять сосуды.
Вещества — антагонисты кальция, входящие в состав лекарств иАПФ, способны замедлить проникновение ионов кальция в клетки сердца и сосудов из межклеточного вещества. Тем самым стимулируя снижение его концентрации и расширение сосудов. Диуретические компоненты средств с иАПФ воздействуют на процессы, происходящие в почках.
Показания к применению
Помимо своего главного предназначения, иАПФ направлены на защиту внутренних органов человека. Действующие вещества помогают работе качающего кровь аппарата, почкам, а также сосудам. При хронической почечной недостаточности помогают страдающим восстанавливать здоровье и лучше чувствовать себя.
Ингибиторы АПФ применяются при следующих показаниях:
- при гипертонии;
- ишемической болезни;
- атеросклерозе;
- поражение почек на фоне сахарного диабета;
- сердечная недостаточность хронического типа;
- инфаркт;
- постинфарктное состояние.
Препараты
Наука не стоит на месте и придумывает всё новые и новые средства для борьбы с повышенным давлением, усердно пополняя их списки.
Капотен
Активные субстанции подавляют образование гормона, который приводит к сужению сосудов. Благодаря этому действию значительно снижается АД.
Функциональные элементы снимают напряжение с правого предсердия и соответственно с малого круга кровообращения. Способствует уменьшению выведения надпочечниками гормона альдостерона, который задерживает в тканях воду, а также провоцирует переход жидкости и натрия из кровеносных сосудов в ткани.
Выводятся вещества в основном при помощи почек. Применяется при:
- повышенном кровяном давлении;
- сердечная недостаточность в хронической форме;
- после инфаркта, для восстановления функции левого желудочка;
- при нефропатии на фоне сахарного диабета 1 типа;
Нежелательные последствия:
- сердечные отёки, учащённое сердцебиение;
- снижение АД;
- возможны аллергические реакции в виде отёков на лице, глотке и гортани;
- головная боль, сонливость;
- сухость во рту, диарея, боли в животе.
Беназеприл
Ингибитор, который расщепляясь в организме превращается в субстанцию которое подавляет выработку организмом гормона, который способствует сужению сосудов и провоцирует накоплению воды, окружающими тканями. Применяется для снижения патологии. Относится к препаратам нового поколения.
Побочные эффекты:
- усталость;
- сбои в пищеварении;
- возможны аллергические отёки.
Зофеноприл
Компоненты снижают уровень гормона, который обладает сужающим влиянием на сосуды. А также при понижении этого действующего элемента снижается уровень альдостерона, который задерживает лишнюю воду в окружающих тканях. Уменьшается нагрузка на миокард и повышается уровень кровоснабжения в нём.
При длительном применении оказывает терапевтический эффект на миокард левого желудочка и способствует уменьшению его патологического увеличенного размера.
Рекомендуется при умеренно повышенном АД и после инфарктов, после которых развилась сердечная недостаточность.
Побочный результат:
- нервные явления, утомляемость, депрессия;
- невозможность сконцентрироваться на предмете, шум в голове;
- патология пищеварения, рвота, понос, гепатит;
- одышка, кашель;
- снижение гемоглобина;
- аллергические реакции.
Эналаприл
Компоненты при попадании в организм подвергаются расщеплению, а затем, то активное вещество, которое образовалось уменьшает выработку гормона который сужает сосуды, из-за этого нарушается выработка Функциональных субстанций, которые приводят к накоплению в тканях излишней жидкости.
При этом снижается нагрузка на сердечную мышцу. При длительном приёме медикамента снижается риск сердечной недостаточности. А также улучшается кровообращение в тех участках миокарда, которые подверглись ишемическим изменениям.
Терапевтический результат наступает через 4-6 ч, продолжительностью до 24 ч.
Побочные эффекты:
- патология почек;
- сильное снижение кровяного давления;
- диспепсические расстройства;
- одышка, кашель;
- аллергия, дерматиты;
- снижение либидо.
Квинаприл
Действующие элементы снижают гипертонию и устраняют прогрессирование сердечной недостаточности.
Побочный результат:
- анемия;
- бессонница;
- патология работы желудка и кишечника;
- аллергия;
- болезни почек;
- понижение либидо.
Применение одновременно с диуретиками, усиливает его свойство.
Ренитек
Активные компоненты снижают кровяное давление, снижают риск сердечной недостаточности. Обладает длительным эффектом.
Побочные эффекты:
- шум в голове;
- повышенная утомляемость, является следствием нарушения работы нервной системы;
- обморок;
- патологии почек;
- аллергические реакции;
- нарушение сердцебиения;
- инсульт или инфаркт на фоне гипотонии;
- расстройство пищеварения;
При лечении этим препаратом, необходим контроль работы почек.
Рамиприл
Компоненты оказывают сосудорасширяющее действие, также повышается минутный объём сердца и его сопротивляемость к нагрузкам. Применение этого медикаменты будет хорошей профилактикой инсультов и инфарктов.
Побочные результаты:
- головная боль, нарушение сна;
- желтуха;
- расстройство пищеварения;
- кашель;
- анемия;
- облысение;
- понижение либидо.
Трандолаприл
Функциональные элементы обладают гипотензивным влиянием, защищают миокард от перегрузок, расширяют сосуды.
Побочные результаты:
- неприятные ощущения в груди;
- аритмия;
- снижение гемоглобина;
- инфаркты на фоне низкого давления;
- нервные явления;
- инсульт;
- судороги;
- патология пищеварения;
- патологии почек;
- расстройство дыхания.
При одновременном приёме бета-адреноблокаторов усиливается эффект снижения гипертонии.
Капозид
Препарат комбинированного типа, он понижает АД и обладает диуретическим свойством. Усиливает кровоток в сосудах сердца и почках.
Побочное влияние:
- инфаркты и инсульты при гипотонии;
- расстройство сердечного ритма;
- боли в голове;
- отёк Квинке;
- нарушение работы желудка и кишечника;
- анемия.
Корипрен
Это медикамент в сочетанном действии с антагонистами кальция, активные вещества являются блокаторами кальциевых каналов. Механизм основан на расслабляющем эффекте гладких мышц сосудов, благодаря подавлению проникновения в них и в клетки сердца кальция. Действующие вещества снимают сосудосуживающее влияние гормонов.
Побочный результат:
- головокружение;
- отёк Квинке;
- рези в животе;
- кашель;
- снижение гемоглобина:
- патология печени;
- анемия на фоне разрушения эритроцитов;
Нужно подходить к лечению осторожно, особенно пациентам с почечной недостаточностью.
Триапин
С помощью лекарства расширяются кровеносные сосуды и подавляется гормон их сужающий. Через 1-2 часа наступает гипотензивное действие.
Побочное действие:
- аллергия;
- конъюнктивиты;
- бессонница;
- нарушение сознания;
- плохая концентрация внимания;
- учащённое сердцебиение;
- инфаркт;
- ишемический инсульт;
- кашель;
- одышка;
- потеря аппетита;
- отёк Квинке;
- рвота, тошнота;
- патология пищеварения.
В заключение можно отметить, что у всего перечня имеются противопоказания, с которыми необходимо ознакомиться. Дозировку и схему лечения подбирает только лечащий врач, учитывая индивидуальные особенности пациента.
Противопоказания
В некоторых случаях стоит воздержаться от приёма средств иАПФ. Противопоказаниями являются:
- беременность и лактация;
- возраст до 18 лет;
- непереносимость компонентов препарата;
- нарушение работы почек;
- пониженное давление;
- сужение аорты;
- превышение калия в крови.
Следует проявить осторожность, если есть такие патологии как гепатит, цирроз, анемия, тромбоцитопения, агранулоцитоз и пониженное систолическое давление (ниже 90)
Применение ингибиторов АПФ в клинической практике | #09/05 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи
Ингибиторы ангиотензинпревращающего фермента (АПФ) применяются в кардиологии в течение почти 30 лет. За это время благодаря большому количеству крупных исследований была доказана эффективность этой группы препаратов при лечении артериальной гипертонии (АГ), сердечной недостаточности (СН), дисфункции левого желудочка (ЛЖ), гипертонической и диабетической нефропатии.
В настоящее время к ингибиторам АПФ относятся большое количество лекарственных средств, различающихся по физико-химическим и фармакокинетическим свойствам.
В зависимости от характера группы, которая непосредственно связывается с активным центром АПФ, все ингибиторы АПФ делятся на три категории: сульфгидрильную (беназеприл, каптоприл), карбоксильную (цилазаприл, эналаприл, лизиноприл, периндоприл, рамиприл, спираприл, трандолаприл) и фосфонильную (фозиноприл).
Большинство ингибиторов АПФ, кроме каптоприла и лизиноприла, являются пролекарствами и превращаются в активные метаболиты в печени или желудочно-кишечном тракте.
Пролекарства более липофильны и после превращения в активные метаболиты лучше проникают в органы-мишени, однако у пациентов с заболеваниями и нарушениями функции печени наблюдается торможение активации ингибиторов АПФ при первом прохождении через нее, что необходимо учитывать при выборе препарата.
В основном ингибиторы АПФ и их метаболиты выводятся почками, а такие из них, как фозиноприл, трандолаприл и спираприл, — как с мочой, так и с желчью.
Капотен обладает небольшой продолжительностью действия, в связи с чем его необходимо назначать 3–4 раза в сутки, остальные ингибиторы АПФ характеризуются пролонгированным действием и их можно назначать 2 или 1 раз в сутки.
Все ингибиторы АПФ обладают одинаковым механизмом действия — ингибированием АПФ что приводит к уменьшению образования ангиотензина II из ангиотензина I благодаря снижению его уровня в крови и тканях.
При этом снижаются как секреция альдостерона и вазопрессина, так и активность симпатической нервной системы.
Ингибиторы АПФ подавляют кининазу II, вследствие чего происходит торможение распада брадикини-
на — мощного стимулятора высвобождения эндотелийзависимых факторов релаксации: оксида азота, эндотелийзависимого фактора гиперполяризации и простациклина.
Основные терапевтические эффекты ингибиторов АПФ следующие:
- снижение общего периферического сосудистого сопротивления;
- уменьшение пред- и постнагрузки ЛЖ;
- усиление натрийуреза;
- уменьшение гипертрофии стенки сосудов и миокарда;
- улучшение функции эндотелия;
- уменьшение агрегации тромбоцитов.
C09A — Ингибиторы ангиотензин-превращающего фермента (АПФ)
В основе основных клинических и фармакологических эффектов ингибиторов АПФ лежит их способность подавлять активность фермента, превращающего ангиотензин I в ангиотензин II (кининазы II, или АПФ), и таким образом влиять на функционирование ренин-ангиотензин-альдостероновой системы (РААС).
Лишь 10—15% ангиотензина II в организме образуется благодаря участию АПФ, существует альтернативный путь его биосинтеза с участием фермента химазы и химазоподобного фермента CAGE.
Кроме того, возможна трансформация ангиотензина I в ангиотензин II при участии тканевого активатора плазминогена, катепсина G, тонина и других биологически активных веществ.
При этом в одних органах и тканях преобладает классический путь образования ангиотензина II (правые отделы сердца), в других — альтернативный (левые отделы сердца, наружная оболочка кровеносных сосудов). В некоторых тканях (сосудистый эндотелий) образование ангиотензина II осуществляется сбалансированно разными путями.
Фармакодинамические эффекты ингибиторов АПФ связаны с блокированием АПФ и уменьшением образования АТ II в крови и тканях, устранением прессорных и других нейрогуморальных его эффектов. При этом, по механизму обратной связи, может увеличиваться уровень ренина плазмы и АTI, а также транзиторно снижаться уровень альдостерона.
Ингибиторы АПФ способны тормозить секрецию альдостерона и вазопрессина, снижать синтез других сосудосуживающих и антинатрийуретических веществ (норадреналина, аргинина-вазопрессина, эндотелина-1), участвующих в патогенезе кардиальной дисфункции и артериальной гипертонии.
Кроме того, АПФ идентичен ферменту кининазе II, участвующему в деградации брадикинина. Брадикинин — мощный вазодилататор, регулирующий микроциркуляцию и ионный транспорт. Брадикинин имеет короткий период жизни и присутствует в кровотоке (тканях) в низких концентрациях, в связи с чем проявляет свои эффекты как местный гормон (паракринно).
Брадикинин способствует увеличению внутриклеточного Са2+, являющегося кофактором для NO-синтетазы, участвующей в образовании эндотелийрелаксирующего фактора (оксида азота или NO).
Эндотелийрелаксирующий фактор, блокирующий сокращение мускулатуры сосудов и агрегацию тромбоцитов, является также ингибитором митоза и пролиферации гладкой мускулатуры сосудов, что обеспечивает антиатерогенное действие.
Брадикинин также стимулирует синтез в эндотелии сосудов ПГЕ2 и ПГI2 (простациклина) — мощных вазодилататоров и тромбоцитарных антиагрегантов. Таким образом, брадикинин и кининовая система являются противодействующей для ренинангиотензинальдостероновой системы .
Блокирование АПФ потенциально повышает уровень кининов в тканях сердца и сосудистой стенки, что обеспечивает антипролиферативный, антиишемический, антиатерогенный и антиагрегантный эффекты. Кинины способствуют увеличению кровотока, диуреза и натрийуреза без существенного изменения скорости клубочковой фильтрации. ПГ Е2 и ПГI2 также обладают диуретическим и натрийуретическим действием и увеличивают почечный кровоток.
Таким образом, различают следующие основные фармакологические эффекты ингибиторов АПФ:
Нейрогуморальные
- Уменьшение образования ангиотензина II, а также синтеза и секреции альдостерона и ослабление основных эффектов РААС.
- Уменьшение высвобождения антидиуретического гормона.
- Накопление кининов в тканях и крови и потенцирование эффектов, реализующихся преимущественно благодаря активации В2-брадикининовых рецепторов.
- Снижение активности симпатико-адреналовой системы.
- Повышение парасимпатического тонуса, оптимизация барорефлекторных кардиоваскулярных механизмов.
- Увеличение высвобождения NO (эндотелиального фактора расслабления), простагландинов I2 и Е2, предсердного натрийуретического пептида, тканевого активатора фибриногена.
- Уменьшение секреции эндотелина-1 и образования ингибитора активатора плазминогена типа 1.
Гемодинамические
- Снижение системного АД, ОПСС и посленагрузки (системное расширение артериальных сосудов).
- Снижение преднагрузки (расширение венозных сосудов).
- Улучшение регионального кровообращения в сердце, почках, отделах ЦНС и других органах.
- Потенцирование зависимой от эндотелия вазодилатации, индуцируемой ацетилхолином и серотонином.
- Потенцирование эффектов нитропруссида натрия и предотвращение развития толерантности к нему (по данным ряда авторов)
Кардиальные
- Обратное развитие ГЛЖ, миокардиофиброза и уменьшение объемов камер сердца.
- Замедление темпов ремоделирования сердца, предотвращение дилатации левого желудочка.
- Защита кардиомиоцитов (сохранение макроэргических фосфатов и цитозольных ферментов в клетке при ишемии).
- Антиаритмический эффект.
Сосудистые
- Антипролиферативный и антимиграционный эффект в отношении ГМК, нейтрофилов и моноцитов.
- Улучшение функции эндотелия.
- Антитромбоцитарный эффект, потенцирование эндогенного фибринолиза.
- Профилактика повреждения атеросклеротической бляшки.
- Улучшение податливости сосудистой стенки.
Почечные
- Расширение афферентных (приносящих) и в еще большей мере эфферентных (выносящих) артериол почечных клубочков и как следствие — уменьшение выраженности внутриклубочковой гипертонии.
- Повышение натрийуреза и диуреза с задержкой калия в организме (калийсберегающее действие).
- Увеличение кровотока в мозговом веществе почек.
- Уменьшение размеров пор в клубочковом фильтре в результате сокращения мезангиальных клеток.
- Торможение пролиферации и гипертрофии мезангиальных клеток, клеток эпителия почечных канальцев и фибробластов, уменьшение синтеза компонентов мезангиального матрикса.
Метаболические
- Уменьшение инсулинорезистентности (повышение чувствительности периферических тканей к инсулину).
- Повышение синтеза ЛПВП, распада ЛПОНП и уменьшение синтеза триглицеридов.
- Противовоспалительное действие.
Тканевые эффекты ангиотензина II, а также других эффекторных пептидов РААС — ангиотензиногена, ангиотензина (1—7), ангиотензинов I, III, IV — опосредованы специфическими ангиотензиновыми (АТ-) рецепторами.
В настоящее время идентифицированы АТ1-, АТ2-, АТ4-рецепторы и предполагается существование АТ3- и АТх- рецепторов, однако сердечно-сосудистые эффекты активации РААС реализуются главным образом через АТ1 и АТ2 -рецепторы.
Воздействие ингибиторов АПФ на основные патогенетические звенья при систолической дисфункции левого желудочка и хронической сердечной недостаточности (ХСН) изучено достаточно хорошо.
В развитии кардиопротективного эффекта имеет значение фактор подавления активности нейрогуморальных систем, что сопровождается ослаблением вазоконстрикторных и антидиуретических компонентов патогенеза ХСН.
Структурно-морфологические изменения миокарда, происходящие под влиянием лечения ингибиторами АПФ, заключаются в уменьшении дилатации камер сердца и обратном развития гипертрофии левого желудочка (ГЛЖ), что приводит к повышению сократительной способности миокарда и сердечного выброса, а также улучшению диастолического наполнения желудочков сердца.
В замедлении процесса ремоделирования сердца и сосудов играют роль антиишемический, дезагрегационный эффекты, положительное влияние на функцию эндотелия, подавление пролиферации соединительнотканных элементов стромы миокарда.
Ингибиторы АПФ представляют собой практически единственные пока антигипертензивные препараты, которые одновременно подавляют прессорные системы регуляции АД и активируют вазодепрессорные процессы.
Обладая свойствами нейрогуморальных модуляторов, эти препараты подавляют образование таких сосудосуживающих веществ, как ангио-тензин II, альдостерон, а также норадреналин, аргинин-вазопрессин, эндотелин-1. При этом повышается уровень вазодилататоров: брадикинина, оксида азота, эндотелиального фактора гиперполяризации, простагландинов Е2 и I2.
Результатом гуморальных эффектов ингибиторов АПФ служит выраженное снижение общего периферического сопротивления сосудов (ОПСС) при незначительном повышении ударного и минутного объемов сердца (МОС) без существенного изменения частоты сердечных сокращений.
Снижение системного АД под влиянием ингибиторов АПФ сопровождается улучшением кровотока в органах-мишенях. Длительное применение данных препаратов сопровождается обратным развитием ГЛЖ, замедлением темпов прогрессирования нефропатии, уменьшением явлений ХСН.
Ангиопротективное влияние ингибиторов АПФ заключается в подавлении роста и пролиферации ГМК и фибробластов средней оболочки сосудов, что приводит к уменьшению гипертрофии стенки артерий и увеличению их просвета. Кроме того, ингибиторы АПФ уменьшают явления дисфункции эндотелия и ослабляют вазоконстрикторные реакции.
При лечении больных с разными формами ишемической болезни сердца (ИБС) наряду с гемодинамическими и нейрогуморальным имеют значение антиишемический, антиатерогенный эффекты ингибиторов АПФ, а также их благоприятное влияние на функцию эндотелия. При инфаркте миокарда ингибиторы АПФ оказывают влияние на процессы ремоделирования сердца и сосудов, а также на очаги некроза в миокарде.