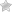Сокращенный перевод статьи
Thrombolitic Therapies: The Current State of AffairsB. Perler, Johns Hopkins Hospital, Baltimore, Meryland, USAJ.Endovasc.Ther. 2005;12:224-232.
Стрептокиназа, выделенная из культуры β-гемолитического стрептококка группы С, является первым фибринолитическим средством, одобренным FDA. Несмотря на эффективность стрептокиназы в лизировании тромбов, высокая частота побочных эффектов в результате ее применения заставила исследователей продолжить работу по поиску новых тромболитиков.
Урокиназный активатор плазминогена начал применяться в клинике в 1940-х годах для лечения ограниченного гематорокса.
В 1957 году урокиназый активатор плазминогена удалось выделить из клеток почки человека и с 1978 года началось промышленное производство препарата урокиназы. Урокиназа стала первым фибринолитическим средством, использовавшимся в терапии тромботических нарушений в США.
За 20 лет клинического применения препарата накоплено значительное количество исследований, доказавших его эффективность в лечении различных заболеваний.
В середине 1980-х, появление рекомбинантных технологий сделало возможным производство альтеплазы (рекомбинантного тканевого активатора плазминогена) и других продуктов генной инженерии, таких как ретеплаза и тенектеплаза. В то время как эти соединения являются более фибрин-специфическими, их клиническое применение выявило ряд побочных эффектов.
Механизм действия тромболитиков
Высокая специфичность к фибрину и фрагменту Х, может вести к повышению побочных эффектов и смертности.
Также было доказано, что дозы рекомбинантного тканевого активатора плазминогена, сохраняющие специфичность к фибрину, относительно неэффективны и реканализация находится в зависимости от степени неспецифичности препарата (5).
Исследования показали, что генетически модифицированные мыши, с отсутствием активности урокиназного активатора плазминогена, обладают существенно более коротким временем тромботической окклюзии, пониженной способностью к восстановлению, более тонкой оболочкой сосудов и более тяжелыми стенозами после повреждения сосудов, чем модифицированные мыши с отсутствием активности тканевого активатора плазминогена (6).
Эти данные подтверждают, что урокиназный активатор плазминогена, возможно в большей степени, чем тканевой активатор плазминогена, участвует в механизмах, отвечающих за состояние сосудов.
Инфаркт миокарда
Основной причиной смертности в США являются сердечно-сосудистые заболевания. Большая часть случаев инфаркта миокарда происходит вследствие острого коронарного тромбоза. Инфаркт миокарда является ведущим показанием для тромболитической терапии и за последние 30 лет накоплен существенный опыт в лечении этого заболевания.
Достоверно доказано, что тромболитическая терапия существенно уменьшает смертность от инфаркта миокарда, в сравнении со стандартами терапии, не включающими тромболизис (7).
Хотя Урокиназа с успехом использовалась в терапии ИМ на протяжении более чем 20 лет, в настоящее время фибрин-специфические агенты (а также стрептокиназа, которая используется редко) утверждены в терапии ИМ.
Исходя из клинической эффективности, решение об использовании фибрин-специфического агента вместо фибрин-неспецифического выглядит необоснованным. При клиническом применении нет разницы между фибрин-специфическими и фибрин-неспецифическими агентами.
Ангиография кровотока коронарной артерии (в исследовании TIMI III) доказала, что величина восстановления проходимости сосуда сходна у пациентов, получающих урокиназу или рекомбинантный тканевой активатор плазминогена (8).
Также было доказано, что, хотя рекомбинантный тканевой активатор плазминогена действует быстрее при инфаркте миокарда, это не увеличивает число пациентов с восстановлением кровотока в поврежденных сосудах или число пациентов с улучшением функции левого желудочка (9).
Несколько клинических исследований показали сравнимую эффективность тромболитических средств в терапии инфаркта миокарда. В исследовании GUSTO, общее число смертей или нефатальных инвалидизирующих инсультов составило 6,9% и 7,8% у пациентов, которым назначались рекомбинантный тканевой активатор плазминогена и стрептокиназа соответственно (р=0,006) (1).
Однако, функция левого желудочка не различалась в группах после 90 минут и после 1 недели лечения, а альтеплаза обладала более высокой стоимостью ($32 678 за год спасенной жизни и $100 000/год среди пациентов меньше 40 лет), по сравнению со стрептокиназой (10).
В исследовании COBALT, которое проводилось позднее GUSTO, но включало те же критерии, был выявлен более высокий 30-дневный уровень смертности в группе рекомбинантного тканевого активатора плазминогена (ТАП), составивший 7,53%. Похожие данные были получены в исследовании GUSTO III, где 30-ти дневная смертность на фоне применения рекомбинантного ТАП составила 7,24% (14).
Учитывая результаты более ранних исследований, показавших отсутствие существенных различий в эффективности тромболитических препаратов, доказательная база большей эффективности фибрин-специфических агентов в сравнении с фибрин-неспецифическими выглядит сомнительной (11,12). К тому же, последние метаанализы отмечают отсутствие достоверной разницы в уменьшении смертности между различными тромболитическими агентами (13,14).
В то время как уменьшение смертности при инфаркте миокарда сходна у всех типов тромболитиков, они отличаются по оказываемым побочным эффектам.
В исследовании GUSTO, пациентов, которым понадобились последующие ангиографические процедуры было на 0,5% больше в группе рекомбинантного ТАП, а пациентов, которым было проведено коронарное шунтирование, было на 0,8% больше, чем в группе стрептокиназы (15).
В этом исследовании также было отмечено повышение числа геморрагических инсультов в группе рекомбинантного ТАП по сравнению с группой стрептокиназы (15).
Метаанализ 15 исследований, оценивающих тромболитическую терапию при инфаркте миокарда (включая исследования II и III фазы), большинство из которых проводили с использованием фибрин-специфических агентов, показал статистически достоверное повышение внутричерепных геморрагий (р=0,01) (16).
Объединенная группа FTT проанализировала все доступные исследования, и нашла явное доказательство общей пользы применения фибринолитической терапии для группы пациентов с инфарктом миокарда, хотя на фоне тромболитической терапии наблюдалось 4 дополнительных инсульта на 1000 человек, из которых 2 были фатальными (7).
Высокая смертность и инвалидность усиливает потребность в эффективной терапии, которая в то же время вызывает меньшее количество внутричерепных геморрагий. Таким образом, риск внутричерепной геморрагии (ВЧГ) является определяющим фактором при выборе соответствующей терапии.
Пациенты, старше 65 лет с инфарктом миокарда обладают повышенным почти в 9 раз риском этого опасного осложнения (17). В то же время, пожилые пациенты имеют самый высокий риск заболеваемости ИМ и самый высокий риск развития внутричерепной геморрагии после использования фибрин-специфических тромболитиков.
Поскольку уменьшение смертности примерно равна при использовании различных тромболитиков, наиболее разумно при выборе терапии отдавать предпочтение препаратам с наиболее низким риском возникновения побочных эффектов.
В данное время исследователи изучают эффективность комбинации различных коагулянтов для повышения уровня реперфузии. Например, для изучения возможного уменьшения смертности изучали добавление половинной дозировки тромболитиков к ингибитору гликопротеина IIb/IIIa. Текущие клинические тенденции повысили потребность в эффективной тромболитической терапии с низким профилем побочных реакций.
Исследователи считают, что такие фибрин-неспецифические агенты, как урокиназа могут быть лучшим выбором в терапии инфаркта миокарда.
Список литературы
- The GUSTO Investigators. N Engl J Med. 1993;329:673-682.
- Gruppo Italiano per lo Studio della Soppravvivenza nell’Infarcto Miokardico. Lancet. 1990;336:65-71.
- Third International Study of Infarct Survival Collaborative Group. Lancet. 1992;339:753-770.
- Weitz JI. J Vasc Interv Radiol. 1995;6:19S-23S.
- Gurevich V. Blood Coagul Fibrinolysis. 2000;11:401-408.
- Schafer K, Konstantinidis S, Riedel C, et al. Circulation. 2002;106:1847-1852.
- Fibrinolitic Therapy Trialists’ (FTT) Collaborative Group. Lancet. 1994;343:311-322.
- Ohman EM, Harrington RA, Cannon CP, et al. Chest. 2001;119:253S-277S.
- Collins R, Peto R, Baigent C, et al. N Engl J Med. 1997;336:847-860.
- Mark DB, Hlatky MA, Califf RM, et al. N Engl J Med. 1995;332:1418-1424.
- Assesment of the safety and Efficacy of a new Thrombolytic (ASSENT-2) Investigators. Lancet. 1999;354:716-722.
- International Joint Efficacy Comparison of Thrombolytics (INJECT) Investigator. Lancet. 1995;346:329-336.
- Dundar Y, Hill R, Dickson R, et al. QJM. 2003;96:103-113.
- Neuhaus KL, Tebbe U, Gottwick M et al. J Am Coll Cardiol. 1988;12:581-587.
- GUSTO Angiographic Investigators. N Engl J Med. 1993;329:1615-1622.
- Eikelboom JW, Mehta SR, Pogue J, et al. JAMA. 2001;285:444-450.
- Gurwitz JH, Goldberg RJ, Chen Z, et al. Arch Intern Med. 1994;154:2202-2208.
Вопросы и ответы
Пациентам важно понять, что для растворения тромбов в сосудах не подходят методы народной медицины и эту терапию невозможно проводить в домашних условиях. Все «народные средства», что предлагаются «целителями» для растворения тромбов в венах нижних конечностей не более чем мошенничество и введение в заблуждение. Никакие настойки, даже если им дать настояться не могут предотвратить образование сгустков крови. Только специальные препараты тромболитики и производные гепарина, применяемые для разжижения крови могут избавить человека от тромбов и предотвратить их появление.
В Инновационном сосудистом центре разработана технология экстренного тромболизиса, позволяющая в кратчайшие сроки растворять тромбы в сосудах для предупреждения развития смертельно опасных осложнений.
Как проводится катетерное растворение кровяных сгустков
Лечение проводится в условиях рентгеновской операционной. Под местной анестезией сосудистый хирург проведёт прокол вены или артерии. Место пункции выбирается соответственно локализации тромботической закупорки, чтобы путь до тромба был кратчайшим.
Через прокол тонкая пластиковая трубка вводится в сосуд и под контролем рентгеновского аппарата проводится к месту тромбоза. Лекарство, растворяющее тромбы, вводится через трубку и в сгусток.
При необходимости через трубку вставляется небольшая машина для разрушения или всасывания сгустка.
После растворения тромбов часто обнаруживаются различные патологические процессы в подвздошной или подключичной вене (синдром Мея-Тернера, перетяжки, сужения, сдавление на выходе из грудной клетки) или в артерии — атеросклеротические бляшки. Эти проблемы с помощью ангиопластики и/или стента возможно устранить уже во время процедуры растворения сгустков. Либо позже проводится отдельное хирургическое вмешательство.
После лечения
Вы можете провести день в палате интенсивной терапии (ПИТ). Вам будут назначены антитромботические препараты (гепарин) в течение 12-14 часов для снижения свёртываемости крови.
После успешного лизиса сгустков в венах необходимо применять компрессионный чулок или рукав для ускорения оттока крови.Ваш сосудистый хирург, вероятно, порекомендует вам принимать средства, разжижающие кровь (ацетилсалициловую кислоту или ксарелто).
Возможно, для уменьшения вязкости крови назначат препарат Vessel Due F.
Риски, противопоказания и осложнения
Хотя растворение может безопасно и эффективно улучшить кровоток и устранить симптомы тромбоза у многих пациентов, оно не рекомендуется для всех. Тромболизис не может быть рекомендован пациентам, которые используют разжижающие кровь лекарства, травы или пищевые добавки, или людям с определёнными состояниями, связанными с повышенным риском кровотечения. Эти условия включают в себя:
- Высокое кровяное давление
- Активное кровотечение или тяжёлая кровопотеря
- Геморрагический инсульт
- Тяжёлая болезнь почек
- Недавняя операция
- Тромболизис также может быть связан с повышенным риском осложнений у пациенток, которые беременны или находятся в преклонном возрасте, а также у людей с другими заболеваниями.
- Пациенты, которые подвергаются тромболизису, имеют небольшой риск инфицирования (менее одного на 1000), а также небольшой риск аллергической реакции на контрастный краситель, который может потребоваться для визуализации.
- Помимо риска серьёзного внутреннего кровотечения, другие возможные риски включают:
- Кровоподтёки или кровоизлияния в месте доступа
- Повреждение кровеносного сосуда
- Миграция сгустка крови в другую часть сосудистой системы
- Повреждение почек у пациентов с сахарным диабетом или другими ранее существовавшими заболеваниями почек
- Наиболее серьёзным возможным осложнением является внутричерепное кровотечение, которое потенциально смертельно. Но это осложнение встречается редко. Кровоизлияние в мозг, вызывающее инсульт, встречается менее чем у 1% больных.
Прогноз
Хотя тромболизис обычно успешен, препараты не способны растворить тромбы у 25% пациентов. Ещё у 12% пациентов впоследствии развивается тромб или закупорка в кровеносном сосуде.
Тромболизис сам по себе не может оживить ткани, которые уже были повреждены нарушенным кровообращением, поэтому может потребоваться дальнейшее лечение для устранения основных причин тромба и восстановления повреждённых тканей и органов. Своевременное растворение также может предотвратить развитие посттромботической болезни и образование трофических язв на ногах.
Фарматека » проблема выбора тромболитического препарата при остром инфаркте миокарда
В статье представлен краткий исторический обзор развития тромболитической терапии при остром инфаркте миокарда и основные сведения о тромболитических препаратах, присутствующих на отечественном фармацевтическом рынке.
Обсуждены результаты проведенных исследований по сравнению этих препаратов.
С четом особенностейфармакокинетики и фармакодинамики, а также клинических эффектов предложены возможные алгоритмы выбора тромболитического препарата в некоторых клинических ситуациях.
Тромболитическая терапия (ТЛТ) признана одним из 10 величайших достижений кардиологии XX в. [1].
Несмотря на внедрение первичной коронарной ангиопластики при остром инфаркте миокарда, тромболизис не теряет своего значения с учетом логистических особенностей нашей страны с большими расстояниями до специализированных инвазивных центров.
Напротив, масса больных до сих пор остаются вообще без реперфузионных вмешательств, поэтому проблема внедрения тромболизиса продолжает оставаться актуальной для отечественного здравоохранения.
Некоторые исторические аспекты
В 1933 г. W. Tillet и соавт. обнаружили свойство стрептококковых культур лизировать кровяной сгусток.
Это была группа А β-гемолитического стрептококка, продуцирующая некую «фибринолитическую» субстанцию, которую авторы назвали «стрептококковый фибринолизин» [2]. В 1945 г. L.R.
Christensen показал, что в плазме крови человека находится фермент плазминоген, который под действием стрептококкового фибринолизина, названного им стрептокиназой (СК), превращается в активный фибринолитический фермент плазмин [3].
В 1948 г. S. Sherry и соавт. сообщили о первом опыте применения СК в клинике для лизиса гнойного плеврального экссудата, содержащего фибриновые пленки [4]. В 1958 г. A.P. Fletcher и соавт.
опубликовали сообщение о первом внутривенном введении СК больным инфарктом миокарда [5].
Впервые было показано, что применение СК этими больными может снижать летальность, поэтому это является перспективным подходом к лечению больных острым инфарктом миокарда (ОИМ).
Параллельно были попытки использовать не активатор плазминогена, а уже активированный плазмин [6]. Отечественные ученые под руководством Г.В. Андреенко и Б.А. Кудряшова в 1961 г. создали аналогичный препарат под названием «Фибринолизин», который долго использовался в клинической практике [7].
Выше представлен «генеральный» путь развития тромболитической терапии. Естественно, были и «тупиковые» направления на этом пути. В частности, параллельно с исследованием СК в качестве тромболитика группой I. Innerfield активно изучался трипсин [8].
В исследованиях на животных (кроликах и собаках) была показана тромболитическая эффективность трипсина при внутривенном введении. При этом наблюдалось значительное уменьшение концентрации фибриногена в крови и увеличивалось протромбиновое время. Кроме тромболитического был обнаружен выраженный противовоспалительный эффект.
После этого проведены клинические испытания на больных различными заболеваниями: тромбофлебиты, артриты, инсульты, коронарный тромбоз. Тромболизис трипсином был проведен 538 пациентам (!) [9]. В т.ч. были 7 больных с клиникой острого коронарного синдрома, 3 из них – с ОИМ.
Среди этих больных один умер, у остальных отмечено значительное улучшение состояния, которое сопровождалось снижением частоты приступов стенокардии, положительными изменениями на ЭКГ и биохимических параметров. Таким образом, первое введение тромболитика больным ОИМ было проведено в 1952 г. группой I. Innerfield.
С учетом большой частоты побочных эффектов, особенно при быстром введении, что требуется при ОИМ, трипсин проиграл в сравнении со СК и в настоящее время в качестве тромболитика не используется.
Классификация тромболитических агентов
По механизму действия все тромболитические средства можно разделить на 3 группы [10]:
Прямые фибринолитики, которые непосредственно разрушают молекулу фибрина. К ним относятся основной естественный фермент тромболитической системы человека плазмин, его лекарственная форма фибринолизин и некоторые грибковые протеазы.
- Активаторы плазминогена: СК, стафилокиназа, тканевой активатор плазминогена и активатор плазминогена урокиназного типа.
- Непрямые фибринолитики.
- Вещества третьей группы не вызывают непосредственной активации плазминогена и не оказывают прямого лизирующего воздействия на фибрин. Они усиливают фибринолиз относительно мягко – путем следующих механизмов:
- повышения биосинтеза плазминогена или его активаторов (анаболические стероиды, никотиновая кислота);
- усиления высвобождения активаторов плазминогена из тканей (гистамин, брадикинин, гепарин, простагландины);
- инактивации естественных ингибиторов фибринолиза;
- специфических антител, солей тяжелых металлов;
- изменения структуры фибриногена или фибрина (Арвин или Анкрод, дефибраза, фибринспецифические антитела).
Из препаратов первой группы в клинической практике использовался только фибринолизин.
Выдающимся достижением отечественной кардиологии стало внутрикоронарное введение фибринолизина при ОИМ, которое впервые в мире 5 июня 1975 г. выполнили кардиологи под руководством Е.И. Чазова [11].
В настоящее время в результате появления новых более эффективных препаратов фибринолизин утратил свое значение.
Непрямые фибринолитики активируют фибринолиз достаточно слабо и поэтому в качестве тромболитиков, тем более при остром тромбозе, не используются. Широко применяется только гепарин, но не как активатор фибринолиза, а как антикоагулянт. Для проведения лекарственного тромболизиса при инфаркте миокарда в настоящее время используются только активаторы плазминогена.
Активаторы плазминогена в свою очередь делятся на тромболитики:
- 1-го поколения (фибриннеспецифичные: СК и УК);
- 2-го поколения (фибринспецифичные: алтеплаза, проурокиназа, рекомбинантная стафилокиназа);
- 3-го поколения (генномодифицированные: тенектеплаза, Пуролаза, Фортелизин).
СК: начало многоцентровых клинических исследований
Первым из этих препаратов считается СК. СК образует комплекс с плазмином, молекула которого при этом изменяется и обнажается его активный центр.
Комплекс СК–плазминоген играет роль фермента в дальнейшем превращении плазминогена в плазмин, причем он активирует как связанные с фибрином, так и свободно циркулирующие молекулы плазминогена.
Как следствие – плазмин лизирует не только фибрин, но и фибриноген, циркулирующий в крови, чем и объясняется снижение фибриногена на фоне тромболизиса. СК антигенна, поэтому титры антистрептокиназных антител быстро нарастают в течение нескольких дней после введения препарата, делая неэффективным и небезопасным его повторное применение.
Самым частым побочным эффектом/осложнением СК является гипотония: снижение систолического артериального давления до 80 мм рт.ст. и ниже наблюдается у 30–40% пациентов [12]. Эта гипотония не является проявлением аллергической реакции, тем более анафилаксии, как это иногда объясняется. СК – это неспецифический тромболитик.
Параллельно с превращением плазминогена в плазмин происходит активация калликреин-кининовой системы, превращение брадикининогена в брадикинин, который и снижает АД [13, 14]. Брадикинин полностью исчезает при однократном прохождении через легочное русло, поэтому этот гипотензивный эффект кратковременный и не представляет опасности для жизни пациента.
Для его купирования вводят небольшие дозы мезатона или «почечные» дозы допамина в виде инфузии.
Напротив, существует мнение, будто снижение АД является маркером эффективности ТЛТ. Чем более эффективна ТЛТ, тем больше образуется не только плазмина, но и брадикинина, тем сильнее должно снижаться АД, хотя статистически это не подтверждено.
В 1960–1970‑х гг. проведены исследования по подбору оптимальных доз и режимов введения СК. Наиболее распространенный, «классический», метод введения СК был предложен в 1981 г. R. Schroder и соавт. и заключается во внутривенной инфузии 1,5 млн ЕД СК за 60 минут [15]. Именно так проводился тромболизис в большинстве исследований. В начале 1980‑х гг.
было проведено первое многоцентровое исследование эффективности тромболизиса при ОИМ, известное как GISSI-1 [16]. В это итальянское исследование были включены 11 806 больных ОИМ, половине из которых в течение первых 12 часов заболевания было введено 1,5 млн ЕД СК в течение часа. Конечной точкой исследования стала летальность.
Впервые было показано, что:
Применение тромболизиса снижает летальность при ОИМ.
Эффективность тромболизиса зависит от промежутка времени между началом заболевания и введением СК. При начале терапии в первый час заболевания, в первые 2–3 и 3–6 часов летальность составила соответственно 8,2, 9,2 и 11,7% против 14,1% в контрольной группе без ТЛТ. Выходит, чем раньше начинается ТЛТ, тем выше ее эффективность.
Эти выводы принципиально были подтверждены в исследовании ISIS-2 [17]. Более 17 тыс. больных были рандомизированы в 4 группы: СК, аспирина, СК+аспирин и контрольную.
Оказалось, что 5-недельная летальность в группе СК снизилась на 25%, в группе аспирина – на 23%, в группе СК+аспирин – на 42%. Т.е. дополнительно к подтверждению эффективности СК была продемонстрирована высокая эффективность аспирина.
Результаты вышеперечисленных исследований стали доказательной основой современной стратегии лечения ОИМ: как можно раньше назначать ТЛТ, аспирин и гепарин.
Проведенный мета-анализ результатов исследований с ангиографическим контролем показал, что при введении СК частота реперфузии коронарной артерии (КА) составляет на 60 минут лечения в среднем 44%, на 90 – 48%, через 3 часа – 72%, а от 24 часов до 21 суток – от 75 до 85%, что статистически значимо выше, чем в контрольной группе без тромболизиса [18].
СК или алтеплаза?
Тканевой активатор плазминогена (ТАП), выделенный в начале 1980 гг., – это белок, который синтезируется эндотелиальными клетками сосудов. В отличие от СК, активирующая плазменный плазмингоген, вызывая системное литическое состояние, ТАП переводит тканевой плазминоген в активный тромбин только в присутствии фибрина.
Таким образом, он является фибриноспецифичным и не обладает выраженным системным действием, хотя при увеличении дозы препарата эта фибриноспецифичность исчезает. Во время тромболизиса ТАП происходит активная выработка тромбина, что определяет обязательную необходимость комбинировать ТАП с внутривенным введением гепарина.
ДНК-рекомбинантным методом был создан промышленный продукт – алтеплаза. В отличие от СК он имеет короткий период инактивации. Период его полураспада составляет 4–8 минут, что требует продолжительного введения для поддержания терапевтической концентрации в крови.
При первых испытаниях алтеплазы для лечения ОИМ ее назначали в общей дозе 150 мг в течение 3 часов, затем схему поменяли на 100 мг за 90 минут.
В 1980‑1990-х гг. проводились сравнительные исследования СК и алтеплазы. В нескольких исследованиях с ангиографическим контролем было показано, что 3-часовая инфузия алтеплазы достоверно чаще вызывает реперфузию КА на 60 и 90 минут тромболизиса по сравнению с СК [19].
С учетом важного значения скорости реперфузии КА логично было ожидать снижения летальности в группах с алтеплазой, но в исследованиях TIMI-1 (290 больных), GISSI-2 (10372 пациента), ISSIS-3 (41 299 больных) не было обнаружено достоверного различия в летальности между группами СК и алтеплазы. И только в исследовании GUSTO-I, в которое включен 41 021 больной, показано, что ускоренный режим введения алтеплазы (100 мг за 90 минут) позволил уменьшить 30-дневную летальность по сравнению с СК: 6,3 против 7,2% соответственно (р=0,001), т.е. на 0,9% [20]. Казалось бы, преимущество алтеплазы доказано.
Но такая однозначная оценка результатов ограничена следующими обстоятельствами:
Достоверное различие в смертности наблюдалось только среди больных, которые лечились в США. В других странах такого различия не было [21].
В группе алтеплазы развилось больше инвалидизирующих инсультов: 0,72 против 0,54% (р=0,03). При этом комбинированная конечная точка (смерть+инсульт) в группе алтеплазы все-таки осталась ниже: 6,9 против 7,8% (р=0,006). Повышение частоты геморрагических инсультов при применении фибриноспецифических препаратов ТАП по сравнению с СК отмечено также в более позднем мета-анализе [22].
В рамках исследования GUSTO-I проведено подисследование: 2431 больным выполнялась ангиография.
Оказалось, что эффективный кровоток (по ТIMI 2–3) в КА к 90 минам от начала ТЛТ в группе алтеплазы был достигнут в 81% случаев, а в группе СК – только в 60%.
Но через 3 часа различия по этому показателю уже не определялось: 74 и 76% соответственно [23]. Таким образом, СК и алтеплаза одинаково часто открывают КА, но алтеплаза делает это чуть быстрее.
В исследовании GUSTO-I изучалось соотношение стоимость/эффективность тромболизиса алтеплазой по сравнению с СК. Один год спасенной жизни больного в результате проведения тромболизиса не СК, а алтеплазой «стоит» 32,678 долл. США [24]. Это соотношение более эффективно/выгодно при передних инфарктах миокарда и менее эффективно при нижних.
Таким образом, к недостаткам алтеплазы по сравнению с СК относятся высокий риск кровоизлияния в мозг, обязательная необходимость параллельной инфузии гепарина и высокая стоимость. Поэтому при выборе алтеплазы для тромболитической терапии необходимо учитывать не только ее достоинства, но и недостатки.
Тенектеплаза – препарат для болюсного введения
Для улучшения фибринолитических характеристик препарата методом генной инженерии были созданы модификации молекулы ТАП: ретеплаза (рекомбинантный активатор плазминогена, r-PA), ланотеплаза (n-PA) и тенектеплаза (TNK-tPA). Наиболее удачный из них – препарат тенектеплаза (Метализе).
Это молекула с более продолжительным плазменным периодом полувыведения, повышенной специфичностью к фибрину и большей устойчивостью к ингибитору первого типа активатора плазминогена (PAI-1) по сравнению с естественным ТАП, поэтому несомненным преимуществом тенектеплазы является возможность ее однократного болюсного введения.
В исследовании ASSENT-1 была определена наиболее оптимальная доза этого препарата: 30–50 мг в зависимости от веса пациента [25].
С использованием этой дозы в исследовании ASSENT-2 проведено сравнение алтеплазы и тенектеплазы.
Хотя частота нецеребральных кровоизлияний и необходимости гемотрансфузий была несколько меньше в группе тенектеплазы, чем алтеплазы, – 26,4 против 28,9% (p=0,0003) и 4,2 против 5,5% (p=0,0002) соответственно, смертность в течение 30 суток в обеих группах не различалась: 6,18 и 6,15% в группе тенектеплазы и алтеплазы соответственно.
Частота геморрагических инсультов также не различалась и составила соответственно 1,78 и 1,66%. Был сделан вывод об одинаковой терапевтической эфективности обоих препаратов, но отмечена более простая методика применения нового тромболитика [26].
Таким образом, преимуществом тромболитиков 3-го поколения группы ТАП (тенектеплаза) является не более высокая клиническая эффективность и безопасность, а удобство, простота в применении. Поэтому именно этот препарат позиционируется как единственный специальный тромболитик для догоспитального этапа.
Многоцентровых сравнительных исследований стрептокиназы и тенектеплазы не было. Мы провели одноцентровое сравнительное исследование этих препаратов при их введении на догоспитальном этапе [27]. Частота реперфузии через 90 минут по ЭКГ-признакам оказалась выше в группе тенектеплазы: 64 против 48% (р
Тромболитическая терапия ишемического инсульта
Для фибринолиза необходима активация плазминогена до плазмина, которая осуществляется посредством расщепления связи в плазминогене между аргинином (Arg-561) и валином (Val-562) [18].
Расщепление этой связи достигается активаторами плазминогена. В случае с ТАП сначала образуется комплекс ТАП—фибрин, на котором фиксируется плазминоген.
Образование тройного комплекса ТАП—фибрин—плазминоген является сигнальным механизмом для активации плазминогена и превращения его в плазмин [19].
Скорость активации плазминогена в значительной степени зависит от третичной структуры молекулы плазминогена и доступности лизиновых окончаний фибрина [20—22].
Молекула плазминогена может иметь закрытую третичную структуру в виде спиралевидной α-конформации — Glu-плазминоген, которая является основной в кровотоке и устойчивой к активаторам [20, 23].
При контакте плазминогена с интактным фибрином в тромбе происходит отщепление N-концевого участка молекулы плазминогена и образование частично активной переходной формы с β-конформацией [24, 25].
Исходно β-плазминоген обладает незначительной фибринолитической активностью, однако, вступая в контакт с лизиновыми окончаниями молекулы фибрина, переходит в активный Lys-плазминоген с открытой γ-конформацией [23, 24, 26]. По мере нарастания фибринолиза увеличивается количество лизиновых окончаний на фрагментах фибрина, что способствует еще большей активации плазминогена, его активному превращению в плазмин и соответствующему усилению фибринолиза [27].
Основными внутренними активаторами плазминогена являются тканевой и урокиназный активаторы. Тромболитический эффект ТАП (исходное название — фиброкиназа) был установлен в конце 40-х годов XX века [28, 29]. В 1979 г.
был выделен высокоочищенный ТАП [30], затем клонирован ген и синтезирован рекомбинантный вариант [31].
В последующем были созданы модифицированные варианты ТАП, отличающиеся временем полувыведения, фибрин-селективностью и возможностью болюсного введения (табл. 2).
Таблица 2. Рекомбинантный ТАП и его производные Примечание. * — разрешено клиническое применение; # — проводятся экспериментальные и/или клинические исследования. F — пальцевой домен, G — домен, гомологичный ростовому фактору, K1, K2 — подковообразные 1 и 2 и P — протеазный домен.
Исходно молекула ТАП является одноцепочечной и состоит из 527 аминокислот с 5 функционально значимыми областями — доменами (см. табл. 2, 3)
Таблица 3. Функциональные области (домены) молекулы ТАП [31—39]. При ограниченном протеолизе связи Arg275—Ile276 (аргинин—изолейцин) образуется двухцепочечная молекула с 4 доменами на α-цепи и одним доменом на β-цепи [40]. В присутствии фибрина вследствие эффекта аллостерической регуляции обе молекулы имеют одинаковую активность [41].
В организме ТАП фоново секретируется клетками сосудистого эндотелия, обеспечивая атромбогенность сосудистой стенки.
При развитии тромбоза первоначальное взаимодействие ТАП с фибрином происходит при активации F-домена с последующим участием К2-домена, с которым связываются вновь образуемые лизиновые окончания фибрина (см. табл. 3).
В результате плазмин из плазминогена в основном образуется на поверхности фибрина, что обусловливает его фибрин-селективность, преимущественное локальное тромболитическое действие и незначительное системное влияние на гемостаз [42, 43].
Наряду с эндотелием ТАП вырабатывается в других органах и тканях, что обусловливает его системное действие. ТАП выполняет сигнальные, регуляторные и иные функции, влияя на пластичность, процессы роста и ветвления нейронов и глиальных клеток и на локальный кровоток.
В головном мозге его вырабатывают нейроны, макро- и микроглия и основным местом действия являются синапсы, в первую очередь гиппокампа и миндалины. ТАП взаимодействует с рецепторами к липопротеинам низкой плотности [33], к эпидермальному фактору роста [35], к фактору роста из тромбоцитов (PDGF) [37], тем самым участвуя в миграции клеток, ремоделировании тканей.
Взаимодействие ТАП с NMDA-рецепторами, в частности с субъединицой N1, влияет на пластичность, в том числе на долгосрочное потенцирование и, следовательно, память, пространственную ориентацию и эмоциональное восприятие [38]. ТАП повышает проницаемость ГЭБ, усиливает экспрессию Е- и Р-селектинов и ICAM-1 с последующей миграцией лейкоцитов и воспалением в этой области [44, 45].
При повреждении аксонов он способствует их регенерации посредством протеолиза отложений фибрина [46]. С возрастом протеолитическая активность ТАП снижается, уменьшается его содержание в различных областях головного мозга, что может способствовать ухудшению пространственной ориентации, снижению памяти и другим расстройствам [47].
Возрастающее внимание в последние годы уделяется участию ТАП в регуляции локального кровотока с обеспечением физиологической адаптации кровотока под функциональное состояние и потребности определенных областей головного мозга [48].
По данным ряда экспериментальных исследований, высокие концентрации экзогенного ТАП, которые, в частности, отмечаются при ТЛТ, могут способствовать активации NMDA-рецепторов и эксайтотоксическому повреждению нейронов [49]. Эти данные подтверждаются тем, что блокирование моноклональными антителами взаимодействия ТАП с NMDA-рецепторами уменьшает объем ишемического повреждения и продлевает терапевтическое окно [50].
Впервые клиническая эффективность рекомбинантного ТАП — альтеплазы — была показана при ОИМ [51]. В 1993 г. T. Yamaguchi и соавт. [52] продемонстрировали его эффективность в первые 6 ч ИИ полушарной локализации. В 1995 г.
были опубликованы результаты многоцентровых исследований альтеплазы при ИИ в США и в Европе [11, 12].
К настоящему времени эффективность системного введения альтеплазы в первые 4,5 ч ИИ в дозах 0,6—0,9 мг/кг подтверждена международными клиническими исследованиями и отражена в национальных рекомендациях [53, 54].
Результаты метаанализа многоцентровых рандомизированных исследований показывают, что назначение ТАП в первые 6 ч, и особенно в первые 3 ч, ИИ достоверно уменьшает число больных с неудовлетворительным функциональным восстановлением или с летальным исходом [2].
Несмотря на высокую тромболитическую активность и эффективность в восстановлении кровотока и улучшении функционального исхода, необходимость длительного капельного внутривенного введения, особенно в условиях ограниченного времени [55], а также возможность нейротоксического эффекта обусловливают интерес к разработке новых тромболитических препаратов на основе ТАП (см. табл. 2).
Тенектеплаза относится к тромболитикам III поколения и является модифицированным вариантом ТАП, в котором с целью увеличения времени полувыведения, возможности болюсного введения, повышения сродства к фибрину и большей устойчивости к ингибитору ТАП 1-го типа в трех областях молекулы сделаны аминокислотные замены1.
К настоящему времени по результатам клинических исследований Управление по санитарному надзору за качеством пищевых продуктов и медикаментов Министерства здравоохранения и социальных служб США (англ.
: Food and Drug Administration — FDA) разрешило применение тенектеплазы при ОИМ (см. табл. 2) [56]. При И.И. наиболее крупное исследование тенектеплазы в сравнении с альтеплазой в первые 4,5 ч ИИ было завершено в 2016 г.
(табл. 4)
Таблица 4. Сравнительный анализ тенектеплазы и альтеплазы в первые 4,5 ч ИИ Примечание. * — достоверно чаще в группе пациентов, получающих терапию тенектеплазой, чем в группе альтеплазы (р=0,040; ОШ=3,16, 95% ДИ 1,04—9,75); # — достоверно чаще в группе тенектеплазы, чем в группе альтеплазы (р=0,038; ОШ=1,28, 95% ДИ 1,01—1,61. ВМ — внутримозговая. [57]. Его данные показали, что при нетяжелом ИИ тенектеплаза в дозе 0,4 мг/кг не уступает по эффективности и безопасности альтеплазе. Аналогичные результаты (см. табл. 4) были получены при назначении тенектеплазы, больным с более тяжелым инсультом [58]. Кроме того, в группе пациентов, получающих тенектеплазу, достоверно более часто отмечалось восстановление функциональной активности до 0—1 балла по модифицированной шкале Рэнкина (англ.: Modified Rankin scalе — mRS) [58]. Изучение эффективности различных доз тенектеплазы при ИИ средней тяжести показало, что наиболее эффективной является доза 0,25 мг/кг (табл. 4) [59]. В этом же исследовании было установлено, что назначение тенектеплазы сопровождалось лучшей динамикой по шкале инсульта Национального института здоровья (National Institutes of Health Stroke Scale — NIHSS) в первые сутки заболевания. В метаанализе [60] двух исследований более частая реканализация артерии и лучшая динамика по шкале NIHSS в первые 24 ч, а также исход к 90-м суткам по mRS достоверно чаще наблюдались в группе с тенектеплазой (76 больных, 0,25 мг/кг) по сравнению с альтеплазой (71 больной). По данным B. Campbell и соавт. [61], применение тенектеплазы приводило к лучшему восстановлению перфузии по сравнению с альтеплазой. В то же время объединенный анализ нескольких исследований [62], в которых оценивалось восстановление КТ-перфузии, не выявил достоверных различий между группами с тенектеплазой (36 больных) и альтеплазой (37 больных).
Ретеплаза также относится к тромболитическим препаратам III поколения и является укороченным вариантом ТАП, в котором удалены домены F, G и K1 (см. табл. 2). Это увеличивает время полувыведения и позволяет болюсное введение, но одновременно уменьшает сродство к фибриногену и фибринолитическую активность препарата. После окончания в 1995—1997 гг.
сравнительных исследований с альтеплазой [63, 64] и стрептокиназой [65] препарат был разрешен FDA для лечения ОИМ. При И.И.
выполнено одно сравнительное исследование [66], в котором была показана не меньшая эффективность ретеплазы по сравнению с альтеплазой в уменьшении неврологических симптомов по шкалам NIHSS, mRS и индексу Бартел к 30-м суткам у больных с инсультом средней тяжести (по NIHSS 13,7±6,2 балла).
Другой группой препаратов, применяемых для ТЛТ при ОИМ и ИИ, являются внешние активаторы плазминогена.
Внешние активаторы плазминогена не являются структурной частью человеческого организма, изначально имеют узкую направленность действия (лизис или препятствие свертыванию крови) и поэтому практически не участвуют в сигнальных, регуляторных и иных реакциях в организме человека.
В то же время, будучи чужеродными белками, они иммуногенны, и преодоление иммуногенности при одновременном сохранении фибринолитической активности является одной из основных задач при внедрении их в клиническую практику.
Фибринолитический эффект установлен у ряда растений, микроорганизмов и других представителей животного и растительного мира [67], однако в клинической практике применяются лишь единичные из них, в частности стрептокиназа, стафилокиназа и десмотеплаза.
Первыми гемолитический эффект стрептококка отметили W. Tillett и R. Garner [68] в 1933 г. В последующем был выделен наиболее гемолитически активный штамм — H46A [69]. Клонирование гена [70] позволило создавать рекомбинантные варианты стрептокиназы.
Стрептокиназа активирует плазминоген посредством образования комплекса стрептокиназа—плазминоген, что сопровождается конформационным изменением последнего и его активацией [71].
Стрептокиназа — один из первых препаратов, который начал применяться для ТЛТ при ОИМ и тромбоэмболии легочной артерии (ТЭЛА) [3, 72, 73] и показал высокую эффективность в восстановлении кровотока.
Одновременно наряду с хорошим тромболитическим эффектом было отмечено выраженное системное влияние на гемостаз. При И.И. выполнено три многоцентровых исследования [74—76].
В каждом из них, включая метаанализ [77], было показано, что назначение стрептокиназы в дозе 1,5 млн ЕД, несмотря на тенденцию к улучшению функционального исхода по индексу Бартел и шкале mRS к 180-м суткам, достоверно увеличивало частоту неблагоприятного исхода на 10-е и 90-е сутки и частоту внутричерепных кровоизлияний, в том числе с летальным исходом (табл. 5).
Таблица 5. Метаанализ применения стрептокиназы при ИИ [78] Примечания. * — достоверно чаще, чем в группе сравнения (р