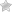Синдром Айкарди-Гутьереса (вариант написания Айкарди-Гутиера) (AGS) — представляет собой прогрессирующую энцефалопатию с дебютом в раннем детском возрасте, сопровождающуюся кальцификацией базальных ганглиев, лейкодистрофией, хроническим лимфоцитозом спинномозговой жидкости (СПЖ) и повышением уровня альфа интерферона ликвора и отрицательными результатами серологического исследования на типичные внутриутробные инфекции.
Синдром Айкарди-Гутьерес имеет аутосомно-рецессивный тип наследования, списана частичная пенетрантность у гетерозигот, и является генетически гетерогенным заболеванием, оно может быть вызвано мутациями в шести генах, соответственно, различают шесть генетических типов синдрома (Таблица 1).
AGS1 связан с мутациями в гене TREX1, расположенном на хромосоме 3p21. Ген TREX1 кодирует 3'>5' экзонуклеазу, участвующую в процессе репарации ДНК.
- AGS2 обусловлен мутациями в гене RNASEH2B на хромосоме 13q14, кодирующем субъединицу B рибонуклеазы H2.
- AGS3 вызван мутациями в гене RNASEH2C на хромосоме 11q13, кодирующем субъединицу C рибонуклеазы H2.
- AGS4 — мутациями в гене RNASEH2A на хромосоме 19q13, кодирующем субъединицу A рибонуклеазы H2.
AGS5 — мутациями в гене SAMHD1 на хромосоме 20q11.2, кодирующем Sam-домен и HD-домен белка, функционирующего как дезоксинуклеозид-трифосфат-трифосфогидролаза.
AGS6 – мутациями в гене ADAR на хромосоме 1q21.3, кодирующем фермент, катализирующий гидролитическую деаминацию аденозина в инозин в двунитевой РНК.
В настоящее время к синдрому Айкарди – Гутьереса отнесены ранее обособленные нозологические формы – энцефалит Кри и синдром псевдо-TORCH (синдром Берейтсера – Реардона).
Таблица1. Генетическая этиология синдрома Айкарди – Гутьереса.
| Тип | Локус | Ген | AGS (%) |
| AGS1 | 3p21.3-p21.2 | TREX1 | >25 |
| AGS2 | 13q14-q21 | RNASEH2B | 40 |
| AGS3 | 11q13.2 | RNASEH2C | 15 |
| AGS4 | 19p13.1 | RNASEH2A | 5 |
| AGS5 | 20q11.2 | SAMHD1 | 5 |
| AGS6 | 1q21.3 | ADAR | 10 |
Наиболее частые у европейцев мутации, вызывающие синдром Айкарди-Гутьерес, расположены во втором экзоне гена TREX1 (с.341G>A p.Arg114His) и зарегестрированы в 12,5% всех случаев AGS, в седьмом экзоне гена RNASEH2B (с.529G>A p.Ala177Thr) – 25% всех случаев AGS, и во втором экзоне гена ADAR (с.577C>G p.Pro193Ala) – 5% всех случаев AGS.
В Центре Молекулярной Генетики проводится поиск наиболее частых в европейской популяции мутаций в генах TREX1 (экзон2), RNASEH2B (экзон 7) и ADAR (экзон 2) методом прямого автоматического секвенирования.
| Поиск частых мутаций в генах TREX1, RNASEH2B, ADAR | 9 100 | 21 |
| Пренатальная ДНК-диагностика | 15 000 | 14 |
Синдром Айкарди :: Симптомы, причины, лечение и шифр по МКБ-10
Синдром Айкарди ( Aicardi syndrom) -это редкое генетическое заболевание, характеризующееся агенезией мозолистого тела, эпилептическими приступами по типу инфантильных спазмов с ранним дебютом, специфическими лакунарными изменениями на глазном дне, типичными изменениями на ЭЭГ (паттерн «расщепленного мозга»), задержкой психомоторного развития , а также лицевым дизморфизмом.
Известно приблизительно о 500 случаях синдрома Айкарди во всем мире, особенно большое количество в Японии. Синдром встречается у детей с различной расовой принадлежностью. По недавно проведенным в Швеции исследованиям распространенность синдрома Айкарди составляет от 2 до 15 случаев на 100000 девочек.( В России аналогичные исследования к сожалению не проводились). Однако, учитывая фенотипическое разнообразие и диагностические трудности, многие случаи заболевания остаются недиагностированными. Это позволяет пересмотреть данные об истинной распространенности синдрома Айкарди в сторону увеличения, возможно, синдром Айкарди является более частой причиной задержки умственного развития и инфантильных спазмов у девочек, чем считается в настоящее время. На сегодняшний день считается, что заболеваемость синдромом Айкарди среди всех детей с инфантильными спазмами составляет всего около 2-4%. Тип наследования синдрома Айкарди- доминантный сцепленный с Х-хромосомой, с предположительным локусом Хр22.3. Болеют только девочки. Трое мальчиков, которым был поставлен диагноз – синдром Айкарди имели генотип ХХY (47 хромосом)- синдром Кляйнфельтера. Для плода мужского пола с генотипом ХY синдром Айкарди является смертельным. За исключением одной пары сестер все описанные случаи являются спорадическими. Все случаи синдрома Айкарди, вероятно, связаны с новыми мутациями, так как ни одного случая передачи от матери к дочери гена, сцепленного с Х-хромосомой, отвечающего за развитие синдрома Айкарди, не зарегистрировано. Риск рождения в одной семье второго ребенка с синдромом Айкарди- менее 1%. Теоретически, риск передачи мутантного аллеля от женщины с синдромом Айкарди- 50%, однако плод мужского пола, носитель мутантного гена является нежизнеспособным. Таким образом, среди ожидаемого потомства 33%- здоровые девочки, 33%- здоровые мальчики и 33% — девочки с синдромом Айкарди.
Он и его семья пережили ужасный 1811-й голодный год в Мадриде, и эта жестокая проверка на выносливость стала для его жены Хосефы слишком тяжёлой. В июне 1812 года, она умерла, и 66-летний глухой старик остался один в своём доме.
Патогенез синдрома Айкарди в настоящее время неизвестен, связан с генетически детерминированными нарушениями этапа нейрональной миграции.
Дети, как правило, рождаются внешне здоровыми, с нормальным гестационным возрастом при рождении, без осложнений в пренатальном и интронатальном периоде, и развиваются по возрасту приблизительно до 2-5 (чаще 3) месяцев, когда чаще всего дебютируют инфантильные спазмы. Инфантильные спазмы — это тип эпилептических приступов, представляющих собой массивные миоклонические и(или) тонические, про- и(или) ретропульсивные, симметричные и(или) асимметричные, серийные и(или) изолированные спазмы аксиальной и конечностной мускулатуры. В 97% случаев при синдроме Айкарди наблюдаются флексорные инфантильные спазмы, которые могут быть атипичными, латерализованными. У 42% больных с синдромом Айкарди имеется сочетание инфантильных спазмов с другими видами эпилептических приступов, чаще с парциальными, реже с генерализованными тонико-клоническими. Итак, манифестными симптомами являются инфантильные спазмы либо реже парциальные приступы, дебют эпилептических приступов в 68% наблюдений приходится на первые три месяца жизни, в 23% случаев синдром дебютирует неонатальными судорогами в первый месяц жизни. Судорожные пароксизмы резистентны к проводимой противосудорожной терапии. Большая часть девочек с синдромом Айкарди имеет резкую задержку психомоторного развития. Но описаны случаи незначительного снижения интеллекта и умеренной задержки развития. В неврологическом статусе часто отмечается –микроцефалия, мышечная гипотония, возможна односторонняя мышечная гипертония и спастичность, оживленные глубокие сухожильные рефлексы или геми- или тетрапарез. Агенезия мозолистого тела при синдроме Айкарди обычно тотальная, часто сочетается с гетеротопией коркового вещества мозга, атрофией коры, структурной асимметрией полушарий мозга, нормотензивной гидроцефалией, полимикрогирией или пахигирией, хориоидальными кистами и папилломами, вентрикуломегалией, внутримозговыми кистами, синдромом Денди-Уокера. Предполагается, что наличие комплекса аномалий нейрональной миграции даже более специфично для синдрома Айкарди, чем изолированная агенезия мозолистого тела. Аномалии органа зрения: при синдроме Айкарди описано большое разнообразие аномалии развития глаз. Патогмоничным для данного синдрома является пигментный ретинит, проявляющийся различной степенью снижения остроты зрения (чаще довольно выраженной). Другие описанные аномалии глаз включают микрофтальмию, атрофию зрительного нерва, колобому, катаракту, которые могут быть одно- или двусторонними, или асимметричными. Скелетные аномалии: отмечаются такие врожденные дефекты, как полупозвонки и отсутствующе ребра, иногда приводящие к выраженному сколиозу у трети пациентов. Челюстно-лицевые аномалии: на сегодняшний день нет описания характерных лицевых симптомов при синдроме Айкарди, но наиболее часто встречающиеся, по данным авторов, наблюдавших 40 девочек с синдромом Айкарди, являются выступающие резцы, вздернутый кончик носа, уменьшенный угол носовой перегородки, редкие латерально расположенные брови ( признаки, проявившиеся у половины пациенток). Аномалии строения лица, описанные ранее в изолированных случаях, включают лицевую асимметрию, аномалии строения ушных раковин и уплощенную носовую перегородку, гипертелоризм, птоз, гипоплазию носа и микрогнатию, расщелину верхней губы и неба. Авторы также описали различные кожные поражения (включающее невусы, кожные дивертикулы, гемангиомы, ангиосаркомы) – у 20% пациенток. Пороки развития конечностей ( у 7,5%), включали каптодактилию, проксимальное расположение большого пальца, гипоплазию мизинцев, асимметрию конечностей, единственную поперечную ладонную складку, неполное удвоение большого пальца синдактилию 2 и 3 пальцев стоп. Желудочно-кишечный тракт: гастроезофагальный рефлюкс, запоры, диарея и трудности с кормлением. У пациентов с синдромом Айкарди увеличена частота случаев опухолей. Чаще всего это папиллома сосудистых сплетений, так же описаны гемангиома, ангиосаркома, гепатобластома, полипоз кишечника, эмбриональные карциномы. Рост. Темп роста замедляется в возрасте 7-10 лет и соответствует 5 центилю и ниже, увеличение веса также замедляется к этому возрасту до 25 центиля и ниже.
Эндокринная система. Возможно раннее наступление половой зрелости или задержка полового развития.
До настоящего времени не существует специального лабораторного диагностического теста или исследования, которое бы позволило поставить диагноз синдрома Айкарди. Для этого необходимо: неврологический осмотр, офтальмоскопия, ЭЭГ, МРТ с контрастом и/или без, рентгенограмма скелета. На МРТ можно обнаружить агенезию мозолистого тела, асимметрию полушарий коры, гетеротопию коркового вещества, внутримозговые кисты, папиллому сосудистых сплетений Аксоны коры, которые в норме должны перекрещиваться, при его агенезии не формируются и соответственно не идентифицируются при нейровизуализации. Агенезия мозолистого тела позволяет боковым желудочкам распространиться вверх, во фронтальное и париетальное белое вещество. Это состояние именуется верхней транслокацией боковых желудочков в лобно-теменные регионы мозга. Аналогичное смещение вверх претерпевает и III желудочек , что является одним из нейрорадиологических маркеров агенезии мозолистого тела. Увеличенный III желудочек, выдвигаясь вперед и вверх, раздвигает передние рога боковых желудочков, при сопутствующей гидроцефалии объем желудочков увеличивается, задние рога расширяются и изгибаются по направлению к средней линии (форма «ухвата»). Вероятно отсутствие поддерживающей функции мозолистого тела является основой для типичной черты агенезии мозолистого тела — расширения полушарий, III желудочка и Монроева отверстия. Типичные изменения на ЭЭГ в виде гипсаритмии, характерные для инфантильных спазмов встречаются далеко не у всех больных. Наиболее характерные изменения приступной ЭЭГ заключаются во вспышках нерегулярных быстрых и медленных волн продолжительностью от 3 до 6 секунд, которые перемежаются некоторым уплощением основного ритма в течение 5-20 секунд, причем изменения не синхронизированы по полушариям. На ЭЭГ – феномен «расщепленного мозга» ( Split-brain ). Так как практически у половины (42%) пациентов инфантильные спазмы сочетаются с другими видами эпилептических приступов, то данные ЭЭГ могут быть противоречивы. При офтальмоскопии обнаруживаются белого, или желто-белого цвета, хорошо отграниченные, круглые депигментированные участки. Пренатальная диагностика:
Пренатальное молекулярно-генетическое исследование (ДНК диагностика) –пока что невозможно , так как ген точно не выявлен. Тем не менее, даже без ДНК-анализа при синдроме Айкарди возможна пренатальная диагностика с помощью ультразвукового исследования.
Применяя методику ультразвукового сканирования плода во внутриутробном периоде на ранних сроках гестационного развития можно выявить агенезию мозолистого тела. Так же можно выявить некоторые другие аномалии, такие как внутримозговые кисты.
Таким образом, ультразвуковой и , возможно, другие активно разрабатываемые в последние годы методы нейровизуализации (такие как МРТ плода) могут позволить заподозрить синдром Айкарди еще в пренатальном периоде.
Лечение синдрома Айкарди не разработано в настоящее время. Применяется симптоматическое лечение. Основная стратегия терапии- купирование инфантильных спазмов, которые зачастую резистентны к АЭП, лечение их сложное и эффективность его невелика. Применяют различные медикаменты в максимально высоких дозах. Стартовая терапия начинается с вигабатрина (сабрил) – 50-100мг/кг/сут и вальпроатов (депакин-сироп)- 50-100мг/кг/сут. При частых приступах назначают комбинации АЭП с бензодиазепинами (клоназепам) -0,25-2мг/сут, или фенобарбиталом(5-15мг/кг/сут), а так же может быть введен суксилеп 15-30мг/кг/сут. Альтернативным методом является применение кортикостероидных гормонов (АКТГГ, синактен-депо в/м, дексаметазом,преднизолон –per os) и Ig (октагам). Средняя дозировка преднизолона 1-2,5мг/кг/сут с последующим переходом на минимальную поддерживающую дозу. Гормоны назначают в сочетании с базовыми АЭП. В качестве паллиативного хирургического лечения возможно использование стимуляции блуждающего нерва. Так как костно-мышечные дефекты могут приводить к сколиозу, для его предотвращения используется физиотерапия, лечебная физкультура, возможна хирургическая коррекция.
Семьям детей с синдромом Айкарди предоставляется возможность больше узнать о синдроме, о новых научных открытиях, познакомиться с другими семьями, обменяться идеями и опытом и получить полезные советы от родителей и специалистов. Так же на сайте регулярно размещается информация о благотворителях конференциях и концертах, которые организует и финансирует Фонд Айкарди.
Прогноз при синдроме Айкарди,как правило, серьезен в связи с выраженной умственной отсталостью и резистентным характером судорог. Часть детей (до 25%) погибает в первые годы жизни. Из выживших детей только 25% самостоятельно ходят и только 50% имеют навыки самообслуживания.
Продолжительность жизни очень вариабельна, в зависимости от степени выраженности симптомов. Средняя продолжительность жизни по разным данным составляет от 8,3 до 18,5 лет. Но имеются сведения о женщине 32 лет с синдромом Айкарди, а так же 49 лет с умеренной формой синдрома.
42a96bb5c8a2acfb07fc866444b97bf1 Модератор контента: Васин А.С.
Синдром Айкарди — генетический порок с тяжелыми неврологическими нарушениями
Синдром Айкарди является редким цереброретинальным генетическим расстройством. При данном заболевании мозг, частично или полностью, лишен одной из основных составляющих – мозолистого тела. Это является следствием дефекта Х-хромосомы. В сетчатке происходят изменения, ведущие к инфантильным спазмам.
- Мозолистое тело – центральный отдел нервной системы, представленный нервными окончаниями, соединяющими полушария головного мозга.
- Сидром Айкарди не является отдельной формой эпилепсии, а является самостоятельным заболеванием, которое в 1965 году было описано невропатологом из Франции Жаном Экарди.
- Синдром Айкарди-Гутьереса является угрозой для мальчиков с хромосомным набором ХХY или с синдромом Клайнфельтера.
По данным статистики, на сегодняшний момент наблюдалось около 500 случаев этого заболевания. Наибольшее распространение оно получило в Японии.
Однако, национальности и расы не играют ключевой роли. Все зависит от уровня медицины в регионе. Недостаток знаний ведет к не выявленным случаям. Из 2 – 4% детей, у которых проявляются инфантильные спазмы, обнаруживается болезнь Экарди.
Наследование
Синдром Айкарди-Гутьереса является наследственным (аутосомно-рецессивным) состоянием, что означает, что болезнь передается генетически. Автосомальное рецессивное состояние возникает, когда обе копии гена или кластера генов являются дефектными.
https://www.youtube.com/watch?v=IGrtbgymCEA
Если плод наследует дефектные копии от обоих родителей, то возникает заболевание. В качестве альтернативы, плод может наследовать один дефектный ген от одного родителя, а оставшаяся нормальная копия повреждается из-за экологических причин, таких как вирусная инфекция или воздействие повреждающих ДНК агентов.
- Рецессивное состояние указывает на то, что заболевание возникает только в случае дефектов обеих копий гена.
- При доминирующей форме наследования только одна дефектная копия может вызвать проблему.
- Автосомальное заболевание указывает, что состояние передается от одного поколения к другому через одну из 23 хромосом (аутосомы), а не половых хромосом (X или Y).
Синдром Айкарди наблюдается у младенцев в течение 4 месяцев после рождения и приводит к физической, умственной отсталости. Влияет на мозг, кожу, иммунную систему организма. Иммунный ответ подобен реакции организма на вирусную инфекцию, известен как «имитация врожденной инфекции».
При рождении типичными характеристиками являются неврологические аномалии, повышенный уровень белков печени в крови, увеличение печени, селезенки (гепатоспленомегалия), снижение уровня тромбоцитов крови (тромбоцитопения).
Существует два типа синдрома Айкарди, основанных на стадии возникновения. Ранняя стадия заболевания наблюдается у новорожденных, младенцев. Поздняя стадия заболевания наблюдается у детей старшего возраста (от 1 до 2 лет) с меньшим повреждением головного мозга.
Клиника
Как же выглядят дети, имеющие синдром Айкарди? Симптомы вначале достаточно неспецифичны, потому что дети рождаются в срок, через естественные родовые пути и выглядят здоровыми. До трех месяцев новорожденные развиваются без клинических проявлений, затем появляются эпилептические приступы.
Они представлены в виде ретропульсивных симметричных серийных клонико-тонических судорог конечностей. В подавляющем большинстве случаев к этому еще присоединяются инфантильные спазмы мышц-сгибателей. В редких случаях дебют заболевания встречается в первый месяц жизни.
Эпилептические припадки не купируются медикаментозно.
В неврологическом статусе у таких детей наблюдается уменьшение размеров черепа, снижение тонуса мышц, но при этом одностороннее расторможение рефлексов или, наоборот, парезы и параличи. Кроме того, у половины пациентов отмечаются аномалии развития скелета: агенезия позвонков или отсутствие ребер. Это приводит к выраженным сколиотическим изменениям осанки.
Причины
Как упоминалось ранее, Синдром Айкарди является генетическим состоянием, которое наследуется аутосомно-рецессивным способом. В очень редких случаях синдром является преимущественно унаследованным. Мутация может возникать внезапно или спорадически.
Точный ген, который его вызывает, не совсем понятен. Гены, которые показывают мутации при этом расстройстве: SAMHD1, RNaseH2A, RNaseH2B, RNaseH2C, TREX1.
Ген SAMHD1 генерирует белок, который участвует при иммунном ответе. Дефекты приводят к иммунному отказу.
TREX1 расположен на хромосоме 3, называется AGS1. TREX1 кодирует белок DNase III, который режет одноцепочечную ДНК. RNaseH2A, RNaseH2B, RNaseH2C, кодируют ферменты, которые образуют белковый комплекс под названием RNAse2H, разрушают РНК. TREX1, RNaseH2A, RNaseH2B, RNaseH2C представляют собой гены, которые кодируют ферменты, называемые нуклеазами.
Узнать больше Амнестические синдромы: виды, диагностика, методы лечения
Они участвуют в разрушении ДНК и РНК. Когда есть дефекты в нуклеазах, существуют избыточные молекулы ДНК и РНК, заставляющие организм думать, что в нем присутствуют вирусные частицы. Это вызывает иммунную реакцию (защиту организма) против себя.
Последствиями реакции являются поражения, наблюдаемые на коже, дефекты головного мозга (энцефалопатия). Мутации ADAR6 также являются причиной расстройства.
Мутации RNaseH2C (AGS3) на хромосоме 11 наблюдаются в 40% случаев синдрома Айкарди-Гутьера. RNaseH2B (AGS2) на хромосоме 13 наблюдаются в 14%, RNaseH2A на хромосоме 19 (AGS4) – 4% случаев. Мутации TREX1 – 25% случаев.
TREX1, RNaseH2A, RNaseH2B способствуют развитию раннего синдрома Айкарди. RNaseH2B способствует позднему.
Существуют другие генетические нарушения, которые возникают из-за мутаций. Генетические расстройства, связанные с мутациями приведены ниже.
Генетическое расстройство, вызванное мутацией ADAR:
- Dyschromatosis symbolrica hereditaria 1 (DSH).
Генетические расстройства, вызванные TREX1:
- Семейная желчная волчанка;
- Критический энцефалит;
- Системная красная волчанка (СКВ);
- Аутосомно-доминантная вагиналопатия сетчатки с церебральной лейкодистрофией (RVCL).
Симптомы
При раннем начале синдрома Айкарди-Гутьерса симптомы появляются примерно через 4 месяца после рождения. Беременность нормальная, ребенок не проявляет никаких симптомов при рождении. Начальные признаки на этом этапе представлены ниже:
- Трудность кормления;
- Сильная раздражительность;
- Частые лихорадки без причины;
- Ошибочные режимы сна;
- Приступы или эпилепсия.
Существуют дефекты развития мозга, что приводит к замедлению роста головы, ухудшению тонких моторных навыков, вообще замедлению неврологического развития.
Эти симптомы описаны ниже:
- Реакция испуга даже на мягкие раздражители;
- Только частичное управление головкой;
- Аномалии движения глаз и детских рефлексов (например, сосание);
- Языковое общение также ухудшается.
Эти симптомы сохраняются в течение нескольких месяцев, затем стабилизируются или исчезают. Существует прекращение прогрессирования заболевания.
- В фазе позднего начала Синдрома Айкарди-Гутье, эти симптомы появляются только через 1 или 2 года после нормального физического развития и развития мозга.
- 20% случаев признаки появляются у новорожденных.
- В матке могут быть обнаружены типичные особенности увеличенной печени и селезенки, повышенные уровни ферментов печени в крови, аномальное образование головного мозга, снижение тромбоцитов крови (тромбоцитопения), анемия.
- Другие пострадавшие органы – кожа, печень, глаза, дефициты гормонов и иммунной системы.
- Поражения кожи, воспаление, рубцевание ткани (например, уши, пальцы ног, пальцы);
- Глаукома;
- Инсулинзависимый сахарный диабет;
- Дефицит антидиуретического гормона (гормональное мочеиспускание);
- малокровие;
- Антитела против иммунной системы (аутоантитела);
- Малая голова (микроцефалия);
- Непроизвольные мышечные сокращения, влияющие на осанку, движение.
Распространенность
С момента своего официального признания Айкарди синдром встретился неврологам около полутысячи раз. Большинство больных проживали в Японии и других странах Азии. По данным швейцарских исследователей, встречаемость болезни — 15 случаев на сто тысяч детей. К сожалению, статистика, скорее всего, дает заниженные цифры, так как большинство пациентов остается необследованными.
Заболевание развивается у девочек. И врачи предполагают, что именно оно является причиной большинства случаев задержки психофизиологического развития и инфантильных спазмов.
Диагностика
Синдром Айкарди-Гутьера можно диагностировать на основании клинических симптомов с использованием компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ), анализа генов.
Существуют определенные характерные особенности, которые могут быть использованы для конкретной диагностики людей с синдромом Айкарди-Гутье. Они заключаются в следующем:
- Увеличение концентрации неоптерина в спинномозговой жидкости (CSF);
- Больше кальцификации ганглиев в головном мозге;
- Увеличение концентрации интерферона-альфа (IFN-a);
- Церебральная атрофия;
- Интерферонная подпись;
- Изменения в белом веществе;
- Увеличение количества белых кровяных телец (лейкоцитоз).
КТ-сканирование помогает визуализировать кальцификацию головного мозга. Атрофия мозга, изменения в белом веществе, лейкоцитоз, другие изменения обнаруживаются с помощью МРТ.
Узнать больше Стадии адаптационного синдрома
Количественная ПЦР используется для обнаружения интерфероновой сигнатуры. Это очень надежный тест, поскольку может обнаруживать экспрессию интерфероно-стимулированных генов крови.
- Гены видны даже после того, как симптомы синдрома Айкарди-Гутьера сократились.
- Неоптериновые концентрации в CSF являются надежным источником для подтверждения диагноза.
- Индивидуальное тестирование для 6 основных генов, которые вызывают синдром Айкарди-Гутье, полезно для подтверждения диагноза.
Тестирование мультигенных панелей является более эффективным и надежным для подтверждения диагноза. Мультигенная панель анализирует все 6 генов одновременно.
Пренатальное тестирование включает взятие пробы крови (PUBS), предимплантационную генетическую диагностику, генетическое тестирование. Кровь тестируется у плода в третьем триместре.
При предимплантационной генетической диагностике семьи, у которых есть подозрение о наличии причинных генов синдрома Айкарди, используют генный тест для эмбриона.
Международный неврологический журнал 5 (75) 2020
Идиопатические генерализованные эпилепсии, официально признанные Международной противоэпилептической лигой
DOUGLAS R. NORDLI, JR., Children's Memorial Hospital, Northwestern University, Feinberg School of Medicine, Chicago, Illinois, USA
Резюме
В настоящее время Международная противоэпилептическая лига выделяет 8 эпилептических синдромов, которые соответствуют базовому определению идиопатических генерализованных эпилепсий: доброкачественная миоклоническая эпилепсия раннего детского возраста, генерализованная эпилепсия с фебрильными приступами плюс (находится в стадии разработки), эпилепсия с миоклоническими абсансами, эпилепсия с миоклонически-астатическими приступами, детская абсанс-эпилепсия, юношеская абсанс-эпилепсия, юношеская миоклоническая эпилепсия и эпилепсия с изолированными тонико-клоническими приступами. При наличии характерных клинических признаков каждый из перечисленных синдромов может быть легко диагностирован. В некоторых случаях такие признаки отсутствуют или появляются позже по мере прогрессирования заболевания, что затрудняет диагностику. Электроэнцефалография часто помогает в диагностике идиопатических генерализованных эпилепсий, но нужно помнить, что сам по себе этот метод не всегда позволяет провести дифференциальную диагностику между различными видами эпилепсии, имеющими сходную клиническую картину. То же самое касается и генетических тестов, хотя и предполагается, что дальнейшее изучение взаимоотношений «генотип — фенотип» расширит наши возможности в установлении точного диагноза. В настоящее время клинические признаки все еще остаются краеугольным камнем для точной диагностики вида эпилептического синдрома, а следовательно, и определения его исхода.
Впервые синдромы генерализованной эпилепсии были отделены от синдромов локальной эпилепсии в классификации Международной противоэпилептической лиги (МПЭЛ) 1989 г. [1].
Однако работа над классификацией продолжалась, и в настоящее время вместо дихотомического подхода вниманию специалистов предлагается многоосевой, в котором для категоризации эпилепсии используются семиология припадков, классификация припадков, вид эпилептического синдрома, этиология и степень имеющихся нарушений [2].
Некоторые из хорошо распознаваемых синдромов были сохранены в обновленной классификации МПЭЛ 2001 г.
, но их не подразделяют на фокальные и генерализованные эпилепсии (этот шаг следует расценивать как освобождающий от жесткой классификации маневр, особенно в отношении эпилепсий раннего детского возраста, где точно установить фокальную или генерализованную природу эпилепсии было не всегда возможно).
Если рассмотреть эпилептические синдромы, которые в настоящее время выделяет МПЭЛ и которые соответствуют определению идиопатической генерализованной эпилепсии, введенному еще в 1989 г.
, то можно выделить следующие их виды: доброкачественная миоклоническая эпилепсия раннего детского возраста, генерализованная эпилепсия с фебрильными приступами плюс (находится в стадии изучения), эпилепсия с миоклоническими абсансами, эпилепсия с миоклонически-астатическими приступами, детская абсанс-эпилепсия, юношеская абсанс-эпилепсия, юношеская миоклоническая эпилепсия и эпилепсия с изолированными тонико-клоническими приступами. Последние три рассматривают в качестве разновидностей идиопатических генерализованных эпилепсий с вариабельным фенотипом. Ниже будет представлен краткий обзор клинических признаков, данных электроэнцефалографии (ЭЭГ), генетических аспектов и прогноза для вышеперечисленных синдромов.
- Доброкачественная миоклоническая эпилепсия раннего детского возраста
Эта довольно редкая форма эпилепсии впервые была описана в 1981 г. Частота ее встречаемости даже в специализированных центрах не превышает 1 % [3, 4].
В частности, при анализе наших данных о 2874 пациентах такой диагноз был обнаружен только у 2 детей. Согласно данным литературы, этот синдром наблюдается в 2 раза чаще у мальчиков [5].
Кроме того, в 40 % случаев семейный анамнез отягощен случаями эпилепсии или фебрильных судорог [6].
Клинические проявления
До появления припадков развитие ребенка происходит нормально. Заболевание обычно манифестирует в возрастном интервале между 5 месяцами и 5 годами жизни. Вначале судороги выражены слабо, по мере прогрессирования заболевания они нарастают, однако редко имеет место падение больного во время приступа.
У младенцев и детей наблюдаются запрокидывание головы, отклонение глаз вверх либо непродолжительные судороги в руках. Приступы наблюдаются ежедневно, иногда их может быть несколько подряд.
Среди больных встречаются дети с миоклонусом, провоцируемым сенсорными стимулами, такими как укол или внезапный шум [7].
При доброкачественной миоклонической эпилепсии раннего детского возраста (ДМЭРДВ) в межприступном периоде на ЭЭГ обычно патологии не выявляется.
Лишь изредка удается обнаружить фокальные нарушения или генерализованные спайк-волны [8].
Во время миоклонических подергиваний наблюдаются быстрые генерализованные спайк- или полиспайк-волны, хорошо распознающиеся при полиграфических записях или при использовании видео-ЭЭГ [5].
Генетические аспекты
Хотя и предполагают, что наследственность вносит вклад в развитие ДМЭРДВ, убедительно это показано не было.
В одном из исследований, посвященных семейной миоклонической эпилепсии раннего детского возраста, которая в некоторой степени схожа с ДМЭРДВ, была обнаружена связь с аутосомно-рецессивными генами в 16р13.
Однако следует иметь в виду, что у 5 из 8 пациентов в данном исследовании наблюдали генерализованные тонико-клонические припадки, что не характерно для ДМЭРДВ.
Прогноз
Прогноз в отношении контроля приступов обычно благоприятный, хотя избежать остальных клинических проявлений удается не всегда. Тем не менее при достаточно долгом наблюдении пациентов лишь у незначительной части отмечаются слабо или умеренно выраженные когнитивные нарушения. У тех больных, у которых терапия сразу же дает положительную динамику, результаты лечения лучше [5].
Научная электронная библиотека Монографии, изданные в издательстве Российской Академии Естествознания
С клинической точки зрения Х-сцепленную умственную отсталость принято разделять на синдромальную (MRXS – mental retardation, X-linked, syndromic) и несиндромальную (неспецифическую, MRX – mental retardation, X-linked) [Kerr et al., 1991].
При синдромальных формах Х-сцепленной умственной отсталости помимо нарушений интеллекта обнаруживают различные аномалии при клиническом осмотре, лабораторных и функциональных исследованиях.
Больные могут иметь нарушения физического развития, пороки развития мозга и других органов, комплекс микроаномалий, неврологические симптомы, особенности поведения, метаболические нарушения. При несиндромальных формах эти признаки отсутствуют, и наблюдается изолированная умственная отсталость [Chiurazzi et al., 2004].
Деление на синдромальные и несиндромальные формы является общепринятым, обоснованным с клинических позиций, и при этом не является специфичным только для Х-сцепленной умственной отсталости, а используется в отношении всех, в том числе аутосомных форм.
Суммарный состав моногенных состояний, классифицируемых как Х-сцепленная умственная отсталость, включает более 200 нозологических единиц [Chiurazzi et al., 2008]. По данным Генетического центра Гринвуда [Greenwood Genetic Centre site, 2016] из 126 идентифицированных генов Х-сцепленной умственной отсталости 105 генов связаны с синдромальными её формами.
Поиск генетических причин несиндромальных форм XLMR связан со значительными трудностями, поскольку при MRX отсутствуют другие клинические критерии диагностики, кроме снижения IQ и Х-сцепленного характера родословной. К настоящему времени идентифицировано 50 генов MRX [Greenwood Genetic Centre site, 2016].
Сложности дифференциальной диагностики синдромальных и несиндромальных Х-сцепленных состояний с точки зрения этиологии связаны с тем, что в обеих группах заболеваний были обнаружены мутации в одних и тех же генах [Kleefstra, Hamel, 2005]. Одновременно с синдромальной и несиндромальной XLMR связаны 29 генов.
Например, мутации гена RSK2 встречаются как при синдроме Коффина – Лоури (синдромальная форма ХLMR), так и при неспецифической Х-сцепленной умственной отсталости. Мутации гена МEСР2 могут вызывать у лиц женского пола как классическую форму RTT, атипичные формы заболевания, так и несиндромальную умственную отсталость с различной степенью снижения интеллекта.
Возможно, что тип мутации, локализация её в различных доменах соответствующих белков либо генетическое окружение могут влиять на фенотип, приводя к синдромальной или несиндромальной формам заболевания.
- Поскольку синдромальная Х-сцепленная умственная отсталость характеризуется аномалиями различных органов и систем, рядом авторов предпринята её клиническая классификация. В частности, Chiurazzi с соавторами [2004] предложено деление синдромальной ХLMR на следующие классы:
- 1) синдромы мальформаций, характеризующиеся множественными врожденными аномалиями,
- 2) нервно-мышечные заболевания, в основном проявляющиеся неврологическими симптомами и патологией мышечной системы (атаксия, гиперкинезы, нарушения мышечного тонуса и др.),
- 3) метаболические болезни, возникающие вследствие дефицита определенных ферментов,
4) доминантные состояния, при которых заболевание наблюдается у девочек, а мальчики погибают внутриутробно [Chiurazzi et al., 2004].
Однако, начиная с 2008 г., от подобного деления было решено отказаться, поскольку в нем смешивались сразу несколько принципов классификации (особенности наследования, наличие мальформаций, метаболических расстройств и др.). Так, в каталоге Chiurazzi [2008] MRXS разделена лишь на 2 класса: синдромы с мальформациями и нервно-мышечные болезни, что, с нашей точки зрения, представляется
не совсем оправданным. Так, синдром RTT, согласно делению Chiurazzi, был отнесен к нервно-мышечным заболеваниям, под которыми авторы подразумевают синдромы, характеризующиеся умственной отсталостью и неврологическими симптомами (эпилепсией, спастической параплегией, атаксией и др.).
Однако данная классификация вступает в противоречие c общепринятым понятием «нервно-мышечные заболевания», подразумевающим группу болезней, связанных с нарушением функции произвольной мускулатуры вследствие поражения собственно мышц, нервно-мышечных соединений, периферических нервов или моторных нейронов спинного мозга [Гехт, 1982]. Следует отметить, что RTT проявляется, прежде всего, психическими, но не мышечными нарушениями, и поэтому согласно международной классификации болезней (МКБ-10) относится к разделу «Расстройства психологического развития» класса «Психические расстройства и расстройства поведения».
По нашему мнению, помимо обоснованного разделения на синдромальную и несиндромальную Х-сцепленную умственную отсталость, удобной является классификация, основанная на характере наследования заболевания.
Среди всех форм XLMR преобладают те, которые проявляются преимущественно у гемизигот по Х-сцепленным мутациям. В настоящее время выделено менее десятка так называемых доминантных состояний, проявляющихся преимущественно у гетерозигот.
Однако они заслуживают отдельного рассмотрения, так как в силу высоких частот ряда нозологических форм вносят значительный вклад в XLMR (табл. 2).
Таблица 2
Доминантные формы Х-сцепленной умственной отсталости
| Название заболевания | Номер по каталогу OMIM | Ген | Локализация гена | Фенотипические признаки |
| Гольтца синдром | 305600 | PORCN | Xp11.23 | Умственная отсталость, фокальная дермальная гипоплазия, короткие или отсутствующие пальцы, полисиндактилия, микрофтальмия |
| Айкарди синдром | 304050 | Не идентифицирован | Xp22 | Агенезия corpus callosum, умственная отсталость, хориоретинопатия, микрофтальмия, судороги |
| MIDAS синдром | 309801 | HCCS | Xp22.2 | Умственная отсталость, микрофтальмия, дермальная аплазия, склерокорнеа |
| Оро-фацио-дигитальный синдром | 311200 | OFD1/ CXORF5 | Xp22.2 | Умственная отсталость, срединные расщелины лица, узелки на языке, синдактилия |
| Эпилепсия, ограниченная женским полом, с умственной отсталостью | 300088 | PCDH19 | Xq21.3-q22.2 | Умственная отсталость и эпилепсия |
| Кранио-фацио-скелетный синдром | 300712 | Не идентифицирован | Xq26-q27 | Легкая умственная отсталость, микроцефалия, низкий рост, маленькие ушные раковины, утолщенный кончик носа, короткий фильтр, маленькие нижняя челюсть, кисти и стопы, избыточный арковидный рисунок на пальцах кистей при исследовании дерматоглифики |
| Синдром Ретта | 312750 | MECP2 | Xq28 | Деменция, аутизм, стереотипные движения рук, апраксия целенаправленных движений рук, нарушения ходьбы |
| Х-сцепленная перивентрикулярная гетеротопия | 300049 | FLNA | Xq28 | Умственная отсталость, эпилепсия, перивентрикулярная узелковая гетеротопия, легкая гипоплазия corpus callosum и мозжечка |
|
308300 | IKBKG (NEMO) | Xq28 | Умственная отсталость, поражение кожи, проходящее несколько стадий от эритематозно-везикулезных высыпаний до пигментных отложений и причудливой формы депигментации, аномалии зубов, сетчатки |
Объяснение существования Х-сцепленных заболеваний, проявляющихся преимущественно у девочек, было дано на основе выявления повышенной частоты спонтанных абортов в родословных некоторых семей с данной патологией и состоит в том, что пораженные плоды мужского пола погибают внутриутробно [Lenz, 1975].
Альтернативное объяснение было предложено Thomas [1996], который предположил, что Х-сцепленные доминантные состояния возникают как мутации de novo генов хромосомы Х в половых клеткак у мужчин, и, следовательно, передаются ими исключительно дочерям.
При большинстве Х-сцепленных доминантных состояний принято считать, что мальчики более тяжело поражены, и поэтому могут погибать до или вскоре после рождения, а мальчики с такой же тяжестью заболевания, как у девочек, имеют либо кариотип 47,XXY (синдром Клайнфельтера), либо мозаицизм по мутации соответствующего Х-сцпленного гена [Vorsanova et al., 2016].
Особый механизм наследования наблюдается при таком заболевании, как эпилепсия с умственной отсталостью, ограниченная женским полом.
Это состояние возникает вследствие мутаций Х-сцепленного гена протокадерина 19 (PCDH19), при этом мальчики имеют нормальный фенотип благодаря присутствию другого гена протокадерина PCDH11Y на хромосоме Y [Dibbens et al., 2008].
Другим примером Х-сцепленного заболевания, при котором мальчики с мутацией Х-сцепленного гена практически не имеют фенотипических признаков, а у девочек развиваются тяжёлые симптомы, является кранио-фронто-назальный синдром (OMIM 304110).
Данный синдром обусловлен мутациями гена эфрина B1 и протекает с тяжелым краниосиностозом у женщин и бессимптомно у мужчин. Предполагается, что развитие этого заболевания только у гетерозигот связано с взаимодействием (интерференцией) двух популяций клеток с активной нормальной и мутантной хромосомами Х [Depienne et al., 2009].
Таким образом, отказ от выделения заболеваний, проявляющихся преимущественно у гетерозигот («доминантные заболевания» по Chiurazzi), на наш взгляд, не целесообразен.
По-видимому, характер наследования, как принцип классификации Х-сцепленных форм умственной отсталости, будет пересмотрен и переоценен.
В целом, классификация XLMR продолжает обсуждаться и ещё неоднократно будет подвергнута критическому пересмотру.