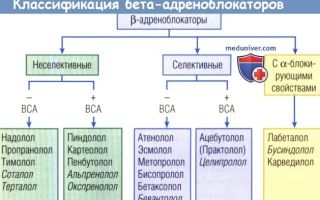
Открытие Алквистом в 1949 году адренорецепторов, воспринимающих симпатические влияния в различных органах, послужило основой создания нового класса медикаментов, позволяющих целенаправленно осуществлять стимулирующее (агонистическое) или тормозящее (антагонистическое) влияние на эти рецепторы. В дальнейшем оказалось, что адренорецепторы далеко не однородны, и они были подразделены на альфа- и бета-рецепторы.
Кроме того, в каждой из групп было выделено по две подгруппы — первая и вторая. Установлено, что стимуляция адренергических альфа-1-рецепторов вызывает вазоконстрикцию.
Следствием стимуляции альфа-2 адренергических рецепторов является торможение выделения норадреналина и вазодилатация.
Стимуляция бета-1-рецепторов имеет результатом учащение ритма сердца, повышение его работы, инотропизма, в то время как воздействие ни бета-2-рецепторы ведет к расширению бронхиол, вазодилатации.
Для лечения артериальной гипертонии применяется альфа-1-блокатор — празозин, который снижает тонус артериол, при этом не учащает ритм сердца и не повышает МО; центрального и прямого действия на почки не оказывает; не вызывает нарушений метаболизма. Вместе с тем его первая доза может вызвать резкую постуральную гипотензию. Монотерапия празозином часто недостаточно эффективна. Применяют его в сочетании с другими препаратами, в частности, с мочегонными.
К этой же группе препаратов относится алкалоид спорыньи — дигидроэргокристи, который обычно применяется в комплексных препаратах (кристепин). Альфа-1 -блокаторы могут вызывать синдром обкрадывания, так как сильно расширяют периферическую коронарную сеть. В связи с этим они не назначаются при значительных, особенно острых, коронарных нарушениях.
Альфа-2-агонистическая активность адренорецепторов при лечении артериальной гипертонии используется в препаратах, которые характеризуются преимущественно центральным действием (клонидин и допамин).
Наибольшее значение в терапии гипертензии имеют блокаторы бета-адренорецепторов или бета-блокаторы (ББ). По своей активности, стойкости эффекта они, несомненно, относятся к основным препаратам для лечения АГ.
Общим механизмом действия для всей группы ББ является тормозящее влияние на центральные отделы симпатической нервной системы с одновременным усилением действия парасимпатической системы.
На начальном этапе действие ББ приводит к урежению ЧСС, ослаблению сократительной функции сердца, падению МО. При этом несколько снижается продукция ренина.
Однако на периферические сосуды на этом этапе бета блокаторы могут оказывать сосудосуживающее действие, усиленное в связи с падением МО.
Если бы действие ББ ограничивалось влиянием на работу сердца, оставался бы необъяснимым более поздний (на 7—14 день) стойкий гипотензивный эффект, который при АГ может быть обусловлен только падением периферического сопротивления. Оказалось, что даже при нормализации МО гипотензивный эффект сохраняется.
Установлено, что снижение периферической вазоконстрикции обусловлено усилением влияния блуждающего нерва, повышением чувствительности барорецепторов к уровню АД, снижением продукции катехоламинов, уменьшением продукции ренина, а следовательно, и ангиотензина II.
Установлено, что важную роль в лечении артериальной гипертензии играет кардиопротективное влияние бета-блокаторов, тормозящее развитие гипертрофии миокарда. Более того, было установлено, что длительное применение ББ может в ранних стадиях АГ-привестн к обратному развитию гипертрофии миокарда и гладких мышц сосудов.
— Также рекомендуем «Классификация бета-адреноблокаторов. Эффективность бета-адреноблокаторов»
Оглавление темы «Лечение артериальной гипертензии»: 1. Рекомендации при артериальной гипертензии. Диета при артериальной гипертензии 2. Медикаментозная терапия гипертензии. Резерпин в лечении артериальной гипертензии 3. Клонидин в лечении артериальной гипертензии. Диуретики при лечении гипертонической болезни 4. Эффективность диуретиков при гипертензии. Калийсберегающие диуретики 5. Блокаторы каналов ионов кальция при гипертензии. Антагонисты кальция 6. Верапамил и дилтиазем в лечении гипертензии. Эффективность антагонистов кальция 7. Адреноблокаторы в лечении гипертензии. Эффективность блокаторов адренорецепторов 8. Классификация бета-адреноблокаторов. Эффективность бета-адреноблокаторов 9. Побочные эффекты бета-адреноблокаторов. Ингибиторы АПФ в лечении гипертензии 10. Токсичность иАПФ. Противопоказания к назначению ингибиторов АПФ
Почему при лечении доброкачественной гиперплазии простаты урологи назначают адреноблокаторы α1? * Клиника Диана в Санкт-Петербурге
Доброкачественная гиперплазия предстательной железы — очень распространенное заболевание у мужчин, приводящее к обструкции (сужению) мочевыводящих путей и появлению вследствие этого различных симптомов заболеваний нижних мочевыводящих путей.
Ранее считалось, что это заболевание пожилых мужчин, но сейчас гиперплазия все чаще встречается и у пациентов среднего возраста. Гиперплазия простаты есть примерно у 50% мужчин, перешедших рубеж за 60 лет. К 80 годам этот диагноз будет поставлен примерно 88% мужчин.
Как проявляется гиперплазия простаты
гиперплазия простаты
Симптомы со стороны нижних мочевыводящих путей сразу испытывают не все пациенты. Обычно недержание мочи возникает постепенно, по мере того как уретра под давлением предстательной железы сужается и удлиняется, что препятствует нормальному оттоку мочи из мочевого пузыря.
Мужчины замечают следующие признаки ухудшения здоровья:
- отток мочи ослабевает;
- становится труднее начать мочеиспускание;
- несколько раз приходится вставать ночью, чтобы помочиться.
У таких мужчин могут быть рецидивирующие инфекции мочевыводящих путей и развиться почечная недостаточность.
Иногда больные не обращают внимания на измененное мочеиспускание, а после простуды или употребления спиртных напитков попадают в лечебное учреждение из-за острой задержки мочи. Одновременно с остановкой мочеиспускания возникает сильная боль внизу живота. Облегчение пациенту приносит только опорожнение мочевого пузыря с помощью катетера.
Лечение пациентов с гиперплазией зависит от субъективных, например, раздражение и обструкция, и объективных, например, внутрипузырная обструкция, выявленная при уродинамическом исследовании, симптомов.
Симптомы раздражения включают остаточную мочу после мочеиспускания, принудительное мочеиспускание, дизурию. Замедленное начало мочеиспускания, снижение мочеиспускания, выделение жидкости после мочеиспускания — симптомы обструкции.
Для лечения патологии применяется несколько групп препаратов:
- Блокаторы α1 неселективные, например доксазозин, и уроселективные, например тамсулозин.
- Ингибиторы α-редуктазы (финастерид и дутастерид);
- экстракты растений, например, экстракты семян тыквы, корня крапивы.
Блокаторы α1 — во многих странах преобладающая группа препаратов для лечения симптомов со стороны нижних мочевыводящих путей. Например, в США более 90% лекарств, прописываемых для лечения симптомов гиперплазии, состоят из блокаторов α1
Принципы действия адреноблокаторов α1
Адренорецепторы α1 расположены в постсинаптических эффекторных клетках, особенно в гладких мышцах. Этих рецепторов много в простате, ее строме, капсуле, области шейки мочевого пузыря.
По мере прогрессирования доброкачественной гиперплазии предстательной железы строма, а также гладкие мышцы в ней увеличиваются. Адренорецепторы α1 поддерживают тонус гладких мышц, затрудняя мочеиспускание.
После блокировки α1-адренорецепторов, гладкие мышцы предстательной железы и шейки мочевого пузыря расслабляются, облегчая пациенту мочеиспускание.
Блокаторы α1-адренорецепторов действуют быстро, и положительные эффекты достигаются быстро. Но, выписывая такое лекарство, уролог должен учитывать и вероятные побочные эффекты.
Поскольку блокаторы α1-адренорецепторов влияют на все гладкие мышцы, включая кровеносные сосуды, могут возникнуть ортостатическая гипотензия, тахикардия, головная боль, головокружение, слабость, обмороки, тошнота и другие побочные реакции.
Недавние исследования выявили подтипы α1-адренорецепторов, присутствующие в организме человека. Оказывается, таких подтипов 3:
Эти подтипы рецепторов распределены в организме неравномерно. Неселективные блокаторы рецепторов α1 оказывают более неблагоприятное воздействие на сердечно-сосудистую систему, блокируя рецепторы подтипа α1B в кровеносных сосудах.
Адренорецепторы подтипа α1A играют самую важную роль в сокращении гладких мышц простаты, так как на них приходится 70% всех подтипов α1-адренорецепторов, присутствующих в простате.
Адренорецепторы подтипа α1A также преобладают в строме простаты.
Сравнительные исследования показали, что блокаторы рецепторов α1 имеют разное сродство к рецепторам α1A и α1B. Наиболее селективный в отношении терапевтически важных адренорецепторов подтипа α1A — тамсулозин. Рецепторы подтипа α1B отвечают за гладкие мышцы сосудов.
Сравнительная характеристика адреноблокаторов α1 — что показали исследования
что показали исследования
Исследование, проведенное в 1999 г. уч. Джаваном и Марбергером, охватило данные 6333 пациентов с гиперплазией простаты. Ученые оценивали эффективность и переносимость альфузозина, теразозина, доксазозина и тамсулозина . Оказалось, что все препараты были одинаково эффективны и значительно превосходили эффект плацебо: у больных облегчались симптомы нижних мочевыводящих путей и улучшалось качество мочи.
Различия между этими препаратами стали очевидны при изучении частоты побочных эффектов. Среди всех α1-адреноблокаторов наименьшее количество побочных эффектов дали альфузозин и тамсулозин — они лучше всего переносились пациентами.
В том же исследовании было показано, что тамсулозин гораздо меньше влияет на артериальное давление, сердечно-сосудистую систему и с меньшей вероятностью вызывает симптоматическую ортостатическую гипотензию, чем альфузозин, особенно у пожилых пациентов.
Также в 1999 г. уч. Na YJ и его коллеги сравнили безопасность, эффективность и частоту побочных эффектов теразозина и тамсулозина. В исследовании приняли участие 212 пациентов.
Теразозин и тамсулозин почти одинаково облегчили симптомы со стороны нижних мочевыводящих путей (39 и 45,1% соответственно), но в меньшем количестве случаев улучшили уродинамические параметры (25,8 и 37,5%).
Теразозин вызвал больше побочных эффектов, чем тамсулозин (50 и 13 соответственно), наиболее распространенными были головокружение и гипотония.
В 2000 г. уч. Tsujii продолжил тему, проведя исследование результатов терапии 121 пациента с гиперплазией. Специалист сравнил эффективность и безопасность празозина, теразозина и тамсулозина.
По его данным положительный эффект на симптомы со стороны нижних мочевыводящих путей составил 38 и 39 и 26%.
Улучшение уродинамических параметров было больше в группах празозина и тамсулозина, но празозин и теразозин снижали артериальное давление чаще и значительнее по сравнению с группой тамсулозина.
В 2006 г. состоялось новое исследование, посвященное этой теме. Уч. Рахарджо и его коллеги изучили данные 101 пациента с симптоматической гиперплазией предстательной железы, сравнив безопасность и эффективность доксазозина и тамсулозина.
Оказалось, что оба препарата хорошо уменьшают симптомы со стороны нижних мочевыводящих путей, но тамсулозин значительно улучшает уродинамические параметры, практически не влияя на систолическое, диастолическое артериальное давление и частоту сердечных сокращений, чего нельзя сказать о доксазозине.
Рекомендации европейских коллег по выбору адреноблокатора α1
Все α1-адреноблокаторы эффективны для устранения или облегчения симптомов нижних мочевыводящих путей и улучшения уродинамических параметров.
Но во многих исследованиях в Европе и во всем мире было показано, что тамсулозин имеет меньше побочных эффектов из-за его более высокого сродства к адренорецепторам подтипа α1A.
Он не оказывает негативное воздействие на сердечную систему (артериальное давление, частота сердечных сокращений). Поэтому в настоящее время тамсулозин наиболее интересен урологам.
Альфа-адреноблокаторы > Клиника профессора Азизова
Являются относительно новыми препаратами, недостаточно известными отечественным урологам, андрологам. Широкое применение, которых ограничено целым рядом побочных эффектов.
Применение a-адреноблокаторов при лечении расстройств мочеиспускания, связанных с доброкачественной гиперплазией (аденомой) простаты, сегодня стало делом привычным в консервативной терапии этих больных.
Расстройства мочеиспускания делятся на обструктивные (обусловленные сужением просветамочеиспускательного канала вследствие сдавливания аденоматозным узлом, самой увеличенной простатой) и ирратативные (обусловленные раздражением рецепторов).
Альфа-адреноблокаторы, блокируя альфа-аденорецепторы, снимают в первую очередь ирритативную симптоматику.
В пользу применения a-адреноблокаторов при хроническом простатите свидетельствует ряд известных факторов: высокое содержание a-адренорецепторов в области шейки мочевого пузыря, предстательной железы и уретры; сходство клинической картины аденомы простаты и простатита у некоторых пациентов; наличие различных расстройств мочеиспускания у значительного числа пациентов с хроническим простатитом. Некоторые формы хронического простатита связаны с первоначальным нарушением функции симпатической нервной системы и гиперреактивностью a-адренорецепторов. При этом достаточно часто повышается внутриуретральное давление, особенно в задней уретре, что может быть причиной возникновения уретропростатических рефлюксов (попадания мочи из уретры в предстательную железу), что, в свою очередь, по мнению некоторых исследователей, является одной из главных причин хронического простатита. Вследствие этого развивается воспалительный процесс, происходит выработка большого количества биологически активных веществ (медиаторов воспаления), которые, в свою очередь, вызывают боли, неприятные ощущения и различную симптоматику расстройств мочеиспускания. Так формируется порочный круг: повышение давления в задней уретре, заброс мочи в простату, воспаление, отёк, боль, нарушение мочеиспускания, а вследствие этого ещё большее повышение внутриуретрального давления. Применение a-адреноблокаторов разрывает этот круг.
Идеальным кандидатом для назначения α – адреноблокаторов является больной, у которого симптомы заболевания возникают или усиливаются вследствие увеличенного сопротивления мочеиспускательного канала, вызванного повышенным тонусом гладкомышечных элементов. Значительное число больных с существенными симптомами нарушения мочеиспускания и без признаков инфекционно – воспалительного процесса в нижних мочевыводящих путях соответствует этим критериям (DeLaKossettr,1992).
M. McNanghton-Collinsи соавт. (1999) провели анкетирование среди урологов и выявили, что 77% урологов США назначают a-адреноблокаторы в половине и более случаев хронического простатита.
Больным хроническим простатитом, у которых 2-недельный курс антибактериальной терапии оказался неэффективным, может быть начато пробное лечение α- адреноблокаторами в режиме, аналогичном таковому у больных с доброкачественной гиперплазией простаты (A. Dobl, D.
Taylor- Robinson, 1994). Рациональным подходом является титрование до максимальной эффективной /переносимой дозы, однако имеются указания на то, что для симптоматического улучшения у больных ХП в целом требуются меньшие дозы α -адреноблокаторов по сравнению с больными ДГП (G. A.
Barbalias, 1998).
S. G. Weiss и T. D. Moon (2000) считают оправданным и назначение α -адреноблокаторов на срок 1 месяц и в последующем переход на интермиттирующее или постоянное лечение в зависимости от конкретной клинической ситуации.
Наш опыт применения a-адреноблокаторов свидетельствует о возможности их применения в качестве составляющих комбинированного лечения совместно с антибактериальными, противовоспалительными средствами и физиотерапией.
При этом симптомы расстройства мочеиспускания купируются быстрее и результат терапии дизурических нарушений более устойчив, чем в отношении другой симптоматики.
При назначении a-адреноблокаторов для лечения различных расстройств мочеиспускания необходимо помнить, что достаточно быстро достигнутый результат от их применения может быть неустойчивым. Необходимо понимание этиологии и патогенеза происходящих процессов в каждом конкретном случае и назначение комбинированного лечения. Длительность приёма a-адреноблокаторов — 1-3 месяца и более:
Альфузозин, дальфаз, доксазозин, тамсулозин, индорамин, кардура, кетансерин, корнам, ницерголин, омник, празозин, теразозин, тонокардин, феноксибензамин, фентоламин.
Блокаторы a-адренергических рецепторов как антигипертензивные препараты
Блокаторы a-адренергических рецепторов представляют собой довольно большую группу лекарственных препаратов, которые с 60-х годов используются при лечении различных форм артериальной гипертензии.
Интерес к a-адреноблокаторам как антигипертензивным средствам заметно ослабел в 70-е и 80-е годы, когда для лечения гипертонической болезни стали широко применяться антагонисты кальция и ингибиторы АПФ.
В начале 90-х годов интерес к блокаторам a-адренорецепторов вновь усилился, поскольку было показано, что селективные блокаторы a-адренорецепторов длительного действия вполне сравнимы по антигипертензивной эффективности, переносимости и безопасности с тиазидными диуретиками, b-адреноблокаторами, антагонистами кальция и ингибиторами АПФ.
Кроме того, a1-адреноблокаторы, как оказалось, обладают рядом ценных дополнительных свойств, благодаря которым они особенно полезны при лечении артериальной гипертензии у больных с доброкачественной гиперплазией (аденомой) предстательной железы, атерогенной дислипидемией и сахарным диабетом.
Таким образом, несмотря на широкое применение тиазидных диуретиков, b-адреноблокаторов, антагонистов кальция, ингибиторов АПФ и блокаторов АТ1-ангиотензиновых рецепторов, селективные блокаторы a1-адренорецепторов по-прежнему являются антигипертензивными препаратами выбора в некоторых клинических ситуациях. По определенным показаниям продолжают использоваться также неселективные a-адреноблокаторы. Блокаторы a-адренергических рецепторов разделяют на две основные группы: 1) неселективные, которые ослабляют эффекты катехоламинов как на a1-, так и на a2 — адренорецепторы; 2) селективные, которые избирательно блокируют эффекты катехоламинов на a1-адренорецепторы сосудов и других органов и тканей. Кроме того, a-адреноблокирующими свойствами обладают некоторые антигипертензивные препараты, которые формально не относятся к группе a-адреноблокаторов (табл. 1). Так, например, a1-адреноблокирующее действие обнаружено у двух неселективных b-адреноблокаторов карведилола и лабетолола, у селективного блокатора С2-серотониновых рецепторов кетансерина и у агониста центральных С1А-серотониновых рецепторов урапидила.
Таблица 1 Основные группы блокаторов a-адренергических рецепторов 1. Неселективные a-адреноблокаторы: Дигидрированные алкалоиды спорыньи (дигидроэрготоксин и др.) Пироксикан Тропафен Феноксибензамин
|
К неселективным a-адреноблокаторам относятся такие препараты, как фентоламин, феноксибензамин и дигидрированные алкалоиды спорыньи.
Фентоламин вызывает кратковременную и обратимую блокаду как постсинаптических a1-адренорецепторов гладкомышечных клеток сосудистой стенки, так и пресинаптических и экстрасинаптических a2-рецепторов. Фентоламин является эффективным антигипертензивным препаратом.
Он используется главным образом при лечении гипертонических кризов, связанных с гиперкатехоламинемией, например, у больных с феохромоцитомой. При гипертоническом кризе фентоламин вводится внутривенно в виде болюса или внутривенной инфузии (2,5-10 мг).
Фентоламин используется также с диагностической целью при подозрении на феохромоцитому в тех случаях, когда невозможно биохимическое подтверждение диагноза.
Наряду с феохромоцитомой развитие гиперкатехоламинового криза может быть следствием внезапной отмены агониста центральных
a2-адренорецепторов клонидина, а также наблюдается у больных, принимающих ингибиторы моноаминооксидазы (МАО).
Таблица 2Сравнительная характеристика a1-адреноблокаторов
| Препараты | Длительность действия, ч | Максимум действия, ч | Терапевтические дозы, мг/сут | Кратность приема в сут. |
| Буназозин-ретард | ~ 24 | ? | 6-12 | 1 |
| Доксазозин | 18-36 | 5-6 | 1-20 | 1 |
| Празозин | 4-6 | 0,5 | 1-20 | 2-3 |
| Теразозин | > 18 | 1-1,7 | 1-20 | 1-2 |
| Тримазозин | 3-6 | 3-7 | 100-900 | 2-3 |
| Индорамин | > 6 | 2 | 50-150 | 2-3 |
| Кетансерин | > 12 | 1-2 | 20-40 | 1-2 |
| Урапидил | 6-8 | 3-5 | 15-120 | 1-2 |
| По: N. Kaplan [8] с некоторыми изменениями и дополнениями. |
У больных, получающих ингибиторы МАО, гиперкатехоламиновый гипертонический криз может развиться при одновременном приеме лекарственных препаратов или пищевых продуктов, содержащих тирамин, эфедрин и другие симпатомиметические амины.
Богаты тирамином и потому несовместимы с ингибиторами МАО такие пищевые продукты, как шоколад, бананы, соевые бобы, кефир, пахтанье, куриная печень, некоторые сорта сыра (чеддер, камамбер и стилтон) и вина (например, кьянти), а также экстракты дрожжей (включая пивные).
Симпатомиметические амины, помимо прочего, входят в состав комбинированных препаратов, используемых при лечении ринита, сенной лихорадки и бронхиальной астмы. Феноксибензамин в отличие от фенталамина вызывает длительную и необратимую блокаду a-адренергических рецепторов. Его a-адреноблокирующее действие после приема внутрь продолжается до 2 сут или более.
Феноксибензамин служит для лечения больных с феохромоцитомой перед операцией, а также в неоперабельных случаях. Начальная доза препарата составляет 10 мг 1 раз в сутки. При необходимости доза феноксибензамина постепенно повышается с тем, чтобы снизить артериальное давление (АД) до желаемого уровня.
Ни фентоламин, ни феноксибензамин не используются при лечении гипертонической болезни, так как часто вызывают такие побочные проявления, как ортостатическая гипотония, рефлекторная тахикардия, головокружение, слабость и другие. Побочные действия фенталамина и феноксибензамина объясняют неселективностью их действия на
a-адренергические рецепторы. Ведь эти неселективные a-адреноблокаторы оказывают свое антигипертензивное действие в основном благодаря блокаде a1-адренорецепторов сосудистой стенки. Вызываемая же фентоламином и феноксибензамином блокада a2-адренорецепторов, расположенных на пресинаптической мембране окончаний симпатических нервных волокон, в общем нежелательна у больных с артериальной гипертензией. При блокаде пресинаптических a2-адренорецепторов увеличивается высвобождение норэпинефрина (норадреналина) из окончаний симпатических нервов и одновременно уменьшается высвобождение ацетилхоламина из окончаний блуждающего нерва [1, 2]. Из дигидрированных алкалоидов спорыньи заслуживают упоминания лишь производные дигидроэрготоксина. Дело в том, что дигидроэрготоксина метансульфонат (дигидроэргокристин) входит в состав таких некогда популярных комбинированных антигипертензивных препаратов, как бринердин, кристепин и синепрес. Дигидроэрготоксин и другие дигидрированные алкалоиды спорыньи традиционно относят к a-адреноблокаторам [3, 4]. Однако, по некоторым наблюдениям, антигипертензивное действие производных дигидроэрготоксина по крайней мере отчасти опосредуется допаминергическими механизмами. В начале 70-х годов был синтезирован празозин, который переносился гораздо лучше, чем другие блокаторы a-адренергических рецепторов. Дальнейшие исследования показали, что празозин является селективным блокатором постсинаптических a1-адренорецепторов. В 80-е и 90-е годы были созданы другие a1-адреноблокаторы (альфузозин, буназозин, доксазозин, теразозин, тамсулозин и др.). Но среди доступных a1-адреноблокаторов большую часть фармацевтические фирмы-производители предназначают для лечения доброкачественной гиперплазии предстательной железы (например, альфузозин и тамсулозин). Для длительной терапии гипертонической болезни использовались два селективных a1-адреноблокатора — празозин и доксазозин. Кроме того, перспективными представляются теразозин и ретардная форма буназозина [5-7]. Празозин — селективный a1-адреноблокатор с относительно коротким антигипертензивным действием, поэтому его необходимо принимать 2-3 раза в сутки (табл. 2). После приема внутрь празозин быстро всасывается в желудочно-кишечном тракте. Плазменные концентрации препарата достигают максимума через 2-3 ч. С плазменными белками связывается более 70% празозина. Метаболизируется он главным образом в печени, 70% празозина и его метаболитов экскретируется с фекалиями, остальная часть — через почки. Период полужизни празозина в плазме крови — 2-4 ч. Для празозина характерен так называемый эффект первой дозы — резкое снижение АД после приема первой дозы препарата, которое особенно выражено в ортостатическом положении и проявляется головокружением и в ряде случаев обмороком.
Опыт клинического применения празозина показывает, что по
антигипертензивной эффективности он не уступает тиазидным диуретикам, b-адреноблокаторам, антагонистам кальция и ингибиторам АПФ. По наблюдениям F. Zeenen и соавт. [9], празозин вызывает обратное развитие гипертрофии левого желудочка у мужчин с гипертонической болезнью.
Важное клиническое значение имеют дополнительные фармакологические эффекты празозина и других a1-адреноблокаторов. В отличие от всех других антигипертензивных препаратов селективные a1-адреноблокаторы улучшают липидный состав крови.
Они значительно снижают содержание в крови общего холестерина за счет его атерогенной фракции — холестерина липопротеидов низкой плотности и одновременно повышают уровни антиатерогенных липопротеидов высокой плотности. Под влиянием a1-адреноблокаторов также снижается содержание триглицеридов [10].
Празозин и другие a1-адреноблокаторы повышают чувствительность тканей к действию инсулина. Они вызывают небольшое, но статистически достоверное снижение базальных уровней глюкозы (на 7 мг/дл или 5%) и инсулина (на 14 пмоль/л или 17%) у больных гипертонической болезнью.
Преобладание a1-адренорецепторов в гладкой мускулатуре предстательной железы и шейке мочевого пузыря послужило основанием для использования празозина, а затем и других a1-адреноблокаторов у больных с доброкачественной гиперплазией (аденомой) предстательной железы.
В ряде контролируемых исследований показано, что a1-адреноблокаторы значительно улучшают клинические симптомы и признаки у больных с доброкачественной гиперплазией предстательной железы. В частности, они увеличивают максимальную и среднюю скорость мочеиспускания.
Благодаря этим полезным фармакологическим свойствам празозин и другие a1-адреноблокаторы считаются особенно показанными для лечения артериальной гипертензии у больных с доброкачественной аденомой предстательной железы, атерогенной дислипидемией, сахарным диабетом или нарушенной толерантностью к глюкозе.
Другое показание к назначению a1-адреноблокаторов — лечение доброкачественной гиперплазии предстательной железы вне зависимости от уровня АД. Наблюдения показывают, что у лиц с исходно нормальным АД a1-адреноблокаторы улучшают мочеиспускание, не оказывая при этом существенного антигипертензивного действия.
По этой причине a1-адреноблокаторы могут быть использованы для лечения доброкачественной гиперплазии предстательной железы у больных как с повышенным, так и с нормальным АД.
Несмотря на свои потенциально полезные свойства, первый селективный a1-адреноблокатор празозин не получил широкого распространения при лечении гипертонической болезни из-за частого развития побочных явлений, а также недостаточно высокой антигипертензивной эффективности при длительном применении.
Так, в многоцентровом контролируемом исследовании VACS (Veterans Affair Cooperative Study) из-за побочных явлений празозин пришлось отменить у 12% больных. Слабость, сонливость и головокружение встречались при лечении празозином достоверно чаще, чем при назначении плацебо [11]. Празозин при длительном применении оказался недостаточно эффективным как антигипертензивный препарат у больных черной расы (30-35%), а также у молодых белых мужчин (46%). И лишь у белых мужчин в возрасте 60 лет и старше антигипертензивная эффективность празозина была достаточно высокой (66%) [12]. Неожиданными оказались результаты исследования VACS, касающиеся влияния празозина на гипертрофию левого желудочка у больных гипертонической болезнью. После 1-годичной терапии празозином масса миокарда левого желудочка не уменьшилась. У больных с исходной массой левого желудочка не более 350 г лечение празозином сопровождалось недостоверным увеличением массы миокарда левого желудочка [13].
Учитывая непродолжительное действие празозина, недостаточную антигипертензивную эффективность, отсутствие влияния на гипертрофию левого желудочка и плохую переносимость, нетрудно понять, почему первый селективный
a1-адреноблокатор в последние годы довольно редко используют для длительной терапии гипертонической болезни. Доксазозин — другой селективный a1-адреноблокатор, который обладает всеми ценными фармакологическими свойствами празозина, но лишен многих его недостатков. Как a1-адреноблокатор доксазозин более чем в 2 раза превосходит празозин по селективности в отношении a1-рецепторов. Доксазозин оказывает длительное антигипертензивное действие, которое продолжается от 18 до 36 ч. Благодаря этому доксазозин назначают 1 раз в сутки. Для доксазозина не характерен «эффект первой дозы». Ему свойственно постепенное начало антигипертензивного действия. При однократном приеме внутрь в утренние часы максимум антигипертензивного действия доксазозина наблюдается через 5-6 ч [8, 14]. При приеме препарата на ночь максимальный эффект наступает через 8-12 ч и приходится в период времени с 6 до 11 ч утра, т.е. на утренний подъем АД [15]. Утренний подъем АД, который связывают с гиперактивацией симпатико-адреналовой системы, у больных гипертонической болезнью часто сочетается с развитием таких сердечно-сосудистых осложнений, как мозговой инсульт и инфаркт миокарда. Поэтому предполагают, что профилактический эффект доксазозина при гипертонической болезни, возможно, окажется более выраженным, если препарат назначать на ночь, а не в утренние часы, как это обычно делается.
По фармакокинетическим показателям доксазозин также значительно отличается не только от празозина, но и от других селективных a1-адреноблокаторов. После приема внутрь доксазозин почти полностью всасывается в желудочно-кишечном тракте.
Пища замедляет всасывание доксазозина примерно на 1 ч, но не оказывает существенного влияния на его основные фармакокинетические показатели. Поэтому считается, что доксазозин можно принимать вместе с пищей, а не только натощак. Биодоступность препарата колеблется от 62 до 69%.
В крови 98-99% доксазозина циркулирует в связи с плазменными белками.
Плазменные концентрации доксазозина достигают максимума через 2-3 ч после приема препарата внутрь. Его период полужизни в плазме крови составляет от 19 до 22 ч, что значительно больше, чем у всех других
a1-адреноблокаторов. Антигипертензивная эффективность доксазозина в сравнении с плацебо, амлодипином, ацебутололом, хлорталидоном и эналапралом была хорошо изучена в крупном рандомизированном исследовании TOMH,S (Treatment Af Mild Hypertension Study), в котором принимали участие 902 больных с мягкой формой гипертонической болезни (исходно диастолическое АД в пределах от 90 до 99 мм рт.ст.).
Больные наблюдались ежемесячно в течение 4 лет. При лечении доксазозином (1-2 мг/сут) средние значения АД достоверно снизились по сравнению с плацебо (на 13,4/11,2 мм рт.ст. против 8,6/8,8 мм рт.ст.; р
Альфа-адреноблокаторы в лечении когнитивных и сосудистых нарушений головного мозга
М.Ф. Иванова, С.К. Евтушенко, Донецкий национальный медицинский университет им. М. Горького, Институт неотложной и восстановительной хирургии им. В.К. Гусака АМН Украины, г. Донецк
Цереброваскулярная патология занимает одно из ведущих мест в структуре заболеваемости и смертности населения развитых стран. Распространенность инсультов и транзиторных ишемических атак составляет, по различным данным, от 500 до 800 на 100 тыс.
населения, причем отмеченный показатель имеет четкую тенденцию к росту в последние годы [1, 2, 5]. В Украине регистрируется около 110-125 тыс.
инсультов ежегодно, при этом показатели смертности от данной патологии превышают в 2,5 раза аналогичные показатели в странах Запада [2].
Существенное значение, особенно в пожилом и старческом возрасте, имеет хроническая цереброваскулярная недостаточность, приводящая к развитию когнитивных нарушений. В свою очередь, сосудистые и когнитивные нарушения существенно влияют на трудоспособность и социальную адаптацию.
Благодаря широкому спектру фармакологических эффектов на центральную и периферическую нервную систему для лечения сосудистых и когнитивных нарушений головного мозга используются препараты, принадлежащие к группе альфа-адреноблокаторов.
Напомним, что в адренергических синапсах передача возбуждения осуществляется посредством медиатора норадреналина. В пределах периферической иннервации норадреналин принимает участие в передаче импульсов с адренергических (симпатических) нервов на эффекторные клетки.
В ответ на нервные импульсы происходит высвобождение норадреналина в синаптическую щель и последующее взаимодействие его с адренорецепторами постсинаптической мембраны. Адренергические рецепторы находятся в ЦНС и на мембранах эффекторных клеток, иннервируемых постганглионарными симпатическими нервами [3].
Существующие в организме адренорецепторы обладают неодинаковой чувствительностью к химическим соединениям. Образование комплекса «лекарство — рецептор» с одними веществами вызывает повышение (возбуждение), с другими — снижение (ингибирование) активности иннервируемой ткани или органа.
Для объяснения этих различий в реакциях разных тканей в 1948 году Ahlquist предложил теорию существования двух типов рецепторов: альфа и бета. Обычно стимуляция альфа-рецепторов вызывает эффекты возбуждения, а стимуляция бета-рецепторов сопровождается эффектами ингибирования, торможения.
Хотя в целом альфа-рецепторы относятся к рецепторам возбуждающим, а бета-рецепторы — к рецепторам тормозного плана, из этого правила имеются определенные исключения. Так, в сердце, в миокарде превалирующие бета-адренорецепторы являются стимулирующими.
Возбуждение бета-рецепторов сердца повышает скорость и силу сокращений миокарда, сопровождается повышением автоматизма и проводимости в AV-узле. В желудочно-кишечном тракте и альфа-, и бета-рецепторы являются ингибирующими. Их возбуждение вызывает релаксацию гладкой мускулатуры кишечника.
Препараты, обладающие способностью экранировать (закрывать) постсинаптические альфа-адренорецепторы от контакта с медиатором (норадреналин) или адреномиметиками, циркулирующими в крови (эндогенный адреналин, лекарственные средства), делят на селективные альфа-1-адреноблокаторы (альфузозин, празозин, доксазозин, тамсулозин, теразозин и др.
) и неселективные, блокирующие и альфа-1-, и альфа-2-адренорецепторы (фентоламин, троподифен, алкалоиды спорыньи и их производные, ницерголин, пророксан, бутироксан и др.). Препараты этой группы препятствуют прохождению сосудосуживающих импульсов через адренергические синапсы и вызывают за счет этого расширение артериол и прекапилляров [1, 3].
Альфа-адреноблокирующее средство ницерголин является синтетическим производным алкалоидов спорыньи (спорынья (лат.
Claviceps) — род микроскопических грибков семейства спорыньевых (Clavicipitaceae) из отряда сумчатых (Hypocreales) грибов, паразитирующий на некоторых злаках, в том числе на ржи и пшенице) с присоединенным бромзамещенным остатком никотиновой кислоты (никотиновая кислота, или ниацин, витамин PP, витамин B3 — растворимый в воде витамин, участвующий во многих окислительных реакциях живых клеток). Оказывает вазодилатирующее (в т.ч. в отношении мозговых артерий) действие. Улучшает микроциркуляцию. Содержащийся остаток никотиновой кислоты оказывает прямое миотропное спазмолитическое действие на мышечную оболочку резистивных сосудов, повышает их проницаемость для глюкозы (нивелируя противоположный эффект эрголинового кольца), что наиболее ярко проявляется в отношении сосудов головного мозга и конечностей. Повышает мозговой, легочный и почечный кровоток. Снижает тонус центральных сосудов, повышает артериальный кровоток, увеличивает доставку кислорода и глюкозы. Улучшает кровоснабжение в конечностях, особенно при нарушениях периферического кровообращения, обусловленных функциональными артериопатиями. В терапевтических дозах не влияет на АД, у больных с артериальной гипертензией может вызывать постепенное умеренное снижение давления.
Ницерголин зарегистрирован в более чем 50 странах мира, применяется более 30 лет в терапии когнитивных, аффективных, поведенческих расстройств у пожилых людей [11]. На протяжении периода использования препарата возросла рациональность его назначения.
Первоначально ницерголин рассматривали как вазоактивное вещество и назначали главным образом при цереброваскулярных расстройствах.
Дальнейшие исследования показали, что фармакологический профиль ницерголина более комплексный, и препарат начали применять при различных формах деменции, включая болезнь Альцгеймера [8, 11].
Важными в действии ницерголина являются его изученные нейромедиаторные эффекты. Ницерголин влияет на холинергические процессы в мозге. Ослабление холинергической нейромедиации рассматривается в настоящее время как ведущее звено в развитии возрастных нарушений памяти, когнитивных функций, в патогенезе различных нейродегенеративных заболеваний головного мозга [1, 9].
Ницерголин повышает синтез ацетилхолина путем активации холинацетилтрансферазы, повышает высвобождение ацетилхолина из пресинаптических терминалей, уменьшает распад ацетилхолина путем ингибирования ацетилхолинэстеразы, нормализует содержание постсинаптических М-холинорецепторов в различных отделах ЦНС, стимулирует рецептор-эффекторные реакции путем активации фосфоинозитидного каскада [1, 10].
Ницерголин обладает прямым протекторным действием в отношении образования бета-амилоида — основного гистологического субстрата болезни Альцгеймера, активируя транслокацию фермента протеинкиназы С [6, 11].
Также ницерголин обладает разнообразными нейропротекторными свойствами: стимулирует обратный захват глутамата и препятствует развитию опосредованных глутаматом нейротоксических эффектов при гипоксии, оказывает антиапоптозное действие, проявляет антиоксидантные эффекты, стимулирует образование фактора роста нервов (нейротрофическое действие), способствующего сохранности холинергических нейронов, регулирует обмен кальция в нервной ткани [1, 11]. Еще один компонент ноотропного и вазотропного действия ницерголина — стимуляция мозгоспецифичной синтазы оксида азота [1]. По современным представлениям, оксид азота не только обладает вазорегулирующими свойствами в отношении сосудов головного мозга, но и вовлечен в обеспечение процессов обучения и памяти [11]. Препарат обладает антиагрегантным эффектом, ингибируя агрегацию тромбоцитов и эритроцитов и препятствуя таким образом развитию реакции тромбообразования.
Таким образом, фармакологический спектр действия ницерголина характеризуется наличием следующих эффектов:
- ноотропного;
- вазотропного;
- нейромедиаторного;
- нейропротекторного;
- метаболического;
- антиагрегантного [4].
Уникальность эффектов ницерголина является фундаментом его клинического применения, существенно расширившегося за последние годы.
Фармакодинамические свойства ницерголина основываются на его способности влиять на клеточный метаболизм — повышать утилизацию глюкозы и кислорода, увеличивать содержание АТФ, белков и синтез нуклеиновых кислот.
Препарат улучшает мозговое кровообращение, обеспечивает защиту головного мозга от повреждения в условиях гипоксии и ишемии.
Положительно влияет на нейронную передачу, увеличивая интенсивность обмена допамина и норадреналина, увеличивает уровень цАМФ [6].
Цифровой анализ данных ЭЭГ свидетельствует о положительном влиянии ницерголина на биоэлектрическую активность головного мозга и его адаптационные возможности. Ницерголин оказывает положительный эффект на когнитивную функцию, улучшает память, психомоторную активность, предотвращает аффективные нарушения и соматические дисфункции (повышенную утомляемость, анорексию, головокружение).
В суточной дозе 30-60 мг ницерголин способствует улучшению клинического состояния при синдроме деменции в течение 3-6-месячного периода наблюдения.
Терапевтический эффект увеличивается постепенно и становится клинически значимым приблизительно после 3 мес. лечения.
У пациентов с положительной реакцией на лечение ницерголином улучшение при синдроме деменции становится выраженным к 6-му мес. лечения [7].
Ницерголин быстро и почти полностью всасывается в пищеварительном тракте. Подвержен значительному эффекту первичного прохождения через печень. При приеме внутрь в дозе 70 мкг/кг концентрация в плазме крови составляет 100-200 нг/мл.
Ницерголин способен связываться с альбумином плазмы крови; степень связывания с ним приблизительно в 4 раза ниже способности препарата связываться с гликопротеином.
Процент связывания остается относительно постоянным при физиологических концентрациях протеина в плазме крови, даже когда концентрация ницерголина является повышенной (составляет 87 % при низких концентрациях ницерголина и 82 % — при высоких) [6].
Поскольку концентрация гликопротеина в плазме крови у пожилых пациентов при патологических состояниях, например при острых воспалительных процессах, злокачественных опухолях, или в случае стресса может повышаться, есть основания полагать, что эффективная концентрация активного ингредиента в этих условиях может быть сниженной. Ницерголин почти полностью метаболизируется путем гидролиза эфирной связи и N-деметилирования. Активные метаболиты, которые при этом образуются, конъюгируются с глюкуроновой кислотой.
Около 80 % метаболитов ницерголина экскретируется почками, 10 % — выводятся с калом. Период полувыведения ницерголина составляет 2,5 ч, период полувыведения основного метаболита 10-метокси-дигидролизергола (MDL) составляет 12-17 ч, а второго метаболита 1-метил-10-метокси-дигидролизергола (1-MMDL) — от 2 до 4 ч.
Показаниями к назначению ницерголина являются: острая и хроническая недостаточность мозгового кровообращения (в том числе при атеросклерозе сосудов головного мозга, преходящих нарушениях мозгового кровообращения, тромбозах и эмболиях сосудов головного мозга); мигрень; синдром Рейно; артериальная гипертензия (в качестве вспомогательного средства); используется в качестве поддерживающего средства для лиц пожилого возраста при цереброорганическом психосиндроме с такими основными признаками: снижение концентрации внимания, ослабление памяти, дезориентация, нарушения сна, болезнь Альцгеймера, болезнь Паркинсона, сосудистая и смешанная деменция.
Пациентам с нарушенной функцией почек (уровень креатинина в сыворотке крови выше 200 мг/мл) дозу необходимо снизить. Поскольку терапевтический эффект нарастает постепенно, рекомендуется принимать препарат в течение длительного времени (не меньше 3 месяцев), однако не реже чем через каждые 6 мес. следует оценивать необходимость дальнейшего лечения препаратом.
Противопоказанием к назначению Ницериума® являются повышенная чувствительность к ницерголину, алкалоидам спорыньи или другим компонентам препарата; перенесенный инфаркт миокарда; кровотечения; риск развития коллапса; ортостатические реакции; одновременное лечение адреномиметиками; период беременности и кормления грудью, детский возраст.
Побочные эффекты ницерголина весьма ограничены, как правило, слабо или умеренно выражены и в основном связаны с его адреноблокирующими свойствами: гипотензия, головокружение, ощущение жара и приливов крови к лицу; возможны нарушения сна и желудочно-кишечные расстройства (устраняются приемом препарата во время еды). В большинстве случаев описанные эффекты либо проходят спонтанно, либо после уменьшения дозы препарата и не требуют его отмены во время курса лечения.
Поскольку ницерголин угнетает агрегацию тромбоцитов и уменьшает вязкость крови, во время приема препарата следует чаще контролировать параметры коагулограммы при одновременном применении с другими препаратами, влияющими на свертывание крови. Ницерголин может усиливать действие гипотензивных препаратов.