В данной статье будет подробно раскрыта тема такого состояния как гиперинсулинемия, причины его развития, возможные симптомы, диагностика, а также необходимая помощь и профилактика.
Что представляет собой гиперинсулинемия?
Гиперинсулинемия – состояние, для которого характерна высокая концентрация в крови гормона инсулина.
Инсулин синтезируется поджелудочной железой. Этот гормон в норме производит транспортировку глюкозы из крови в ткани, при этом организм получает достаточное количество энергии. При развитии гиперинсулинемии в организме наблюдается резистентность к действию данного гормона.
В результате чего поджелудочная железа пытается синтезировать еще больше инсулина, чтобы компенсировать гормональный недостаток. Весь процесс приводит к избытку инсулина в организме человека.Данная патология является причиной развития преддиабета.
Без проведения необходимой терапии состояние достаточно быстро и легко может перейти в диабет.
Выделяют первичный и вторичный гиперинсулинизм.
- Первичный – возникает из-за опухолевого роста клеток или гиперплазии поджелудочной железы;
- Вторичный – характеризуется дефицитом других гормонов, патологическими процессами в печени и нарушениями в нервной системе.
Часто избыток инсулина связывают с сахарным диабетом. Но существует множество других причин, при которых наблюдается рост гормона в крови, однако определить их не всегда удаётся.
Причины гиперинсулинизма
Врожденные патологические процессы, которые возникают из-за внутриутробных аномалий, мутаций и задержки роста плода.
Выделяют причины приобретенной гипогликемии:
- Панкреатические – способствуют возникновению абсолютной гиперинсулинемии;
Наблюдается при доброкачественных или злокачественных опухолях.
- Непанкреатические – способствуют относительному росту содержания инсулина в крови).
Развивается при:
- Нарушенном питании;
- Эндокринных заболеваниях;
- Патологии печени.
Основные симптомы повышенного инсулина
- Артериальная гипертензия;
- Снижение остроты зрения;
- Головные боли;
- Набор массы тела;
- Мышечная слабость;
- Усталость;
- Тахикардия;
- Тревога и раздражительность;
- Тремор;
- Онемение конечностей;
- Постоянная жажда;
- Частое желание сладкой пищи;
- Снижение внимания.
Необходимо своевременно заметить патологические изменения в своем организме и проконсультироваться с врачом-эндокринологом, который даст правильные рекомендации.
Повышенный инсулин в крови также связан с инсулинорезистентностью, ишемической болезнью сердца и рядом других заболеваний.
К наиболее опасным последствиям относится диабет, который является серьезной проблемой из-за высокого распространения и быстрого роста количества больных.
Конкретно диабет 2 типа вызван инсулинорезистентностью, при этом поджелудочная железа вырабатывает достаточно гормона инсулина, который никак не действует.
Организм воспринимает это как недостаток инсулина и пытается восполнить его дефицит. Так возникает гиперинсулинемия.
Высокий инсулин при нормальном сахаре у женщин является основным компонентом в развитии серьезного заболевания СПКЯ – синдрома поликистозных яичников.
Проведено множество исследований, которые подтверждают, что у женщин с СПКЯ и избыточной массой тела (и без нее) присутствуют такие патологические состояния как гиперинсулинемия и инсулинорезистентность.
Именно они являются главной причиной заболевания.
Артериальную гипертензию зачастую связывают с лишним весом и чаще встречается она у людей с избытком инсулина. Именно поэтому высокое артериальное давление проявляется чаще в несколько раз у лиц, страдающих сахарным диабетом второго типа, нежели у людей без данной патологии.
В нормальных условиях гормон инсулин способствует расширению сосудов. Когда развивается инсулинорезистентность- эффект расширения сосудов блокируется и развивается тоническое напряжение, которое приводит непосредственно к высокому артериальному давлению.
Также, за счет высокой концентрации сахара в крови, начинает усиливаться обратное всасывание глюкозы вместе с натрием, что в конечном итоге приводит к развитию высокого артериального давления.
Правильный и полноценный медицинский осмотр, а также история заболевания пациента предоставят необходимую информацию для врача, которая поможет детально разобраться в причине повышенного инсулина в крови и определить всевозможные осложнения.
Последствия высокого инсулина в организме человека могут быть необратимыми. К ним относится: ишемическая болезнь сердца, артериальная гипертензия, заболевания сердца и сосудов, высокая вероятность развития синдрома поликистозных яичников, избыточная масса тела, патология щитовидной железы.
Осложнения при избытке инсулина
Подразделяют осложнения на ранние и поздние.
Ранние осложнения проявляются в виде инсульта и инфаркта миокарда. В крайних случаях может развиться гипогликемическая кома.
Поздние осложнения проявляются в виде нарушения памяти, затруднения речи, энцефалопатии и паркинсонизме.
При отсутствии должной диагностики и правильного лечения данное заболевание способствует истощению эндокринной системы, что в конечном итоге приводит к развитию диабета.
Диагностика гиперинсулинемии
Клиническая картина заболевания является основным этапом диагностики, при этом определяется наличие тремора, уточняется частота потери сознания, изучается психоэмоциональное состояние пациента. Врач-эндокринолог узнает анамнез заболевания и наличие возможных наследственных и приобретенных заболеваний.
Людям с повышенным инсулином в крови необходимо определить гликемический профиль, который заключается в суточном измерении количества глюкозы в крови.
Используется индекс инсулинорезистентности, благодаря которому можно точно определить чувствительность тканей организма на действие инсулина. Так же его используют для определения возможных сердечно-сосудистых патологий, заболевания поджелудочной железы, печени, сахарного диабета.
Данный анализ необходимо проводить строго натощак утром. Необходимо исключить прием пищи за 10 часов до исследования. Непосредственно в день исследования не курить и минимизировать физическую активность. Лечащего врача поставить в известность о постоянном приеме медикаментов.
Повышенный индекс инсулинорезистентности означает то, что уровень инсулина в крови превышает норму. Это говорит о высокой вероятности развития сердечно-сосудистых заболеваний, сахарного диабета, патологий со стороны печени, поджелудочной железы и почек.
Лечение
Лечение гиперинсулинемии основывается на:
- Соблюдении правильного питания и индивидуальной диеты. В своем рационе следует ограничить продукты с высокой калорийностью, полностью исключить полуфабрикаты и алкоголь;
Для составления корректного рациона питания с расчетом калорий необходимо обратиться за консультацией к специалисту.
- Физическая активность должна присутствовать в жизни каждого человека. Благодаря ей улучшается состояние всех важных органов и систем. От физической активности полностью зависит самочувствие человека.
Для эффективного лечения необходима полноценная диагностика и постановка точного диагноза. При первых признаках быстрой утомляемости, набора массы тела, повышенного артериального давления, онемения конечностей и потоотделения следует незамедлительно обратиться за помощью к врачу-эндокринологу.
Консультация специалиста
Я, врач-эндокринолог, Романов Георгий Никитич, являюсь специалистом высшей квалификационной категории. Опыт моей работы, который составляет более 25 лет, получен за время стажировки в Великобритании, Франции, Германии, а также работы в больницах, частных клиниках и в зарубежных медицинских учреждениях.
Принципом моей работы является детальный сбор анамнеза, точная диагностика, после которой назначается индивидуальное лечение. Врач-эндокринолог работает не только с одним заболеванием, но с его всевозможными осложнениями.
Моей целью является оказание необходимой помощи людям, которые страдают патологией эндокринной системы, как при личном общении на приеме, так и при онлайн-консультации. Моя онлайн-консультация проводится не только по результатам анализов. Вы также можете воспользоваться услугой при изменении самочувствия и для уточнения возникших вопросов.
Вместе мы обсудим, что представляет собой избыток инсулина в организме, после чего я проведу полную диагностику и будет назначено правильное лечение с дальнейшей профилактикой.
Преимуществом онлайн-консультации является экономия времени, возможность обратиться за помощью не выходя из дома, быстрое получение ответа на все волнующие Вас вопросы, а также оплата услуги с помощью банковской карточкой.
Чтобы записаться на онлайн-консультацию необходимо точно выбрать дату и время, после чего оставить заявку на сайте. После записи ожидайте звонка администратора для подтверждения услуги.
Вывод
Гиперинсулинемия – состояние, от которого зависит качество жизни человека в целом. Важно понимать, что данная патология является очень серьезной и связана с нарушением метаболизма.
Человек счастлив, когда здоров, именно поэтому следует внимательно относиться к своему здоровью, так как своевременное обращение к специалистам поможет Вам избежать серьезных последствий, а здоровый образ жизни и правильное питание должны быть постоянной привычкой каждого человека.
Повышен инсулин в крови — причины у женщин, мужчин, что означает повышенный инсулин при нормальном сахаре
Инсулин — один из ключевых гормонов, участвующий в метаболических процессах. Его своевременная и достаточная продукция требуется для нормального функционирования всех органов и систем. Потому важно понимать его роль, границы нормы в анализе крови, о чем говорит повышение критерия и что можно предпринять для восстановления баланса.
Инсулин — что это и зачем исследуется
Инсулин — гормон, синтезируемый поджелудочной железой. За его продукции отвечают бета-клетки, а концентрация связана с уровнем глюкозы. При попадании последней в организм, например, с приемом пищи, поджелудочная железа активно секретирует инсулин для транспортировки сахара и его последующего использования.
Для инсулина характерны два основных направления действия:
| Активация/усиление | Подавление |
| Процессов поглощения глюкозы клетками: мышечными, жировыми и печеночными | Образования глюкозы из соединений не углеводного типа |
| Синтеза гликогена в печени | Естественного разрушения клеточных структур |
| Восприимчивости клеток к аминокислотам | Разрушения жировых тканей |
| Биосинтеза ДНК, белков и жирных кислот | |
| Процессов транспорта ионов |
Для определения уровня инсулина проводится забор венозной крови, при условии, что за 12 часов до этого человек ничего не ест и пьет только чистую воду, а за 3 часа — не курит. Вместе с этим за день до сдачи материала требуется исключение ряда лекарственных средств, список которых формирует врач. Целью исследования может быть:
- Выявление новообразований поджелудочной железы.
- Определение причин развития гипогликемии.
- Контроль состояния здоровья пациента в период проведения плановой диспансеризации.
- Подтверждение или опровержение наличия инсулиннезависимого сахарного диабета и/или контроль его прогрессирования.
- Наблюдение за уровнем эндогенного инсулина у лиц с нарушениями в функционировании эндокринной системы.
- Диагностика резистентность к инсулину.
- Подтверждение или опровержение необходимости пациентам с диабетом использования дополнительного инсулина или препаратов, снижающих уровень глюкозы.
- Контроль состояния после пересадки островковых клеток.
Нормальные значения
Референсные значения варьируют в соответствии с возрастной группой:
| Группа | Нормы, мкЕд/мл |
| С рождения до 9 лет | 3-19 |
| 10-18 лет | 2.7-10.4 |
| 18-60 лет | 3-26 |
| От 60 лет | 6-35 |
У беременных женщин допустимыми границами считаются 6-28 мкЕд/мл.
Причины повышения
Высокий уровень инсулина называет гиперинсулинемией или гиперинсулинизмом. Выделяют врожденную и приобретенную формы патологии:
- Врожденная — основывается на мутациях в геноме, аномалиях развития плода или задержках роста плода.
- Приобретенная — возникает на фоне других патологических процессов, стимулирующих выработку избыточного количества инсулина.
Приобретенную гиперинсулинемию могут провоцировать:
- Новообразования поджелудочной железы любого типа.
- Хронический панкреатит.
- Гиперплазия бета-клеток поджелудочной железы.
- Заболевания печени (опухоли, гепатозы, цирроз).
- Непереносимость глюкозы, фруктозы, галактозы.
- Другие эндокринные патологии (болезнь Аддисона, акромегалия, гипофизарный нанизм, микседема).
- Ожирение любой степени.
Также патологический процесс может провоцироваться неправильным питанием: продолжительным голоданием, обезвоживанием, дефицитом углеводов при значительных физических нагрузках. Другим этиологическим фактором может выступать неконтролируемый прием препаратов, снижающих концентрацию глюкозы.
Дополнительная симптоматика
Клиническая картина высокого уровня инсулина сопровождается в первую очередь симптомами основного заболевания, спровоцировавшего рост показателя. В число общих входят комбинации из ряда характерных признаков:
- Ощущение сухости во рту.
- Зуд и шелушение кожных покровов.
- Усиленное чувство голода.
- Затяжные процессы заживления даже незначительных ран.
- Онемение конечностей.
- Появление болезненности в мышцах.
- Частые судороги нижних конечностей.
- Повышение массы тела.
- Учащение сердечных сокращений.
- Усиленное потоотделение.
- Повышенная раздражительность и нестабильное эмоциональное состояние.
- Не проходящее недомогание и слабость.
- Потеря трудоспособности.
Опасность высокого инсулина
Повышенный инсулин может привести к ряду осложнений:
- Инсульту.
- Инфаркту миокарда.
- Гипогликемической коме.
- Энцефалопатии.
Вместе с этим, без соответствующей терапии гиперинсулинемия ведет к хронической гипоксии мозга, что повреждает нейроны и снижает интеллектуальные способности человека, затрудняя его повседневную жизнь.
Высокий инсулин при нормальном уровне глюкозы
Гиперинсулинемия в сочетании с нормальным уровнем глюкозы может указывать на относительно редкое заболевание – несахарный диабет.
Оно характеризуется нарушением процесса всасывания жидкости в почках для последующей концентрации мочи. Патология может быть первичной — связанной с генетическими дефектами, либо вторичной или приобретенной.
Приобретенный несахарный диабет делится на несколько подкатегорий:
- Центральный — сопряжен наследственными дефектами или патологическими процессами, вызывающими нарушения в синтезе гипоталамусом антидиуретического гормона.
- Нефрогенный — вызван отсутствием чувствительности почек к воздействию антидиуретического гормона из-за наследственных или приобретенных факторов.
- Функциональный — может наблюдаться у детей возрастной группы до 1 года.
- Гестагенный — иногда развивается у беременных.
- Ятрогенный — провоцируется лекарственными веществами, нарушающими действие антидиуретического гормона.
При выявлении сочетания гиперинсулинемии с нормальным сахаром крови врач в обязательном порядке проводит дополнительную диагностику, дифференцируя причину изменений.
Дополнительные диагностические мероприятия
При выявлении высоких показателей инсулина требуется подробный сбор анамнеза с уточнением наследственной предрасположенности к эндокринным заболеваниям. Затем применяются различные лабораторные и инструментальные исследования:
- Суточный мониторинг глюкозы.
- Функциональные пробы.
- Общий анализ и биохимия крови.
- Мониторинг артериального давления.
- ЭКГ.
- Гормональный профиль.
- Ультразвуковое исследование, сцинтиграция или МРТ поджелудочной железы и органов брюшной полости в целом.
Меры для нормализации показателя
Лечение стартует с корректировки рациона и подбора оптимальных физических нагрузок для человека. Затем к этому добавляется медикаментозная терапия, которая может включать:
- Глюкокортикоиды.
- Проведение инфузий.
- Седативные средства.
- Траквилизаторы.
В сложных случаях рекомендуется проведение удаления части или всей поджелудочной железы, химиотерапия.
Определение уровня инсулина — важный критерий диагностики состояния человека. Выявление отклонений от нормы требует полного обследования с применением всех необходимых дополнительных методов исследования. А на основании полученных результатов формируется вывод о причинах изменений и подбирается соответствующее лечение.
Что такое гиперинсулинемия
Гиперинсулинемия – явление патологического характера, которое по сути является увеличением количества инсулина в составе крови. Причины могут быть связаны с различными нарушениями, происходящими в организме, но результат один – скачок пептидного гормона, который вырабатывает поджелудочная железа. Что известно о гиперинсулинемии и как можно избежать подобного явления?
Почему развивается заболевание?
Специалисты выделяют следующие причины, которые приводят к возникновению патологии:
- поджелудочная железа начинает вырабатывать чрезмерное количество инсулина;
- чувствительность инсулиновых рецепторов снижается – возникает инсулинорезистентность;
- процесс переноса глюкозных молекул нарушается;
- происходят сбои при передаче сигналов в клеточной системе (определенные рецепторы не работают, поэтому у глюкозы нет возможности проникать в клетки).
Кроме этого, есть ряд предрасполагающих к гиперинсулинемии факторов.
Риски повышаются у следующих пациентов:
- обладающих наследственной предрасположенностью и имеющих родственников, страдающих сахарным диабетом;
- при нарушении центра регулирования таких чувств, как голод и насыщение;
- чаще диагностируется у женщин, особенно страдающих гормональными нарушениями, если поставлен диагноз синдром поликистозных яичников, а также при гестационном диабете;
- у людей, которые не проявляют физическую активность;
- при наличии пагубных привычек;
- у людей пожилого возраста;
- на фоне ожирения – излишняя жировая ткань приводит к тому, что рецепторы утрачивают восприимчивость к действию инсулина, и его синтез снижается;
- у пациентов, страдающих атеросклерозом;
- во время климактерического периода;
- при артериальной гипертензии;
- на фоне лечения гормональными препаратами, тиазидными диуретиками, бета-блокаторами.
Воздействие вредных веществ также негативно отражается на работе эндокринной системы
Подобные явления негативно отражаются на передаче сигналов в клетки. Резкое повышение инсулина может привести к развитию сахарного диабета, ожирению, гипогликемической коме. Кроме того, возникают риски нарушений в работе сердечно-сосудистой системы.
Как проявляется заболевание?
Симптомы при начальном развитии болезни отсутствуют, но после возникают явные признаки патологического нарушения:
- появление жировых отложений в области живота и верхней части туловища;
- приступы гипертонии;
- ощущение жажды;
- боли в мышечных тканях;
- головокружение;
- нарушение концентрации внимания;
- дрожь и озноб.
При гиперинсулинемии человек становится слабым, вялым, быстро устает
Если увеличение инсулина возникает из-за генетического синдрома или редкого заболевания, тогда проявляются и другие симптомы:
- нарушается зрение;
- кожные покровы темнеют, возникает сухость;
- на коже живота и бедер образуются заметные растяжки;
- больного беспокоит затрудненная дефекация;
- беспокоит болезненность в костях.
- Гиперинсулинемия – серьезное состояние, которое требует обязательной врачебной консультации.
- Высокий уровень инсулина в крови влияет на различные системы организма и связан с разными заболеваниями, поэтому рекомендована комплексная диагностика.
- Таблица № 1. Диагностические мероприятия для выявления гиперинсулинемии
| Анализ или обследование | Область исследования и особенности |
| Анализ на выявление определенных гормонов | Специалистов интересует уровень:
|
| Измерение артериального давления | Назначается суточный мониторинг – к телу пациента крепят специальный регистратор, оснащенный датчиком, который фиксирует появление и исчезновение пульсовых волн. |
| Вычисление особенностей конституции | Специалист определяет индекс массы тела (соотношение веса и роста), также во внимание берется отношение окружностей талии и бедер. |
| Общий анализ мочи | Определяет микроальбуминурию – наличие в моче небольшого количества белка, которого в норме здесь быть не должно. |
| Ультразвуковое исследование | Обследуется поджелудочная железа, печень, почки. |
| Биохимия крови | Специалистов интересует уровень общего холестерина, триглицеридов, липопротеидов низкой и высокой плотности.Также анализ выявляет количество глюкозы на «голодный» желудок и после приема пищи. |
| КТ (кардиотокография);МРТ (магнитно-резонансная томография) | Исследуются гипофиз и кора надпочечников. Диагностика назначается, чтобы исключить наличие синдрома гиперкортицизма (болезни Иценко-Кушинга). |
При симптомах гиперисулинемии рекомендуется посетить, помимо эндокринолога, консультации и других специалистов. В этом случае поможет кардиолог, диетолог, психотерапевт.
Как лечится заболевание?
В общем-то, как при сахарном диабете, на первом месте в терапии этого заболевания находится диета, направленная на избавление от лишних килограммов – не красоты ради, а больше для здоровья.
В основе питания лежит уменьшение калорийности употребляемой пищи
При составлении рациона учитывается несколько факторов:
- каким видом работы занимается пациент (умственным или физически трудом);
- занимается или нет спортом;
- вес на время обращения к специалисту и др.
Прием пищи сделать дробным – кушать 4-6 раз в день маленькими порциями.
При недостаточных физических нагрузках их следует увеличить, это сделает лечение более эффективным. Однако здесь существуют некоторые нюансы – статистическая силовая нагрузка может негативно отразиться на состоянии больного и стать причиной гипертонического криза. Поэтому при гиперинсулинемии лучше выбирать другие занятия.
Для людей, страдающих резкими повышениями глюкозы в крови, больше подходит йога, пилатес, плавание, аэробика, аквааэробика и т.п
- Коррекция питания и правильно подобранные тренировки, которые основаны на постепенном возрастании нагрузки, являются залогом улучшения состояния пациента.
- Кроме того, лечение также может включать прием медикаментозных средств.
- Таблица № 2. Препараты, назначаемые при гиперинсулинемии, и их действие
| Тип лекарств | Действие |
| Гипогликемические препараты: бигуаниды, тиазолидины | Лекарственные средства, которые снижают уровень сахара в крови. |
| Препараты с антигипертензивным действием | Назначаются для нормализации артериального давления, также, благодаря их приему, удается избежать развития инфарктов, инсультов. |
| Ингибиторы АПФ | Используются для лечения артериальной гипертензии – снижают как систолическое, так и диастолическое давление. |
| Станины и фибраты | Средства, эффективно снижающие уровень холестерина. |
| Ингибиторы обратного захвата серотонина | Лекарственные средства, которые снижают аппетит. |
| Препараты, содержащие альфа-лиоевую кислоту | Повышают утилизацию излишков глюкозы и выводят из организма лишний холестерин. |
Профилактические меры
Гиперинсулинемия – одно из тех заболеваний, которые, в большинстве случаев, можно предотвратить, если придерживаться простых правил:
- не употреблять чрезмерно жирную и сладкую пищу;
- включить в рацион побольше овощей и фруктов зеленого цвета;
- обеспечивать себя достаточными нагрузками – минимум ходить ежедневно в течение получаса;
- отказаться от пагубных привычек, негативно отражающихся на состоянии здоровья.
Данное заболевание является высоким фактором риска развития более серьезных болезней и состояний – сахарных диабетов, инсультов, инфарктов. Поэтому желательно выявлять недуг как можно раньше и своевременно лечить его.
Разные лица инсулиновой резистентности • Библиотека
В последние годы многие развитые страны столкнулись с эпидемическим ростом сахарного диабета 2-го типа (далее просто «диабет»). По данным, приведенным в обзоре профессора Калифорнийского университета Джеролда Олефски (“Cell”, 2013, 152, 673–687, doi: 10.1016/j.cell.2013.01.041), этой формой диабета страдают более 300 миллионов человек во всем мире, из них 55 миллионов в Индии, 25 миллионов — в США и 80 миллионов в Китае, причем количество пациентов удваивается каждые 10–15 лет. Диабет второго типа развивается, когда некоторые ткани пациента малочувствительны к действию инсулина, то есть приобретают инсулинорезистентность. Этот недуг не следует путать с более редким диабетом 1-го типа (юношеским диабетом) — заболеванием, при котором иммунные клетки по неустановленной причине атакуют специализированные бета-клетки поджелудочной железы, вырабатывающие гормон инсулин, и разрушают их.
В результате поджелудочная железа не в состоянии синтезировать достаточное количество инсулина, и больные вынуждены регулярно его вводить. Любой диабет опасен тяжелейшими осложнениями: слепотой, нарушениями свертываемости крови, кровоснабжения конечностей, работы нервной и сердечно-сосудистой систем.
Пытаясь бороться с диабетом 2-го типа, врачи и исследователи обращают особое внимание на его грозный предвестник — инсулинорезистентность.
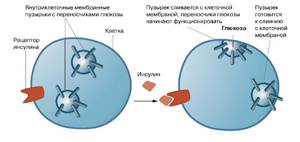
Основная физиологическая функция инсулина заключается в том, чтобы обеспечивать поступление глюкозы из периферической крови в клетки (прежде всего мышечной и жировой ткани) и подавлять избыточную продукцию глюкозы в клетках печени.
Эту задачу он выполняет, стимулируя экспрессию особых белков-транспортеров, которые перетаскивают глюкозу из периферической крови через клеточную мембрану внутрь клетки (рис. 1). В результате действия инсулина количество белков-транспортеров на мембране возрастает в 5–10 раз, а их содержание внутри клетки уменьшается на 50–60%.
Чувствительность клеток к инсулину зависит прежде всего от количества инсулиновых рецепторов и их активности. Так, жировые клетки и гепатоциты (клетки печени) содержат по 200–300 тысяч рецепторов, а моноциты и эритроциты — на порядок меньше.
Количество рецепторов и их сродство (аффинность) к инсулину непостоянны: у здоровых людей они выше вечером и ночью, а утром ниже; возрастают при физических нагрузках, уменьшаются у пожилых людей.
В норме инсулин также вызывает релаксацию гладкомышечной стенки сосудов за счет высвобождения оксида азота, однако и эта способность нарушена у пациентов с инсулинорезистентностью и ожирением.
Если восприимчивость периферических тканей к действию инсулина по какой-то причине снижена, у человека развивается компенсаторная гиперинсулинемия — его поджелудочная железа синтезирует и выделяет в кровь повышенное количество инсулина.
Пока бета-клетки могут работать в авральном режиме и поддерживать в плазме крови уровень гормона, достаточный для преодоления инсулинорезистентности, у пациентов сохраняется нормальная концентрация сахара в крови.
Однако резервы поджелудочной железы не безграничны, бета-клетки «выдыхаются», и тогда уровень сахара начинает расти.
Ситуация усугубляется тем, что при инсулинорезистентности неправильно работает печень.
Обычно этот орган поддерживает необходимую концентрацию сахара, расщепляя гликоген или синтезируя глюкозу из веществ неуглеродной природы. Когда уровень инсулина возрастает, здоровая печень снижает продукцию глюкозы.
А при инсулинорезистентности печень как ни в чем не бывало продолжает выбрасывать ее в кровь, что вызывает у голодного пациента гипергликемию.
Иными словами, когда бета-клетки утрачивают способность постоянно наращивать продукцию гормона, инсулинорезистентность перетекает в сахарный диабет 2-го типа, для которого характерны хроническая нехватка инсулина и, как следствие, повышенное содержание глюкозы в крови. Однако уровень сахара в крови — это только индикатор проблемы, суть которой заключается в том, что глюкоза не может попасть в клетки, они голодают и плохо выполняют свои функции.
Вопрос о причинах возникновения инсулинорезистентности остается открытым. Установлено, что она чаще развивается при избыточной массе тела и ожирении, у людей старше 45 лет, при недостаточной физической нагрузке, стрессе и повышенном артериальном давлении. Каким же образом ожирение содействует развитию инсулинорезистентности?
Ожирение и воспаление
Специалисты Национального института диабета США более 30 лет изучали индейцев племени пима, живущих в Аризоне и Мексике.
Они установили, что половина всех взрослых индейцев, населяющих резервации на территории Аризоны, болеют диабетом и 95% из них страдают от ожирения, а у мексиканских пима это заболевание наблюдается редко, и ожирение им не свойственно, потому что они едят низкокалорийные продукты с высоким содержанием пищевой клетчатки и физически гораздо активнее, чем их заграничные единоплеменники. Исследователи пришли к выводу, что главный фактор риска в развитии диабета 2-го типа — ожирение. Причем риск возникновения ожирения можно снизить даже при наследственной предрасположенности к нему, если вести правильный образ жизни.
В последние десятилетия наблюдается эпидемический рост числа людей с избыточным весом (см.: Калория и ее история, «Химия и жизнь», 2013, № 2). Так, в США около 65% взрослых людей имеют лишний вес и около 32% страдают от ожирения.
Как мы помним, ожирение часто сочетается с инсулинорезистентностью. Если масса человека превышает идеальную на 35–40%, то чувствительность к инсулину снижается более чем на 40%.
Развитию инсулинорезистентности способствует и усиленный выход жирных кислот из адипоцитов (клеток жировой ткани) в кровь.
Клинические исследования показали, что фармакологические ингибиторы липолиза (препараты, замедляющие расщепление жиров и тем самым снижающие уровень жирных кислот в крови) способны быстро вернуть пациентам с ожирением чувствительность к инсулину. Снижение веса также уменьшает поток жирных кислот и улучшает чувствительность к инсулину.
В организме существуют два основных способа энергетического обеспечения: «дневной» и «ночной». При «дневном» способе энергообеспечения главным источником энергии служит глюкоза и в меньшей степени — жир.
При «ночном», напротив, организм черпает энергию в основном из жирных кислот, поступающих в кровь при расщеплении жировых отложений.
По мнению ленинградского профессора-медика Владимира Михайловича Дильмана, при ожирении механизм суточного переключения энергетического гомеостаза нарушается, и организм переходит преимущественно на жировой путь обеспечения. Но почему это происходит?
Известно, что во взрослом организме количество жировых клеток постоянно. Накопление жира увеличивает объем адипоцита, что приводит к снижению плотности инсулиновых рецепторов на ее увеличенной поверхности, и чувствительность жировой ткани к действию инсулина падает.
Однако если человек по-прежнему переедает, клетки вынужденно продолжают синтезировать жиры из тех излишков глюкозы, которые не могут быть «потрачены» в других органах. Поджелудочная железа отвечает на это дополнительным, компенсаторным увеличением продукции инсулина.
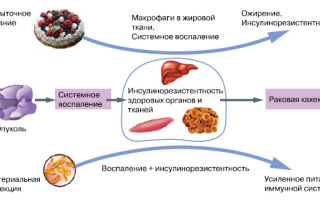
И всё же «накачка» адипоцитов жиром не может быть бесконечной. Когда жировая ткань перегружена, в ней нарастает гипоксия и часть адипоцитов погибает, вызывая воспаление. К очагу воспаления из костного мозга устремляются макрофаги. В норме жировая ткань содержит не более 5% макрофагов, но при ожирении их доля увеличивается до 50%.
При этом макрофаги активируются и секретируют воспалительные цитокины — небольшие пептидные молекулы, обеспечивающие мобилизацию воспалительного ответа, — в частности, фактор некроза опухоли TNF-α (запомним эту аббревиатуру, она нам еще понадобится) и интерлейкин-6.
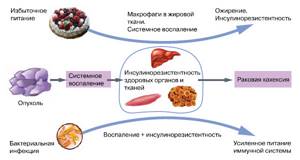
Эти цитокины, в свою очередь, поддерживают инсулинорезистентность как в адипоцитах, так и в клетках печени и мышц (рис. 2).
Как установили американские исследователи под руководством профессора Стивена Гринспуна, директора клиники при Гарвардской медицинской школе (Бостон, США), нейтрализация провоспалительного TNF-α улучшает чувствительность к инсулину при ожирении (“Journal of Clinical Endocrinology & Metabolism”, 2011, 96: E146–E150). Это открытие позволило предположить, что при ожирении жировая ткань становится источником хронической активации воспаления, способного поддерживать инсулинорезистентность (рис. 2, 3). Механизмы такой активации местного и системного воспаления интенсивно изучают.
Однако воспаление — это не болезнь, а нормальная реакция организма, в частности, на бактериальную инфекцию. Цель воспаления — уничтожить бактерии с помощью цитотоксической реакции «респираторного», или «кислородного взрыва».
Такое название она получила потому, что клетки-фагоциты, захватившие бактерии или продукты их распада, резко (взрывообразно) увеличивают потребление кислорода и глюкозы, которые участвуют в образовании высокоактивных радикалов, обладающих антибактериальной активностью.
Реакция достигает максимума уже через 50–120 секунд после начала фагоцитоза. Для осуществления реакции «респираторного взрыва» необходима быстрая доставка большого количества глюкозы к активированным фагоцитам.
Можно предположить, что такой направленный поток глюкозы обеспечивается с помощью физиологического механизма инсулинорезистентности, который временно ограничивает приток глюкозы в мышцы и жировые клетки, направляя ее главным образом в нейтрофилы и макрофаги (рис. 3).
Оказалось, что инсулинорезистентность регулирует потоки глюкозы и в других адаптационных ситуациях, во время беременности например.
Беременность и рост опухолей
Глюкоза — основной источник энергии для матери и плода. По мере роста плоду нужно всё больше глюкозы, причем ее потребление во второй половине беременности опережает ее доступность. Поэтому в норме уровень глюкозы в крови плода примерно на 10–20 мг/100 мл (0,6–1,1 ммоль/л) ниже, чем у матери.
(Физиологическая норма для беременной женщины — 3,3–6,6 ммоль/л.
) Обращает на себя внимание тот факт, что в период максимального роста плода у всех беременных развивается физиологическая инсулинорезистентность, с помощью которой, вероятно, потоки глюкозы и перенаправляются от органов матери к растущему плоду.
Этот эффект регулирует плацента — основной источник секреции TNF-α во время беременности, особенно во второй ее половине. Примерно 94% плацентарного TNF-α высвобождается в кровоток матери, и только 6% — в кровоток плода. Таким образом, высокий уровень TNF-α обеспечивает инсулинорезистенность материнских тканей.
После родов его концентрация резко и быстро снижается, и параллельно восстанавливается чувствительность к инсулину. Однако у беременных с избыточной массой тела содержание TNF-α значительно выше, чем у беременных с нормальным весом.
У чрезмерно полных женщин беременность часто протекает с осложнениями, и после родов чувствительность к инсулину не только не восстанавливается, но и возрастает риск развития диабета.
Однако при правильном течении беременности адаптивная инсулинорезистентность помогает нормальному росту плода.
Эмбриональные ткани по изоферментному и антигенному составам, а также типу клеточного метаболизма (активации гликолиза) подобны опухолевым. Возникает вопрос: развивается ли инсулинорезистентность при опухолевом росте и если да, то к каким последствиям приводит?
Раковые клетки усваивают глюкозу в 10–30 раз активнее нормальных. Потребляя глюкозу со скоростью большей, чем скорость ее поступления, раковая опухоль действует как мощный насос, выкачивающий глюкозу из организма хозяина.
Исследователи из Университета Южной Калифорнии Этан Оргел и Стивен Миттелмен показали, что большинство злокачественных опухолей вызывает инсулинорезистентность в мышцах, печени и жировой ткани больного параллельно с увеличением уровня провоспалительного TNF-α (“Current Diabetes Reports”, 2013, 13, 213–222, doi: 10.
1007/s11892-012-0356-6). Это создает более выгодные условия для роста опухоли в ущерб нормальной работе здоровых органов и тканей.
Вопреки распространенному мнению, что больные раком умирают от метастазов в жизненно важные органы, многие из них погибают от комплекса болезней, известных под названием «паранеопластический синдром».
Это вторичные неспецифические нарушения функций различных органов и систем, непосредственно не связанных с локализацией первичной опухоли. Паранеопластический синдром встречается у 60% онкологических больных.
Он вызван нарастающим синтезом TNF-α, который в высокой концентрации превращается в эндотоксин, вызывающий системное воспаление и длительное ограничение поступления глюкозы в мышцы, печень и жировую ткань. В результате масса мышечной и жировой тканей уменьшается, и пациент заметно теряет в весе — так называемая раковая кахексия (рис.
3). Поэтому при онкологических заболеваниях целесообразно применять препараты, уменьшающие системное воспаление и повышающие чувствительность клеток печени, мышц и жировой ткани к действию инсулина. Они могут не только замедлить рост опухоли, но и предупредить развитие кахексии.
Давно было замечено, что антидиабетические препараты (бигуаниды), восстанавливающие инсулинорезистентность, повышают эффективность лечения онкологических больных, но для предупреждения развития кахексии их не использовали, вероятно, из-за недостаточного внимания к эффекту инсулинорезистентности при опухолевом росте.
А еще резистентность к инсулину может привести к развитию синдрома поликистозных яичников (механизм развития не установлен). У женщин при этом заболевании нарушается менструальный цикл и развивается бесплодие. Полугодовое лечение наиболее известным бигуанидом метформином восстанавливает регулярный цикл овуляции.
Инсулинорезистентность — защитная реакция или болезнь?
Чтобы выбрать правильный ответ, необходим детальный анализ ситуации, при которой возникла инсулинорезистентность, хотя зачастую это становится отдельной непростой задачей.
При неосложненной беременности или при развитии кратковременной реакции «респираторного взрыва», направленного на ликвидацию бактериальной инфекции, инсулинорезистентность представляет собой адаптивный, физиологически оправданный ответ. После родов или победы над инфекцией она проходит сама и не требует лечения.
Однако, по данным профессора-биолога Я. А. Александровского, хроническое повышение уровня сахара в крови само по себе, без инфекции способно вызвать «затяжной респираторный взрыв» у нейтрофилов, которые, скапливаясь вблизи стенок сосудов, способны их повредить. Поэтому при диабете возрастает риск развития сосудистых осложнений.
Иными словами, физиологическая воспалительная реакция по мере увеличения ее продолжительности приобретает патологические черты, и тогда ее действие направлено не столько против бактерий, сколько против сосудов.
Инсулинорезистентность рассматривают как предшественницу клинического проявления сахарного диабета 2-го типа, но она также может указывать на скрытое развитие опухолевого процесса.
В таких ситуациях необходима более детальная диагностика, причем во время обследования человек должен избегать факторов риска: избыточного и неправильного питания, малой физической активности, эмоционального стресса.
После обследования целесообразно корректировать устойчивость к инсулину с помощью бигуанидов, салицилатов и других противовоспалительных препаратов.
Нельзя не отметить удивительные открытия последних лет, сделанные в нескольких зарубежных лабораториях.
По данным профессора Гарвардской медицинской школы Ричарда Ходина, прием кишечной щелочной фосфатазы смягчает негативные последствия избыточного употребления жирной пищи (“Proceedings of the National Academy of Sciences”, 2013, 110, 17, 7003–7008, doi:10.1073/ pnas.1220180110).
Оказывается, некоторые представители кишечной микрофлоры могут поддерживать или подавлять развитие рака и диабета в организме хозяина.
Более того, микрофлора, способствующая развитию диабета, иногда передается от больной диабетом беременной к плоду и таким путем повышает риск развития этой патологии у ребенка. Влияние микрофлоры на развитие диабета сейчас интенсивно исследуют, будущее покажет, насколько справедливы предположения ученых и возможно ли их использовать на практике.
Феномен инсулинорезистентности многолик. Природа экономно использует один и тот же механизм для достижения разных целей: он обеспечивает и антибактериальную защитную реакцию «респираторного взрыва», и нормальное развитие плода. Увы, неправильный образ жизни провоцирует патологическое течение процесса, и тогда инсулинорезистентность способствует возникновению ожирения, рака или диабета.
Гиперинсулинизм
Содержание:
Гиперинсулинизм − эндокринное заболевание, при котором наблюдается повышенный синтез инсулина и постоянное снижение глюкозы. В результате развивается гипогликемия, это состояние грозит комой и летальным исходом.
Описание
Гиперинсулинизм может быть врожденным и приобретенным. Врожденный встречается довольно редко: им заболевает 1 ребенок на 50 тысяч. Приобретенная форма чаще поражает женщин. Зачастую патология протекает периодами: ремиссия сменяется острой фазой и наоборот.
Различают врожденную форму заболевания и приобретенную. Основной опасностью гиперинсулинизма считается поражение клеток головного мозга: вследствие малого количества глюкозы они не получают должного питания и работают неправильно.
Причины
К причинам врожденной формы патологии относят аномалии плода, генные мутации и т.д. К причинам приобретенногого гиперинсулинизма относятся:
- заболевания печени;
- неправильное питание (здесь актуально как переедание быстрыми углеводами, так и недостаточное питание);
- неправильное лечение сахарного диабета;
- гормональный сбой (приводит к неадекватной выработке нужных гормонов);
- неправильная работа определенных ферментов;
- опухоли поджелудочной железы.
Диагностика
Симптомы имеют выраженный характер: есть триада признаков, которые говорят о наличии у человека гиперинсулинизма. К ним оносят:
- Спонтанное снижение уровня глюкозы в крови после физической активности или натощак.
- В это время уроверь сахара не превышает 1,9 ммоль/л.
- Введение глюкозы останавливает приступ.
Основными диагностическими мероприятиями являются: определение уровня сахара и инсулина в крови, КТ или ангиография и т.д.
Лечение
Основным методом лечения гиперинсулинизма является правильно питание. Оно должно быть дробным и иметь в составе нужное количество белков, жиров и сахаров. В момент приступов человеку вводится нужное количество глюкозы. Питание должно быть дробным (5-6 дней), содержание быстрых сахаров снижается до минимума.
При опухолях поджелудочной железы проводится их хирургическое удаление. Это может быть как частичная резекция железы, так и полная. Восстановительный период характеризуется диетой с малым содержанием сахаров. Консервативное лечение при наличии опухоли проводится редко, только в неоперабельных случаях. Если новообразование злокачественное, показана химиотерапия.
Любое самостоятельное диагностирование и лечение опасно и может только усугубить ситуацию. Обратитесь к врачу, он назначит вам адекватное лечение.
Гиперинсулинизм
Гиперинсулинизм (гипогликемическая болезнь) — заболевание, характеризующееся приступами гипогликемии, обусловленными абсолютным или относительным повышением уровня инсулина.
Этиология, патогенез.
Опухоли островков Лангерганса (инсулиномы), диффузная гиперплазия (J-клеток поджелудочной железы, заболевания ЦНС, печени, внепанкреатические опухоли, секретирующие инсупинопсдобные вещества, опухоли (чаще соединительно-тканного происхождения), усиленно поглощающие глюкозу, недостаточная продукция контринсулярных гормонов. Гипогликемия приводит к нарушению функционального состояния ЦНС, повышению активности симпатико-адреналовой системы.
Симптомы, течение. Заболевают в возрасте 26–55 лет, чаще женщины.
Приступы гипогликемии возникают обычно утром натощак, после длительного голодания; а при функциональном гиперинсулинизме — после приема углеводов.
Физическая нагрузка, психические переживания могут являться провоцирующими моментами. У женщин вначале приступы могут повторяться только в предменструальном периоде.
Начало приступа характеризуется ощущением голода, потливостью, слабостью, дрожанием конечностей, тахикардией, чувством страха, бледностью, диплопией, парестезиями, психическим возбуждением, немотивированными поступками, дезориентацией, дизартрией; в дальнейшем наступают потеря сознания, клинические и тонические судороги, иногда напоминающие эпилептический припадок, кома с гипотермией и гипорефлексией. Иногда приступы начинаются с внезапной потери сознания. В межприступном периоде появляются симптомы, обусловленные поражением ЦНС: снижение памяти, эмоциональная неустойчивость, безразличие к окружающему, потеря профессиональных навыков, нарушения чувствительности, парестезии, симптомы пирамидной недостаточности, патологические рефлексы. Из-за необходимости частого приема пищи больные имеют избыточную массу тела.
Для диагностики проводят определение уровня сахара в крови, иммунореактивного инсулина и С-пептида (натощак и на фоне пробы с голоданием и глюкозотолерантного теста). Для топической диагностики используют ангиографию поджелудочной железы, ультразвуковое исследование, компьютерную томографию, ретроградную панкреатодуоденографию.
Лечение инсулиномы и опухолей других органов, обусловливающих развитие гипогликемических состояний, хирургическое. При функциональном гиперинсулинизме назначают дробное питание с ограничением углеводов, кортикостероиды (преднизолон по 5–15 мг/сут). Приступы гипогликемии купируют внутривенным введением 40–60 мл 40% раствора глюкозы.